2. 全军病理学研究所
2. Institute of Pathology, Southwest Hospital, Third Military Medical University, Chongqing, 400038, China
上皮样血管内皮瘤( epithelioid hemangioend-othelioma,EHE) 是一种少见的可发生于全身各处软组织、脏器等的血管源性低度恶性肿瘤。肺上皮样血管内皮瘤( pulmonary epithelioid hemangioend-othelioma,PEH) 是罕见的原发于肺的低度恶性肿瘤,在美国每年的发病率不超过300例,大约占所有血管源性肿瘤的1%[1];我国偶有散发病例报道。由于缺乏特异的临床表现及病理特征,临床上极易误诊[2],多部位发生时尤其易误诊为多发性转移瘤。 有学者统计发现,PHE的初次诊断正确率仅为25%。现回顾性分析2007- 2014年我院诊断的PHE病例资料,结合文献,进一步探讨PHE的临床特征、治疗及预后,以期提高对该病的认识和重视,降低漏诊及误诊率,进而提高该病的诊疗水平。
1 资料与方法收集2007-2014年我院确诊的6例PEH患者,其首要诊断均考虑肺癌或肺转移癌。患者年龄 30~59岁,平均49.8岁。其中男性1例,女性5例。6例患者均经纤维支气管镜或CT引导下穿刺活检获得病理诊断,并通过复诊及电话随访,随访时间为6个月至8 年,末次随访时间为2015年2月。6例患者的 基本资料、主要临床表现、治疗方案及随诊情况见表1。
| 病例 | 性别 | 年龄(岁) | 诊断时间 | 发病部位 | 症状 | 病程(月) | 治疗方案 | 末次随访 |
| 病例1 | 女 | 30 | 2012.05 | 肺、盆腔 | 干咳 | 6 | 顺铂化疗 | 存活 |
| 病例2 | 女 | 48 | 2014.10 | 肺、胸膜、骨 | 咳嗽、咳痰、活动后气促 | 9 | 口服依托泊苷 | 存活 |
| 病例3 | 女 | 59 | 2013.04 | 肺、肝 | 干咳 | 5 | 放弃 | 存活 |
| 病例4 | 女 | 45 | 2010.07 | 肺、肝、骨 | 骨痛 | 1 | 顺铂化疗 | 存活 |
| 病例5 | 女 | 59 | 2007.08 | 肺 | 体检发现 | - | 手术 | 存活 |
| 病例6 | 男 | 58 | 2009.02 | 肺、肝、胸膜 | 咳嗽、咳痰、活动后气促 | 14 | 放弃 | 去世 a |
| a: 患者自发病到去世约27个月 | ||||||||
6例PEH患者均为中青年,且女性居多。其中4例无明显临床症状,多是间断干咳,不易引起重视。2例累及胸膜的患者出现胸腔积液后,伴随有活动后气促;其中1例患者累及肋骨,以骨痛为首发症状。除1例体检发现外,患者病程平均为7(1~14)个月(表1)。胸部CT影像学提示:3例患者表现为双肺内多发大小不等结节影,结节边缘光整,直径均<1 cm;1例表现为左肺门占位性病变并左下肺不张,左侧胸腔积液;1例表现为单个肺部结节,直径约2 cm,边缘光整;1例表现为双肺散在团块影及斑片影,直径为2~4 cm,伴有双侧胸腔积液。6例患者中,2例结节中可见散在钙化灶,3例伴有纵膈淋巴结增多或增大。免疫组化结果提示:6例患者血管内皮相关标志CK、Vim、CD34、CD31、Ⅷ均为阳性,Ki67阳性率普遍偏低,提示恶性程度较低。随访提示患者预后较好,除1例患者去世(发病后约27个月去世)外,其余5例均存活。
2.2 典型病例病例2,女性,48岁,因“间断咳嗽、咳痰9个月,加
重伴左侧胸痛、活动后气促2个月”于2014年10月入院。患者于2014年1月因受凉后开始出现阵发性咳嗽、咳少量白色黏痰,未予重视。2014年7月以来咳嗽、咳痰加重,咳嗽时伴左侧胸痛,有活动后气促。2014年9月外院就诊,B超示:左侧胸腔积液。胸水检查:见较多间皮细胞及淋巴细胞。胸部CT提示左下肺包块,左侧胸腔积液。支气管镜活检病理提示成团异型小细胞,诊断为左肺癌伴胸膜转移。为求进一步明确治疗,我科门诊以“左肺癌伴胸膜转移”收入院。患者既往史、个人史、家族史无特殊。
入院后相关实验室检查:血、尿、便三大常规,肝肾功,心肌酶谱等未见明显异常;结核相关检查及多肿瘤标志物均阴性。胸部CT检查(图1A)提示:左肺门占位。左侧胸腔积液,左下肺不张。纵隔淋巴结增多。肝胆胰脾、肾上腺超声、头颅MRI等未见明显占位。SPECT/CT融合显像:左第9前肋(图1B)及右股骨近端(图1C)代谢异常活跃伴骨质破坏,考虑骨转移瘤。诊断为“左下肺癌伴多发转移癌(左胸膜、左第9肋骨、右股骨)”。行2次胸腔穿刺术及胸膜活检术,胸水常规检查结果提示渗出液,生化检查提示乳酸脱氢酶轻度升高。胸膜活检病理提示组织慢性炎。进一步对左下肺病灶行CT引导下经皮肺穿刺活检术,病理检查结果提示:慢性炎伴广泛坏死。为进一步明确诊断,对右股骨异常活跃部位(图1C)行CT引导下骨穿刺活检术。免疫组化染色:CK(-),TTF1(-),CK7(-),Ki67<10%,CgA(-),EMA(-),Syn(-);血管内皮标记(图2):CD31(+),CD34(+),Fli-1(+),ERg(+)。结合临床、影像学表现,诊断为(多发性)上皮样血管内皮瘤(低度恶性)。患者选择了口服依托泊苷化疗,目前仍在随访之中。
 |
| 图 1 多发性肺上皮样血管内皮瘤典型病例(病例2)胸部影像学及骨扫描图像 |
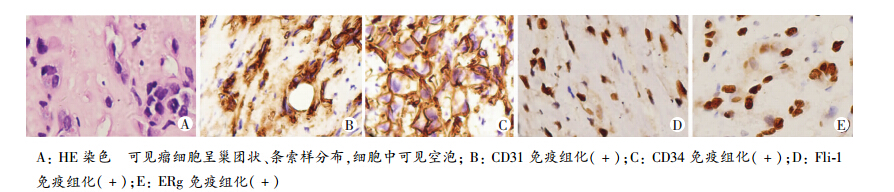 |
| 图 2 多发性肺上皮样血管内皮瘤典型病例(病例2)病理学表现(×400) |
1975 年,Dail等[3]首次报道了PEH病例。此后,又陆续证实在肝、骨、脑等部位也有血管内皮瘤的存在。1982年,Weiss等[4]证实该病变起源于血管内皮细胞,并第一次提出EHE的命名。目前普遍认为:EHE是一种交界性并有恶性倾向的肿瘤,临床生物学行为介于血管瘤和普通型血管肉瘤之间。2002年,WHO软组织和骨肿瘤病理学和遗传学分类将其归为恶性血管肿瘤。2004年,WHO 新版软组织肿瘤的分类中被定为低度恶性肿瘤。
3.1 临床表现目前,EHE患者病因学尚不清楚,可能与口服避孕药物、雌激素水平异常有关。EHE常累及软组织、骨、肺、肝等器官,大约50%的EHE表现为多器官发生[5],以肝、肺同时受累较为多见[6]。该肿瘤见于除小儿外的所有年龄组,发生于骨或软组织时,男女发病无性别差别,而发生于肝、肺器官则女性发病明显高于男性,比例约为1 ∶4[7],与本研究基本一致。多数患者可以无明显临床症状。常见症状是咳嗽、胸痛、呼吸困难,其他症状如胸腔积液、咯血、发热等,缺乏特异性症状,累及肋骨等部位时可有患处疼痛,累及胸膜产生胸腔积液后可有呼吸困难。男性患者出现临床症状较女性多见。实验室检查无特异性检测指标。
3.2 影像学特征PEH患者胸部CT常表现为双肺内大小不等的多发小结节影,沿肺小血管或小支气管周围生长。结节直径多<1 cm,边缘大多光整[8]。部分结节中央为凝固性坏死物质,可引起钙盐沉着并形成影像学可见的钙化灶,坏死物质排出后可出现空洞[9]。PEH可引起局灶性肺出血,故可见多发斑片影,是PEH 影像学特征之一[10]。侵及肋骨时可发现局部骨质破坏改变,局部膨胀,密度减低,内有分隔,可有病理性骨折。在影像学上,PEH 在诊断时需要与肺癌、肺结核、结节病、肺淋巴管肌瘤病、各种肉芽肿性疾病相鉴别,如果多部位同时出现,需特别注意与转移癌相互鉴别[11]。
3.3 病理学特征从组织学上看,PHE细胞具有上皮样细胞形态,圆形或不规则的短梭形,细胞内可见单个或多个空泡,这种单细胞原始空腔结构是血管内皮细胞的特征。瘤细胞常排列成大小不一的巢团状、条索样结构,呈树枝状生长。肿瘤组织中可见坏死、钙化及炎性细胞浸润。沈湘萍等[12]报道部分PEH患者肺泡腔内见大量含铁血黄素沉着。免疫组化检测结果显示:PHE细胞表达CD31、CD34、Ⅷ因子、Vimentin、CK 等血管内皮细胞标志,如CD34阳性率高达100%,Ⅷ因子阳性率达97.5%[13],需要与硬化性血管瘤、上皮样血管肉瘤、上皮样肉瘤等相互鉴别。早期有研究还报道PEH中20%雌二醇受体表达阳性。
3.4 治疗及预后PHE 患者病程进展缓慢,可长期生存,少数可局部或远处转移,5年生存率约为60%。组织学出现瘤细胞明显异型、显著的梭形细胞成分、病理学核分裂≥2 /10HPF 则提示预后不良。有学者从PEH患者的临床表现、影像学特征和预后进行统计分析,得出以下结论[14]:①有肺部结节但无症状的患者预后较好,中位生存时间可达180个月;②体质量减轻、贫血、胸腔积液均是PEH患者预后不良的预测因素。有血管内皮细胞增殖症状的患者(肺泡内出血等)预后较差;血性胸腔积液是提示血管侵袭和预后不良最重要的临床证据。另外,Amin等[15]则认为:男性、有咳嗽咯血胸痛等症状的患者、肺多发结节、胸膜渗出、多部位发生及淋巴结转移是提示肺EHE预后不良的重要危险因素,有症状患者、胸膜渗出是独立的生存率预测因子。但也有人认为肿瘤的转移或多部位发生并不影响患者预后。
目前尚无针对PEH的特殊治疗方法,对于单侧肺单发、多发但病灶较少的PEH患者,手术是首选的治疗方法。对多发无法手术切除者,可选择环磷酰胺、吉西他滨、卡铂等化疗药物治疗,但疗效并不十分确切。该病对放疗不敏感。另外,早期研究发现:激素治疗(如抗雌激素和孕激素)对表达雌激素或孕激素受体的PEH患者可能有效[16]。近年来,也有学者陆续报道了IFN-2α[17]、IFN-α[18]、沙利度胺[19]、贝伐单抗[20]等都可能在PEH的治疗中发挥一定作用,但多是个案报道或小样本临床研究,尚需更多的临床研究证实。由于PEH发病率低,呈散发分布,化疗方案对该病治疗的有效性和安全性尚缺乏足够的循证医学支持,需根据患者具体情况选择个体化治疗方案[21]。目前,随着该病越来越受到重视,国外已开始着眼于PEH的国际多中心临床研究,相信会有更多、更好的药物或治疗方案面世,服务于临床,服务于患者。
| [1] | Geramizadeh B, Ziyaian B, Dehghani M, et al. Prolonged hemoptysis caused by primary pulmonary epithelioid hemangioendothelioma; a case report and review of the literature. Iran J Med Sci, 2014, 39(2 Suppl): 223-227. |
| [2] | Kim M, Chang J, Choi H, et al. Pulmonary epithelioid hemangioendothelioma misdiagnosed as a benign nodule. World J Surg Oncol, 2015, 13: 107. |
| [3] | Dail D, Liebow A. Intravascular bronchioloalveolar tumor. Am J Pathol, 1975, 78(1): 6-7. |
| [4] | Weiss S W, Enzinger F M. Epithelioid hemangioendothelioma: a vascular tumor often mistaker for a carcinoma . Cancer, 1982, 50(5): 970-981. |
| [5] | Celikel C, Yumuk PF, Basaran G, et al. Epithelioid hemangioendothelioma with multiple organ involvement . APMIS, 2007, 115(7): 881-888. |
| [6] | Zhao X Y, Rakhda M I, Habib S, et al. Hepatic epithelioid hemangioendothelioma: A comparison of Western and Chinese methods with respect to diagnosis, treatment and outcome. Oncol Lett, 2014, 7(4): 977-983. |
| [7] | Mendlick M R, Nelson M, Pickering D, et al. Translocation t(1;3)(p36.3;q25) is a nonrandom aberration in epithelioid hemangioendothelioma. Am J Surg Pathol, 2001, 25(5): 684-687. |
| [8] | Cronin P, Arenberg D. Pulmonary epithelioid hemangioendothelioma: an unusual case and a review of the literature .Chest, 2004, 125(2): 789-793. |
| [9] | Jang K Y, Jin G Y, Lee Y C, et al. Pulmonary epithelioid hemangioendothelioma: a tumor presented as a single cavitary mass. J Korean Med Sci, 2003, 18(4): 599-602. |
| [10] | Engelke C, Schaefer-Prokop C, Schirg E, et al. High-resolution CT and CT angiography of peripheral pulmonary vascular disorders. Radiographics, 2002, 22(4): 739-764. |
| [11] | 陶梅梅, 周云芝, 王洪武. 肺上皮样血管内皮细胞瘤研究进展.中华医学杂志, 2012, 92(30): 2157-2159. |
| [12] | 沈湘萍, 张小伟, 许拯国.肺上皮样血管内皮瘤的临床病理分析: 附6例报告. 现代实用医学, 2014, 26(8): 1004-1005. |
| [13] | Mentzel T, Beham A, Calonje E, et al. Epithelioid hemangioendothelioma of skin and soft tissue: clinicopathologic and immunohistochemical study of 30 cases . Am J Sudy Pathol, 1997, 21(4): 363-374. |
| [14] | Bagan P, Hassan M, Le-Pimpec-Barthes F, et al. Prognostic factors and surgical indications of pulmonary epithelioid hemangioendothelioma: a review of the literature . Ann Thorac Surg, 2006, 82(6): 2010-2013. |
| [15] | Amin R M, Hiroshima K, Kokubo T, et al. Risk factors and independent predictors of survival in patients with pulmonary epithelioid haemangioendothelioma. Review of the literature and a case report. Respirology, 2006, 11(6): 818-825. |
| [16] | Singhal S, Jain S, Singla M, et al. Multifocal epitheloid hemangioendothelioma of liver after long-term oral contraceptive use:a case report and discussion of management difficulties encountered. J Gastrointest Cancer, 2009, 40(1/2): 59-63. |
| [17] | Roudier-Pujol C, Enjolras O, Lacronique J, et al. Multifocal epithelioid hemangioendothelioma with partial remission after interferon alpha-2a treatment. Ann Dermatol Venereol, 1994, 121(12): 898-904. |
| [18] | Demir L, Can A, Oztop R, et al. Malignant epithelioid hemangioendothelioma progressing after chemotherapy and Interferon treatment: a case presentation and a brief review of the literature. J Cancer Res Ther, 2013, 9(1): 125-127. |
| [19] | Salech F, Valderrama S, Nervi B, et al. Thalidomide for the treatment of metastatic hepatic epithelioid hemangioendothelioma: a case report with a long term follow-up. Ann Hepatol, 2011, 10(1): 99-102. |
| [20] | Stacher E, Gruber-Mosenbacher U, Halbwedl I, et al. The VEGF-system in primary pulmonary angiosarcomas and haemangioendotheliomas: new potential therapeutic targets? . Lung Cancer, 2009, 65(1): 49-55. |
| [21] | Kpodonu J, Tshibaka C, Massad M G. The importance of clinical registries for pulmonary epithelioid hemangioendothelioma. Chest, 2005, 127(5): 1870-1871. |



