骨化性肌炎是由于损伤或出血引起的骨骼肌、韧带、腱鞘、脂肪组织、结缔组织中出现的一种异位骨化[1]。骨化性肌炎是肘关节术后的主要并发症之一,严重时会导致肘关节功能障碍[2]。非甾体类抗炎药(non-steroidal anti-inflammatory drugs,NSAIDs)以及放射治疗是预防骨化性肌炎发生的常用方法[3, 4],这两种方法联合治疗已在预防髋臼骨折术[5]后和全髋关节置换术[6]后异位骨化中取得更佳疗效,但联合治疗对预防肘关节术后骨化性肌炎的疗效少见报道,更缺少联合治疗与单一治疗之间的对比研究。本研究回顾性分析塞来昔布及局部放疗联合疗法与单一疗法预防肘关节术后骨化性肌炎的早期疗效。
1 资料与方法 1.1 一般资料2008-2012年我院收治的肘关节外伤患者325例,筛选后纳入本研究并进行有效门诊随访者244例,其中肘关节骨折患者194例,肘关节脱位患者31例,肘关节骨折合并脱位患者19例。根据预防骨化性肌炎发生的治疗方案不同,分为塞来昔布组77例、局部放疗组65例、联合治疗组102例。
纳入标准:X线结合临床诊断为肘关节脱位或(和)肱骨远端骨折、尺骨鹰嘴骨折、尺骨冠状突骨折、桡骨小头骨折,就诊时间为24 h之内,入院前未接收其他治疗且年龄大于18周岁,肱骨远端骨折患者采用钢板内固定者。排除标准:既往有肘部外伤或畸形,有其他急、慢性疾病者,有药物过敏史及对本药过敏者,孕妇及哺乳期妇女,不能坚持治疗或不能坚持随访者。
1.2 治疗方法肘关节脱位的复位方法及外固定时间均相同,肘关节骨折除桡骨小头骨折外都采取钢板内固定,桡骨小头骨折采用皮质骨螺钉或钢板螺钉固定。各组患者均予以骨科术后常规护理和治疗,未使用镇痛泵,建议使用冰敷。术后给予石膏外固定制动2周,在此期间鼓励患者主动伸屈、旋转,不允许被动锻炼,床头置功能锻炼计时卡,前1周建议患者每2~3 h主动锻炼1次,每次不少于5 min,每天不少于5次,由患者本人或家属记录;2周后由主管医师制定轻度循序渐进负重锻炼计划。
放射治疗组和联合治疗组患者术前4 h之内对肘关节进行前后或左右对穿照射,单次放疗总剂量 7 Gy;药物治疗组和联合治疗组患者术后第1天开始 口服塞来昔布,200 mg/次,1 次/d,餐后服药,持续15 d。
1.3 评价指标最后1次随访时根据美国特种外科医院(hospital for special surgery,HSS)肘关节功能评分、疼痛数字评价量表(numerical rating scale,NRS)评分、肘关节活动度(range of motion,ROM)、影像学表现进行疗效评价,并记录术后不良反应。HSS评分是一种与临床实际结合较好的肘关节功能评价方法[7]。肘关节活动度以肘关节屈伸弧度表示。X线片可见软组织内不规则钙化化影,呈云雾状环形钙化或棉絮样模糊阴影,或外周骨化明显致密、轮廓清楚、中央透亮,但无骨髓受侵和骨膜反应认定为骨化性肌炎。不良反应主要记录药物过敏情况、胃肠道不良反应、凝血功能、肾功能、软组织反应或伤口愈合不良等。
1.4 统计学分析采用SPSS 19.0统计软件,计量资料以 x±s 表示,多样本均数比较采用单因素方差分析,进一步用LSD和SNK-q检验进行两两比较;计数资料采用χ2检验。
2 结果 2.1 入选病例一般情况的比较研究对象的年龄、性别、外伤类型、随访时间差异无统计学意义(P>0.05,表1),具有可比性。
| 组别 | n | 年龄(岁) | 性别
(男/女,例) |
外伤类型
(骨折/脱位/ 骨折合并 脱位,例) |
随访时间
(月) |
| 塞来昔布组 | 77 | 39.6±15.8 | 53/24 | 63/9/5 | 17.30±5.75 |
| 局部放疗组 | 65 | 41.1±17.6 | 46/19 | 53/8/4 | 16.12±4.41 |
| 联合治疗组 | 102 | 38.6±16.9 | 66/36 | 78/14/10 | 16.79±4.98 |
| P值 | 0.646 | 0.690 | 0.865 | 0.392 |
联合治疗组HSS评分高于塞来昔布组(P < 0.01)和局部放疗组(P < 0.05);各组NRS评分差异无统计学意义(P>0.05);联合治疗组肘关节活动度大于塞来昔布组(P < 0.01)和局部放疗组(P < 0.05,表2)。
| 组别 | HSS评分 | NRS评分 | ROM(°) |
| 塞来昔布组 | 89.61±9.62 a | 1.81±0.92 | 116.36±23.81 c |
| 局部放疗组 | 89.92±9.21 b | 1.85±0.91 | 117.23±17.96 d |
| 联合治疗组 | 93.04±6.68 | 1.62±0.78 | 124.02±15.61 |
| P值 | 0.011 | 0.177 | 0.015 |
| a:P=0.007,b:P=0.020,c:P=0.009,d:P=0.026,与联合治疗组比较 | |||
塞来昔布组4例患者(5.19%)、局部放疗组2例患者(3.08%)、联合治疗组1例患者(0.98%)发生骨化性肌炎,但各组之间骨化性肌炎发生率差异无统计学意义(P=0.266)。
2.4 不良反应各组均未出现因服用塞来昔布而导致的胃肠道反应及其他器官的不良反应或因局部放疗而导致的骨折不愈合和恶性肿瘤等。
2.5 典型病例典型病例1:患者,男性,28岁,入院诊断:左桡骨小头骨折;手术术式:切开复位植骨内固定术;塞来昔布联合局部放疗(治疗方案同1.2描述),术后6个月随访,患者恢复正常体力劳动,伸屈、旋转活动度和健侧相同(图1)。典型病例2:男性,19岁,入院诊断:左尺骨鹰嘴骨折;手术方式:切开复位内固定术;塞来昔布联合局部放疗,术后9个月拆除内固定物,患肘完全恢复正常活动度(图2)。
 |
| 图 1 左桡骨头骨折并肘关节脱位术后及术后6个月影像学改变及功能位像 |
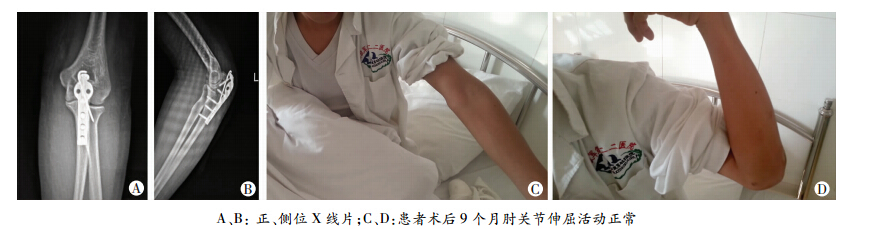 |
| 图 2 左尺骨鹰嘴骨折并肘关节脱位术后9个月影像学检查及功能位像 |
肘关节骨化性肌炎是在肘关节脱位或肘关节骨折后出现的一种异位骨化。肘关节外伤导致血肿形成或骨质创伤,引起前列腺素E2等炎性介质释放,促使肘关节周围骨形成蛋白(bone morphogenetic protein,BMP)转移到肌肉等损伤软组织中,软组织内血管周围的间充质细胞在骨形成蛋白的刺激下演变成骨母细胞、骨细胞,造成异位骨化[8]。骨化性肌炎一旦形成,会严重影响肘关节功能,此时药物干预或其他保守治疗疗效较差,往往等形成成熟骨化组织后再进行手术切除,但手术切除会增加患者尺神经麻痹、伤口感染等并发症的风险,同时造成二次损伤,骨化性肌炎复发率较高[2]。在骨化性肌炎形成前采取适当的干预措施显得非常必要。非甾体类抗炎药以及放射治疗是预防骨化性肌炎发生的常用方法[6]。
非甾体类抗炎药通过抑制环氧化酶阻止前列腺素的合成,减轻局部组织炎症反应,并可抑制间充质细胞向成骨细胞分化,从而达到预防异位骨化形成的作用[9]。地塞米松和β甘油磷酸钠可诱导人骨髓间充质干细胞分化为矿化成骨细胞,而地塞米松、3-异丁基-1-甲基黄嘌呤(IBMX)和吲哚美辛则诱导人骨髓间充质干细胞分化为脂肪细胞[10]。吲哚美辛通过激活过氧化物酶体增殖物激活受体γ1(peroxisome proliferator-activated receptor gamma,PPARγ),并上调PPARγ2表达,在诱导间充质干细胞分化为脂肪细胞中发挥重要作用[11],而塞来昔布亦可激活PPARγ[12]。Beckmann等[13]报道,常规给予萘普生能有效降低髋关节镜检查后异位骨化的发生率,但会导致个别病例出现急性肾衰、急性胃肠炎等不良反应。而选择性环氧酶2抑制剂在减少前列腺素E2生成的同时,对生理性前列腺素的影响较少,胃肠道不良反应较少。Lavernia等[14]报道塞来昔布能明显减低全髋关节置换术术后异位骨化的发生,且无明显不良反应。本研究中所有塞来昔布使用病例均为短期用药,未出现明显不良反应。
Blokhuis等[15]通过Mata分析发现放射治疗比吲哚美辛更能降低髋臼骨折术后异位骨化的发生率。放射治疗通过改变快速分化细胞的DNA结构,阻止多功能间充质细胞分化为成骨细胞的干细胞,从而有效地阻止局限性骨化性肌炎的形成[9]。Hoff等[16]对放疗预防髋部异位骨化的机制研究发现,放疗可能影响了局部免疫系统,进而抑制异位骨化。术前1~4 h或者 术后72 h内单次照射剂量总量7~8 Gy是最常使用的方法,术前放疗较术后放疗更加安全、舒适和便捷[17]。本研究采用术前局部照射,与塞来昔布组相比疗效无差异(P>0.05),未观察到放疗相关的不良反应。
虽然单一疗法都能有效预防创伤性骨化性肌炎的发生,但并不能完全阻止。非甾体类抗炎药和放疗的治疗机制不同,在预防骨化性肌炎的发生上具有协同效应。最近文献报道,放射治疗联合吲哚美辛预防髋关节术后异位骨化取得较好的疗效,未出现明显不良反应[5],但联合应用与单独应用任一治疗的疗效差异仍有待于进一步研究。本研究对比了塞来昔布及局部放疗联合疗法与单一疗法预防肘关节术后骨化性肌炎的临床疗效,联合疗法较单一疗法能明显改善肘关节HSS评分和肘关节活动度。虽然在骨化性肌炎的发生率上差异没有统计学意义,但是可以看出联合疗法有降低其发生率的趋势。本研究因骨化性肌炎病例较少,导致χ2检验理论频数太小,采用Fisher的精确检验后,差异无统计学意义(P>0.05)。以后可以扩大病例数,或者以具有异位骨化史或脑外伤等骨化性肌炎高危因素患者作为研究对象,采用随机对照研究联合治疗与单一疗法的差异,进一步明确联合疗法与单一疗法能否降低骨化性肌炎的发生率。
综上所述,塞来昔布联合局部放疗在改善肘关节术后肘关节功能和活动度方面优于塞来昔布或局部放疗的单一治疗,且无明显不良反应,值得临床推广。
| [1] | 周明旺, 李盛华. 创伤性骨化性肌炎的诊疗现状. 中国中医骨伤科杂志, 2009, 17(4): 67-69. |
| [2] | Salazar D, Golz A, Israel H, et al. Heterotopic ossification of the elbow treated with surgical resection: risk factors, bony ankylosis, and complications. Clin Orthop Relat Res, 2014, 472(7): 2269-2275. |
| [3] | 刘晓冬. 非甾体类药预防性治疗肘部外伤术后并发骨化性肌炎. 创伤外科杂志, 2011, 13(4): 322-323. |
| [4] | 王磊, 柴益民, 郑宪友. 放疗治疗肘关节异位骨化的疗效评价. 中国矫形外科杂志, 2010, 18(18): 1523-1525. |
| [5] | 王立江, 樊巍, 李兰涛, 等. 放射治疗联合吲哚美辛预防髋臼骨折术后异位骨化的临床研究. 中国药业, 2014, 23(11): 93-94. |
| [6] | Zeckey C, Hildebrand F, Frink M, et al. Heterotopic ossifications following implant surgery: epidemiology, therapeutical approaches and current concepts. Semin Immunopathol, 2011, 33(3): 273-286. |
| [7] | 范志航, 王子明, 杜全印, 等. 桡骨头切除与置换治疗难修复性桡骨头损伤的对比研究. 第三军医大学学报, 2014, 36(9): 950-954. |
| [8] | Pavlou G, Kyrkos M, Tsialogiannis E, et al. Pharmacological treatment of heterotopic ossification following hip surgery: an update. Expert Opin Pharmacother, 2012, 13(5): 619-622. |
| [9] | 吴江, 肖海军. 异位骨化的治疗新进展. 医学综述, 2012, 18(22): 3808-3811. |
| [10] | Bruedigam C, Driel Mv, Koedam M, et al. Basic techniques in human mesenchymal stem cell cultures: differentiation into osteogenic and adipogenic lineages, genetic perturbations, and phenotypic analyses. Curr Protoc Stem Cell Biol, 2011, Chapter 1: Unit1H.3. |
| [11] | Zhao X Y, Chen X Y, Zhang Z J, et al. Expression patterns of transcription factor PPARγ and C/EBP family members during in vitro adipogenesis of human bone marrow mesenchymal stem cells. Cell Biol Int, 2015, 39(4): 457-465. |
| [12] | Chu T H, Chan H H, Kuo H M, et al. Celecoxib suppresses hepatoma stemness and progression by up-regulating PTEN. Oncotarget, 2014, 5(6): 1475-1490. |
| [13] | Beckmann J T, Wylie J D, Kapron A L, et al. The Effect of NSAID Prophylaxis and Operative Variables on Heterotopic Ossification After Hip Arthroscopy. Am J Sports Med, 2014, 42(6): 1359-1364. |
| [14] | Lavernia C J, Contreras J S, Villa J M, et al. Celecoxib and heterotopic bone formation after total hip arthroplasty. J Arthroplasty, 2014, 29(2): 390-392. |
| [15] | Blokhuis T J, Frlke J P. Is radiation superior to indomethacin to prevent heterotopic ossification in acetabular fractures?: a systematic review. Clin Orthop Relat Res, 2009, 467(2): 526-530. |
| [16] | Hoff P, Rakow A, Gaber T, et al. Preoperative irradiation for the prevention of heterotopic ossification induces local inflammation in humans. Bone, 2013, 55(1): 93-101. |
| [17] | 张敏, 申文江, 高献书, 等. 肘关节松解术前放射治疗预防异位骨化形成.国际医学放射学杂志, 2011, 34(3): 215-218, 260. |



