2. 400016 重庆,重庆医科大学附属第一医院:神经内科,神经科学研究中心
2. Department of Neurology, Institute of Neuroscience, the First Affiliated Hospital of Chongqing Medical University, Chongqing, 400016, China
重症抑郁(major depressive disorder,MDD)是一种以显著而持久的心境低落、悲观消极为主要临床表现的情感障碍类疾病[1]。患者常伴有不典型躯体症状及认知功能损害,严重者甚至伴有自杀冲动并最终发展为自杀行为。随着患病率的增加及发病年龄提早,重症抑郁已经成为致死、致残的主要原因之一,带来了严重的社会及家庭负担[2]。研究认为抑郁症患者具有广泛的认知及社会功能的损害,涉及注意导向、行为抑制、策略制定、工作记忆编码等多个方面的功能异常[3]。对有明显社会及认知功能损害的患者,心理治疗是一种非常有效的治疗方法[4]。心理治疗通过倾听、解释、鼓励、安慰等方法帮助患者识别和矫正认知的曲解,改善患者人际交往能力和心理适应功能,减少患者的沉思及消极的自我反省。有研究显示与药物治疗相比,心理治疗具有更持久的抗抑郁作用,甚至可以降低远期的复发率[5]。随着功能磁共振成像技术的应用,对抑郁症及抗抑郁治疗相关神经机制的探索已成为研究的热点。
功能磁共振利用脑组织内血氧饱和度的变化间接地反映神经元活动,因此也被称作血氧水平依赖(blood oxygenation level dependent,BOLD)磁共振。1995年Biswal等首次证实静息状态下BOLD信号的低频波动与大脑神经活动密切相关[6]。电生理学研究显示BOLD信号的低频振荡反映了大脑静息状态下的神经元自发活动,是局部脑区之间信息交互产生的节律性活动,具有特定的生理意义。低频振幅(amplitude of low-frequency fluctuation,ALFF)的分析方法通过计算每个体素BOLD信号在0.01~0.08 Hz的振幅强度,间接地反映静息状态下具有生理意义的神经自发活动,在情感障碍类疾病中得到了广泛应用[7]。比率低频振幅(fractional ALFF)是对ALFF的进一步改进,可以更好地抑制生理噪声并对BOLD信号的改变更加敏感[8]。但是ALFF只能反映局部脑区神经自发活动的改变,而功能连接(functional connectivity,FC)研究脑区之间低频信号时间序列的同步性,这种脑区之间同步性反映了脑区之间的功能整合及网络属性,因此联合功能连接的分析方法能够更进一步探索大脑功能网络的改变。
之前的研究发现抗抑郁治疗能够改变局部的神经活动,使活动异常的区域回到正常基线水平[9]。在前期的DTI研究中,我们发现心理治疗早期额叶等区域白质纤维连接增强,表明心理治疗可能通过改变特定功能节点之间的连接来重塑整个情感网络[10]。此外,也有研究认为心理治疗与大脑自上而下的调节机制有关[11],即通过增强额叶对边缘系统的抑制功能促进皮层自上而下的认知控制从而发挥抗抑郁作用。目前抑郁症的功能磁共振研究有很多,但是纵向的抗抑郁治疗研究仍然十分缺乏[12],心理治疗的作用机制及认知模型仍未被完全揭示。因此,我们利用功能磁共振成像技术结合fALFF与功能连接的分析方法,探索抑郁症心理干预治疗早期静息状态下大脑自发活动及功能连接的改变,以及其中的神经调控机制。
1 材料与方法 1.1 研究对象本研究于重庆医科大学附属第一医院精神科门诊纳入重症抑郁干预治疗候选组共25例,其中2例因不能配合扫描被排除。抑郁症患者的诊断基于精神障碍的诊断与统计手册(dliagnostic and statistical manual of mental disorders 4th edition,DSM-IV),并使用汉密尔顿抑郁量表(Hamilton depression scale,HDRS)来评估疾病的严重程度。减轻标准为HDRS-17分数≤7并维持在7以下2周[13]。纳入的患者需排除以下情况:①患有其他精神疾病或神经系统疾病;②有头部外伤史或其他创伤性事件;③前4周正在服用抗抑郁药物;④精神活性药物滥用史;⑤左利手;⑥具有磁共振检查禁忌证。同期通过志愿者征集的方式招募了20名健康对照,遵循同样的排除标准。本研究经重庆医科大学伦理委员会批准,所有治疗过程均详细告知被试者并签署知情同意书。
1.2 数据采集纳入及诊断确立后所有被试进行基线水平的功能磁共振数据采集,然后对患者组进行为期4周的心理干预治疗,并再次进行磁共振数据采集。功能磁共振数据使用General Electric 3.0T磁共振扫描仪获取。T1结构像的扫描使用以下参数(TR=8.268 ms,TE=3.184 ms,翻转角=13°,视野=256 mm×256 mm,像素大小为1 mm×1 mm×1 mm)。功能数据采用梯度平面回波成像(EPI)技术,序列参数:(TR=2 000 ms,TE=30 ms,翻转角=90°,33层,体素大小=3.8 mm×3.8 mm×3.5 mm,每个被试扫描200个时间点),被试在扫描过程中放松闭眼,保持清醒。
1.3 干预治疗本研究由1名经验丰富的心理治疗师采用标准流程引导下的意象疗法[14]对抑郁症患者进行心理干预治疗,同期未服用抗抑郁药物。在治疗过程中,治疗师将引导患者做如下事情:①低频深呼吸;②逐步地对全身肌群进行肌肉放松;③在治疗师的引导下想象一些轻松舒适的场景或自然景观,并注意感受场景中令人愉悦的气味和声音等细节;④想象与自己信赖的人倾 诉,并让自己感到轻松有安全感。整个治疗旨在使患者置身于一种完全放松的氛围中,体验愉悦、积极的身心感受,建立积极正面的情感反馈。疗程结束后使用问卷对治疗的效果进行评分,从完全同意到完全不同意共5个等级,结果显示70%~80%的患者认为效果很好。
1.4 数据处理及分析所有数据使用SMP8(statistical parametric mapping)进行数据的预处理,处理步骤如下:①格式转换:将原始功能数据转化为NIFTI格式;②时间层校正:剔除前10个时间点以保证基线水平的稳定。通过时间层校正将所有层面校正到同一个时间点;③头动校正:首先我们估算出每个被试在扫描过程中的平动及转动,平动>2 mm或转动>2°的患者将会被剔除。其次由于ALFF的算法对扫描过程中的头动敏感,因此我们用Friston 24的方法进行头动的回归,同时我们还要将脑脊液,白质及全脑的信号进行回归;④空间标准化:通过12-参数的仿射变换将功能像配准到标准空间(MNI),并将每个体素重采样为3×3×3 mm3;⑤去线性漂移及平滑:最后进行平滑(FWHM=6 mm)及去除低频漂移。
ALFF的计算使用基于Matlab的REST软件(http://www.restfmri.net):①将每个体素去除线性漂移后的时间序列先经过0.01~0.08 Hz带通滤波器去除高频成分;②经快速傅立叶变化后得到频谱;③计算频谱的平方根即获得每个体素的ALFF值;④由于ALFF的分析方法容易受到头动及噪声的影响,因此将低频信号的值除以整个频段的信号强度得到fALFF,从而减少生理噪声的影响并提高特异性和敏感性[8]。
功能连接数据处理同样使用REST:①将治疗前后出现自发活动改变的脑区作为种子点;②提取治疗前后种子点的平均时间序列并与其他体素的时间序列进行相关性分析获得相关系数值;③将相关系数经过Fisher Z转化使之符合正态分布。
1.5 统计学分析首先使用SPSS 16.0统计软件进行独立样本t检验比较抑郁组及健康对照组的年龄及性别差异。之后使用REST软件(http://www.restfmri.net)中的统计分析模块进行基于全脑的双样本t检验(年龄、性别、灰质体积作为协变量)比较治疗前抑郁患者与健康对照之间的fALFF差异。使用配对t检验来分析治疗前后患者脑区自发活动的改变。使用Pearson相关分析评价差异区fALFF值与HRDS之间的相关性。使用单样本t检验显示与种子点功能连接显著的区域,然后使用配对t检验分析治疗前后功能连接的改变。统计结果均采用AlphaSim进行多重比较校正,体素水平 P<0.005、团块>21个连续体素被认为具有统计学意义。
2 结果 2.1 被试资料纳入抑郁症患者23例,健康对照20例。2组在性别(P=0.54)及年龄(P=0.63)方面差异无统计学意义。干预4周后,86.9%的患者症状减轻。
组别 | 性别 (男/女) | 年龄(岁) | 病程 (年) | HDRS评分 (治疗前/后) |
| 健康对照组 | 8/12 | 28.8±8.7 | - | - |
| 抑郁症患者组 | 7/16 | 27.7±10.9 | 16.4±13.4 | 21.8±6.4/ 4.5±3.5 |
| χ2/t值 | 0.54 | -0.49 | - | -13.09 |
| P值 | - | 0.63 | - | <0.01 |
与健康对照相比,抑郁患者两侧眶额叶皮层及右侧中央旁小叶的fALFF显著升高(图 1,表 2)。
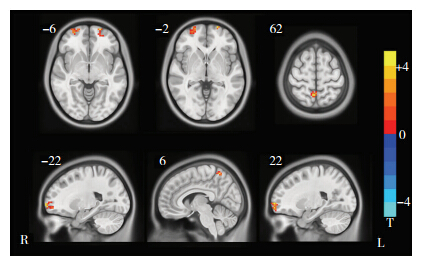 |
| 上下排分别为横轴位和矢状位显示,图像左上方数字为层面所在MNI坐标系中的坐标值,色卡颜色代表双样本t检验的t值图 1 治疗前抑郁患者较健康对照fALFF升高的区域(红色区域) |
| 脑区a | MNI 坐标b | 体素 | BA 分区c | 最大 t值 | |||||
| X | Y | Z | |||||||
| 治疗前fALFF>健康对照的区域 | |||||||||
| 右侧眶额叶皮层 | 21 | 66 | -9 | 65 | 11 | 4.57 | |||
| 左侧眶额叶皮层 | -21 | 66 | -6 | 37 | 11 | 4.75 | |||
| 右侧中央旁小叶 | 3 | -54 | 63 | 26 | 5 | 4.56 | |||
| 治疗后fALFF<治疗前的区域 | |||||||||
| 背侧前扣带回 | 0 | 9 | 48 | 28 | 24 | -4.43 | |||
| 膝下前扣带回 | 6 | 27 | 3 | 23 | 25 | -4.42 | |||
| 治疗后与背侧前扣带回FC增强的区域 | |||||||||
| 右侧额中回 | 42 | 21 | 42 | 55 | 9/44 | 4.95 | |||
| 治疗后与膝下扣带FC增强的区域 | |||||||||
| 左侧辅助运动区 | -12 | 0 | 54 | 26 | 6 | 4.07 | |||
| a: t检验显示差异有统计学意义的脑区,AlphaSim校正:体素水平P<0.005,团块>21个连续体素;b: t检验显著性最大的体素的MNI坐标;c:脑区所在的布罗德曼分区 | |||||||||
治疗后患者背外侧前扣带回、膝下扣带的fALFF显著降低,未发现治疗后fALFF显著升高的区域(图 2,表 2)。
 |
| 上排为轴位显示,下排为矢状位显示,图像左上方数字为层面所在MNI坐标系中的坐标值,色卡颜色代表配对t检验的t值图 2 治疗后抑郁患者fALFF降低的脑区(蓝色区域) |
将治疗后有显著差异的脑区设定为模板,提取其时间序列与HDRS量表及治疗缓解率(用治疗前后HDRS的差值除以治疗前的HDRS评分)做相关,结果显示治疗后膝下扣带(BA25)fALFF值与治疗后的HDRS评分显著正相关(P=0.015,r=0.498),与疾病的缓解率显著负相关(P=0.039,r=-0.434),其余脑区与临床评分无显著相关性。
功能连接结果显示治疗之后膝下扣带与左侧辅助运动区(BA25)的部分区域功能连接显著增强,背侧前扣带回与右侧背外侧前额叶(BA9)的部分区域功能连接显著增强(图 3,表 2)。
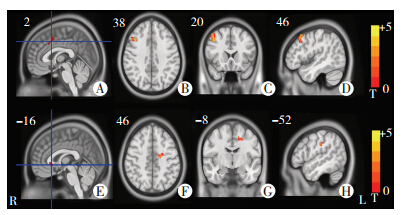 |
| A:以背侧前扣带回为种子点(十字线所示区域);B~D治疗后与背侧前扣带回功能连接增强脑区的轴、冠、矢状位;E:以膝下扣带为种子点(十字线所示区域);F~H治疗后与膝下扣带功能连接增强脑区的轴、冠、矢状位 色卡颜色代表配对t检验的t值图 3 治疗后抑郁患者大脑自发活动功能连接分析 |
本研究联合低频振幅及功能连接的方法探索抑郁症心理治疗早期大脑功能的改变以及相关的神经机制。静息状态是指在安静、放松、清醒但无系统思维活动及明显外部刺激的状态。研究认为大脑静息状态下的神经活动与自我意识、情感记忆等重要的认知功能有着极为密切的关系。对静息状态下大脑活动的研究能够反映脑功能网络的基础状态,具有重要的意义。并且静息状态下存在着各种神经协同活动,这些区域间的功能连接密切且具有很好的稳定性。研究显示抑郁患者存在多个脑区功能连接的异常,默认网络、扣带回等被认为是抑郁症情感环路失调的核心区域[3]。本研究中,4周干预后86.9%患者症状明显缓解。与健康对照组相比,抑郁症患者两侧眶额叶皮层及右侧中央旁小叶的fALFF显著升高,治疗后没有改变。治疗后,患者背侧前扣带回、膝下扣带的fALFF显著降低。治疗后膝下扣带与左侧辅助运动区、背侧前扣带回与右侧背外侧前额叶的部分区域功能连接显著增强。
心理治疗通过改变抑郁症患者的认知及情绪的处理,使患者能够过滤负面的情绪,纠正患者的思维模式从而缓解抑郁症状[15]。Teasdale等[5]通过大样本的随机对照试验证实心理治疗除了作为药物治疗的补充,还能单独应用于急性期的抗抑郁治疗。并且与药物治疗相比心理治疗具有更持久的抗抑郁作用。在本研究中通过将正性的场景视觉化,让患者感受积极放松的情感反馈,纠正其悲观消极的情感偏曲,从而重建患者的认知及情感处理模式。值得注意的是本研究纳入的患者都是自愿参与心理治疗,说明患者比较容易接收或者更倾向于心理治疗,因此可能是本研究中患者缓解率较高的原因之一。
3.1 抑郁患者fALFF异常的区域及治疗后的改变与健康对照相比,抑郁症患者双侧眶额叶皮层的自发活动明显升高,但治疗后未下降。通常认为眶回与认知行为过程中的价值评估以及决策制定有关[16],眶回及尾状核组成的环路是联系前额叶与边缘系统的枢纽,在情感调节及情绪处理过程中具有重要的作用。任务态功能磁共振成像研究发现抑郁症患者对负性刺激的高敏感性可能导致了眶回自发活动及代谢的异常升高[17]。结构像的研究显示抑郁症患者眶回的灰质体积显著降低,并且眶回结构的改变和患者持久的情感障碍密切相关[18]。结合之前的研究我们推测眶回可能与大脑对情感及信息的处理有关,这个区域功能活动的异常可能导致了抑郁症患者对负面信息的偏曲及认知控制的失调。静息状态下眶回自发活动的升高可能是抑郁症患者特征性的(trait relate)神经影像改变。
在本研究中,经过4周的心理治疗,患者静息状态下前扣带回区域自发活动的改变最为显著。扣带回作为边缘叶的重要组成结构与前额叶、丘脑、纹状体等区域有着广泛的解剖连接。它是大脑认知处理过程中较高和较低的认知层级之间的桥梁或中介,从前额皮质中继自上而下认知调节,然后整合边缘系统的情感反馈至高阶认知中心[19]。此外前扣带回在内脏和自主神经的调节过程中及刺激下情感表达与调控中发挥关键作用。新的研究显示膝下扣带与背侧前扣带回对应着扣带回的情感与认知亚区,分别和情感的表达及认知信息的处理密切相关[3]。这一地区功能的紊乱可能引起执行控制、情感调节等高级认知活动的异常,导致悲观的反刍思维及消极的自我反省[20]。治疗后前扣带回自发活动的改变反映了大脑在治疗中对情绪调节环路的调控与重塑。考虑到治疗前扣带回区域并没有明显的自发活动的异常,因此,我们推测干预治疗不是仅仅恢复功能异常的区域,而是通过对一些关键的节点的调控来重塑情感相关的网络。
相关性分析结果显示:治疗后膝下扣带的活动强度与治疗后的HDRS 评分呈正相关(P=0.015,r=0.498),与疾病的缓解率呈负相关(P=0.039,r=-0.434)。即治疗后膝下扣带自发活动越低患者的症状改善越显著。这个结果与之前的抗抑郁症治疗研究比较一致,研究发现膝下扣带回的代谢或自发活动在治疗后下降[20],并且这种改变和预后密切相关[21]。此外膝下扣带还是深部脑刺激(deep brain stimulation,DBS)治疗的一个关键的靶向区域[22]。研究发现对膝下扣带和邻近白质的高频深部刺激不仅仅能够改变此区域的兴奋性,还能够调节与其他区域的功能连接从而改善抑郁症状[23]。结合之前的研究,越来越多的证据表明膝下扣带是抗抑郁治疗中的一个关键节点,治疗后膝下扣带fALFF的改变可能是潜在的影像学预后指标。
3.2 功能连接的改变及相应的神经调节机制之前的研究显示抑郁症涉及默认、凸显、中央执行等多个网络间功能连接的改变,不同功能网络的失调可能对应了不同的症状表现[24]。某些关键区域如前额叶或边缘系统的连接改变可导致认知及情绪调节的异常。心理治疗可通过调节额叶-边缘系统间的连接改善抑郁症状[25]。
本研究结果显示:治疗后膝下扣带与左侧辅助运动区、背侧前扣带回与右侧背外侧前额叶的功能连接显著增强。辅助运动区(supplementary motor area,SMA)与前额叶及扣带回均有广泛的纤维连接,它不仅参与运动功能的执行和调节,还是执行控制、冲突处理等高级认知功能的关键区域之一[26]。在我们早期的DTI研究中同样发现在干预治疗早期SMA区域的白质纤维各向异性分数增加,并且这种白质完整性的提高和抑郁症症状的缓解正相关[10]。因此,我们推测心理治疗能够通过增强sgACC与SMA之间的链接对大脑的认知控制及精神运动性功能进行调节,从而纠正患者的抑郁心理模式[27]。
前额叶被认为是情感处理的核心区域,其中背外侧前额叶(dorsolateral prefrontal cortex,DLPFC)通过认知控制参与情绪的调节,在执行控制及额叶对边缘系统的抑制功能中发挥关键作用[28]。之前研究证实DLPFC与背侧前扣带回(dorsal anterior cingulate cortex,dACC)间有非常紧密的功能连接,两者共同发挥额叶对边缘系统的抑制功能,是大脑自上而下(top-down)调节的核心区域[3]。Goldapple等[29]通过心理治疗与药物治疗的对比研究发现,抑郁症心理干预治疗具有独特的认知调节模式,即通过额叶、扣带回再到丘脑等皮质下区的自上而下的调控。本研究验证了之前的假设,心理治疗可以通过调节DLPFC与dACC之间的功能连接,增强额叶对边缘系统的抑制功能,发挥其自上而下的调节作用,从而重塑额叶的情感调节网络。
综上所述,抑郁症患者眶回的自发活动显著增高,可能导致了抑郁症患者偏向于负面信息并沉溺于悲观的抑郁状态。治疗后背侧前扣带回及膝下扣带的自发活动明显下降,其中背侧前扣带回与背外侧前额叶、膝下扣带与辅助运动区的功能连接治疗后显著增强。这种功能区间连接的改变反映了皮质-边缘系统间的交互作用,通过与扣带回功能连接的调控易化增强皮质的认知控制及情绪调节的功能。因此,我们推测有效的心理治疗可能不仅仅是改变孤立的功能异常的脑区,而是通过调节重要节点间功能的耦合及连接来重塑整个情感网络,改善抑郁患者对情感及负性信息的处理能力。在此过程中扣带回是抑郁症患者功能网络改变的核心组成部分,而大脑自上而下的调节模式可能是心理治疗通路中的重要机制。治疗后膝下扣带fALFF的改变是潜在的影像学预后指标。
| [1] | Cooper J E. On the publication of the Diagnostic and Statistical Manual of Mental Disorders: Fourth Edition (DSM-IV)[J]. Br J Psychiatry, 1995, 166(1): 4-8. |
| [2] | Kessler R C, Berglund P, Demler O, et al. The epidemiology of major depressive disorder: results from the National Comorbidity Survey Replication (NCS-R)[J]. JAMA, 2003, 289(23): 3095-3105. |
| [3] | Pizzagalli D A. Frontocingulate dysfunction in depression: toward biomarkers of treatment response[J]. Neuropsychopharmacology, 2011, 36(1): 183-206. |
| [4] | DeRubeis R J, Siegle G J, Hollon S D. Cognitive therapy versus medication for depression: treatment outcomes and neural mechanisms[J]. Nat Rev Neurosci, 2008, 9(10): 788-796. |
| [5] | Teasdale J D, Segal Z, Williams J M. How does cognitive therapy prevent depressive relapse and why should attentional control (mindfulness) training help?[J]. Behav Res Ther, 1995, 33(1): 25-39. |
| [6] | Biswal B, Yetkin F Z, Haughton V M, et al. Functional connectivity in the motor cortex of resting human brain using echo-planar MRI[J]. Magn Reson Med, 1995, 34(4): 537-541. |
| [7] | 王晓霞, 蒋成刚, 张俐, 等. 抑郁症静息态脑功能异常及其与行为抑制/激活的关系[J]. 第三军医大学学报, 2014, 36(15): 1600-1603. |
| [8] | Zou Q H, Zhu C Z, Yang Y, et al. An improved approach to detection of amplitude of low-frequency fluctuation (ALFF) for resting-state fMRI: fractional ALFF[J]. J Neurosci Methods, 2008, 172(1): 137-141. |
| [9] | Buchheim A, Viviani R, Kessler H, et al. Changes in prefrontal-limbic function in major depression after 15 months of long-term psychotherapy[J]. PLoS One, 2012, 7(3): e33745. |
| [10] | Wang T, Huang X, Huang P, et al. Early-stage psychotherapy produces elevated frontal white matter integrity in adult major depressive disorder[J]. PLoS One, 2013, 8(4): e63081. |
| [11] | Singh M K, Gotlib I H. The neuroscience of depression: implications for assessment and intervention[J]. Behav Res Ther, 2014, 62: 60-73. |
| [12] | Dunlop B W, Binder E B, Cubells J F, et al. Predictors of remission in depression to individual and combined treatments (PReDICT): study protocol for a randomized controlled trial[J]. Trials, 2012, 13: 106. |
| [13] | Caetano S C, Kaur S, Brambilla P, et al. Smaller cingulate volumes in unipolar depressed patients[J]. Biol Psychiatry, 2006, 59(8): 702-706. |
| [14] | Watanabe E, Fukuda S, Shirakawa T. Effects among healthy subjects of the duration of regularly practicing a guided imagery program[J]. BMC Complement Altern Med, 2005, 5: 21. |
| [15] | Clark L, Chamberlain S R, Sahakian B J. Neurocognitive mechanisms in depression: implications for treatment[J]. Annu Rev Neurosci, 2009, 32: 57-74. |
| [16] | Padoa-Schioppa C, Assad J A. Neurons in the orbitofrontal cortex encode economic value[J]. Nature, 2006, 441(7090): 223-226. |
| [17] | Liu J, Blond B N, van-Dyck L I, et al. Trait and state corticostriatal dysfunction in bipolar disorder during emotional face processing[J]. Bipolar Disord, 2012, 14(4): 432-441. |
| [18] | Scheuerecker J, Meisenzahl E M, Koutsouleris N, et al. Orbitofrontal volume reductions during emotion recognition in patients with major depression[J]. J Psychiatry Neurosci, 2010, 35(5): 311-320. |
| [19] | Greicius M D, Flores B H, Menon V, et al. Resting-state functional connectivity in major depression: abnormally increased contributions from subgenual cingulate cortex and thalamus[J]. Biol Psychiatry, 2007, 62(5): 429-437. |
| [20] | Mayberg H S. Targeted electrode-based modulation of neural circuits for depression[J]. J Clin Invest, 2009, 119(4): 717-725. |
| [21] | Siegle G J, Thompson W K, Collier A, et al. Toward clinically useful neuroimaging in depression treatment: prognostic utility of subgenual cingulate activity for determining depression outcome in cognitive therapy across studies, scanners, and patient characteristics[J]. Arch Gen Psychiatry, 2012, 69(9): 913-924. |
| [22] | Morishita T, Fayad S M, Higuchi M A, et al. Deep brain stimulation for treatment-resistant depression: systematic review of clinical outcomes[J]. Neurotherapeutics, 2014, 11(3): 475-484. |
| [23] | Lozano A M, Giacobbe P, Hamani C, et al. A multicenter pilot study of subcallosal cingulate area deep brain stimulation for treatment-resistant depression[J]. J Neurosurg, 2012, 116(2): 315-322. |
| [24] | Sheline Y I, Price J L, Yan Z, et al. Resting-state functional MRI in depression unmasks increased connectivity between networks via the dorsal nexus[J]. Proc Natl Acad Sci U S A, 2010, 107(24): 11020-11025. |
| [25] | Kennedy S H, Konarski J Z, Segal Z V, et al. Differences in brain glucose metabolism between responders to CBT and venlafaxine in a 16-week randomized controlled trial[J]. Am J Psychiatry, 2007, 164(5): 778-788. |
| [26] | Nachev P, Kennard C, Husain M. Functional role of the supplementary and pre-supplementary motor areas[J]. Nat Rev Neurosci, 2008, 9(11): 856-869. |
| [27] | Cheng Y Q, Xu J, Chai P, et al. Brain volume alteration and the correlations with the clinical characteristics in drug-naive first-episode MDD patients: a voxel-based morphometry study[J]. Neurosci Lett, 2010, 480(1): 30-34. |
| [28] | Miller E K, Cohen J D. An integrative theory of prefrontal cortex function[J]. Annu Rev Neurosci, 2001, 24: 167-202. |
| [29] | Goldapple K, Segal Z, Garson C, et al. Modulation of cortical-limbic pathways in major depression: treatment-specific effects of cognitive behavior therapy[J]. Arch Gen Psychiatry, 2004, 61(1): 34-41. |



