3,3-二吲哚基甲烷是来自于蔬菜当中的一种天然化合物,能够诱导结直肠癌细胞的凋亡和保护DNA免于损伤[1]。3,3-二吲哚基甲烷是一种芳香烃受体(AhR)的配体,近年来在抗癌方面被广泛研究。AhR作为一种保守的核转录因子广泛地存在于大多数细胞当中,伴有许多重要的作用。已有研究报道在癌组织中许多生长因子及其受体高表达,影响着癌细胞的增殖,其中就包括角质细胞生长因子(KGF)和角质细胞生长因子受体(KGFR)[2]。近年研究发现人和鼠的KGFR能够受E2F1转录因子的直接调控[3],而AhR能通过周期蛋白调节E2F1的活性[4]。因此我们假设配体活化的AhR能够调节KGFR的表达,从而影响癌细胞的增殖。本实验探究被AhR内源性激动剂FICZ活化的AhR对KGFR表达的调节以及对结肠癌细胞增殖的影响。
1 材料与方法 1.1 材料与试剂6甲酰基吲哚并[3,2-b]咔唑(6-formylindolo [3,2-b] carbazole,FICZ)(美国Enzo LifeSciences公司),CH223191(德国CalBioChem公司),KGF(北京博奥森技术有限公司),GAPDH抗体(Goodhere Biotechnology),CYP1A1抗体(武汉三鹰技术有限公司),KGFR抗体(美国Stanta公司),AhR抗体(美国Abcam公司)。激光共聚焦显微镜(德国徕卡显微镜公司),Image Station 4000R(美国柯达公司)及化学发光增强剂ECL(武汉博士德生物有限公司)。
1.2 细胞培养LoVo细胞从ATCC细胞库购买并培养在1 ∶1 DMEM/Ham’s F-12 培养基中(含10%胎牛血清,加入适量的抗生素-青霉素50 U/mL和链霉素50 U/mL)。培养基每2天换1次液。待细胞长到90%时用胰酶消化传代或直接用于实验。Caco-2细胞同样从ATCC细胞库购买并培养在DMEM基础培养基中(含20%胎牛血清,加入适量的抗生素-青霉素50 U/mL和链霉素50 U/mL)。培养基1周更换2次液。待细胞长到90%时用胰酶消化传代或直接用于实验。
1.3 细胞增殖实验将细胞以2×105/孔接种到6孔板,待细胞长到60%后将培养基替换成无血清的基础培养基,饥饿处理24 h后,将AhR激动剂FICZ(100 nm/L)和KGF(0、120 ng/mL)加入到培养基中36 h,收集细胞并使用细胞计数板人工计数,台盼蓝检测活细胞数。
1.4 RNA提取和荧光定量PCR细胞用PBS洗涤3次之后,加入1 mL TRIzol,室温放置5 min,轻轻吹打后移入离心管;然后加入氯仿(200 μL/mL),振荡混匀15 s,室温放置15 min;4 ℃ 12 000×g离心15 min;吸取上层水相,转移至另一离心管中;按0.5 mL/mL加入异丙醇混匀,室温放置5~10 min;4 ℃ 12 000×g离心10 min,弃上清,RNA沉于管底;加入75%乙醇(按1 mL 75%/mL),温和振荡离心管,悬浮沉淀;4 ℃ 8 000×g离心5 min,尽量弃上清;室温晾干5~10 min;适量DEPC双蒸水溶解样品。提取细胞的RNA,用NanoDrop分光光度计对RNA含量进行检测(μg/cm)。根据PrimeScript RT reagent kit (TaKaRa)试剂盒操作说明将RNA逆转录成cDNA。Rotor-Gene Q (Qiagen) 和SYBR_Premix Ex TaqTM Ⅱ(TaKaRa)用于荧光定量PCR。引物序列:KGFR上游5′-GAAACGGCTCGGGTTTCAGTGG-3′,下游 5′-CGAG-TTGCGAAGGCTCAGAGC-3′,293 bp;CYP1A1上游5′-CCATGTCGGCCACGGAGTT-3′,下游5′-ACAGTGCCA-GGTGCGGCTT-3′,174 bp;β-actin上游5′-CCACGA-AACTACCTTCAACTC-3′,下游5′-GTGATC TCCTTCTGCATCCTG-3′,132 bp。
1.5 细胞蛋白提取和Western blot检测倒掉培养基,预冷PBS清洗细胞3次,细胞刮刮脱细胞,收集至离心管,1 000 r/min离心5 min。洗涤后的细胞转移至洁净EP管,加入1 mL Lysis,Buffer(细胞裂解液)和1 μL PMSF(蛋白酶抑制剂)。混匀后冰上保存数分钟待用,移液器反复吹打,至蛋白析出。4 ℃摇床,温和振摇15 min。14 000 r/min,4 ℃离心15 min,上清即为细胞全蛋白提取物。BCA法测蛋白浓度。每孔上样25 μg蛋白进行聚丙烯酰胺凝胶电泳,然后将分离的蛋白转到聚偏氟乙烯膜上,将膜放入5%脱脂牛奶中封闭1 h后,孵育AhR抗体(1 ∶500)、CYC1A1抗体(1 ∶1 000)、KGFR抗体(1 ∶200)、GAPDH抗体(1 ∶1 000)过夜,第2天用PBS洗涤3次,最后孵上二抗1 h,再洗涤3次。对膜蛋白条带进行检测。
1.6 免疫荧光检测将细胞接种在荧光共聚焦培养皿中,待细胞长到60%时DMSO或(100 nmol/L)FICZ添加到培养皿当中。细胞被刺激12 h后,单层细胞用PBS洗涤两遍后用4%的甲醇固定10 min。再次洗涤细胞两遍后用0.1% Triton X-100破膜10 min,然后用10%的脱脂牛奶封闭1 h,AhR抗体(1 ∶100)孵育4 ℃过夜。第2天细胞洗涤3次后,FITC共轭的羊抗兔抗体(1 ∶200,boster)加入荧光共聚焦培养皿 1 h避光,DAPI染核5 min,成像。
1.7 临床样本收集新鲜结直肠癌样本从新桥医院普通外科获得。收集样本前向患者说明情况,经患者同意并签署知情同意书。收集的组织标本均来自接受手术的结直肠癌患者。新鲜组织取出后一部分组织用多聚甲醛固定,一部分立即提取RNA。研究得到第三军医大学(中国,重庆)伦理委员会批准。
1.8 免疫组化组织石蜡切片经二甲苯脱蜡和系列乙醇浓度梯度水化后,用PBS(0.l mol/L,pH 7.4)冲洗3次,每次5 min; 0.3%过氧化氢室温孵育10 min;PBS冲洗切片,3 min×3次;10%山羊血清封闭,置于湿盒内,室温封闭10 min;切片加一抗KGFR(1 ∶100),置于湿盒内,4℃过夜;PBS冲洗切片,3 min×3次;切片加生物素标记的IgG二抗,1 ∶200稀释,室温孵育15 min;PBS冲洗切片,3 min×3次;切片加辣根酶标记链霉卵白素工作液,室温孵育15 min;PBS冲洗切片,3 min×3次;切片加100 μL新鲜配制的DAB溶液30~60 s。自来水冲洗,终止显色反应;苏木精复染,95%乙醇脱色: 二甲苯透明,1 min×3次;室温下风干后,中性树胶封片;用光镜观察。
1.9 统计学分析采用SPSS 1.0统计软件,计量资料数据用 ±s表示,各组间比较采用t检验。
2 结果 2.1 患者一般资料12例结直肠癌患者,包括男性10例,女性2例,≤60岁8例,>60岁4例,平均年龄57岁。部位:结肠4例,其中男性3例,女性1例;直肠8例,其中男性6例,女性2例。
2.2 结直肠癌组织中KGFR高表达12例结直肠癌患者的肠道组织KGFR蛋白阳性染色主要分布在肠道上皮细胞,呈棕黄色颗粒状(图 1)。进一步荧光定量PCR显示,12个临床样本中有11个癌组织的KGF表达量明显高于对应的正常组织,8个癌组织样本中KGFR表达量显著增高。
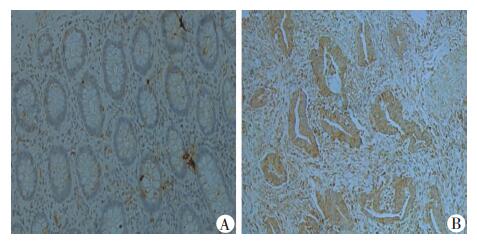 |
| A:正常结直肠组织中;B:结直肠癌组织中 图 1 免疫组化定位KGFR在结直肠正常组织和相应癌组织中的表达(S-P ×100) |
AhR在未激动下主要分布于细胞质,少数处于细胞核(图 2)。CYP1A1作为AhR的靶向基因,已被广泛用于衡量AhR的活性。如图 3,AhR内源性配体FICZ(1、10、100、1 000 nmol/L)刺激12 h后,LoVo细胞和Caco-2细胞中CYP1A1的蛋白水平显著增高。然而,AhR蛋白的表达水平明显降低,可能由于AhR在发挥功能后被快速地降解。
 |
| A:在LoVo细胞中的分布;B:在Caco-2细胞中的分布 图 2 免疫荧光检测AhR在LoVo细胞和Caco-2细胞中的分布(×800) |
 |
|
1:对照组;2:FICZ(1 nmol/L)处理组;3:FICZ (10 nmol/L) 处理组;4:FICZ(100 nmol/L)处理组;5:FICZ(1 000 nmol/L) 处理组 A:LoVo细胞中FICZ能够活化AhR;B:Caco-2细胞中FICZ能够活化AhR 图 3 蛋白免疫印迹检测LoVo细胞与Caco-2细胞中AhR下游靶向基因CYP1A1的表达 |
FICZ刺激LoVo细胞和Caco-2细胞12 h后收集细胞蛋白和RNA,发现在LoVo细胞中KGFR的蛋白 水平和mRNA水平在12 h分别降低了50%和58.8%。 在Caco-2细胞中分别降低了52.6%和62.5%(图 4、5)。提示在LoVo细胞和Caco-2细胞中,FICZ活化的AhR能够下调KGFR的表达。
 |
| 1:对照组;2:FICZ组 图 4 Western blot检测FICZ作用LoVo细胞12 h后KGFR RNA水平 |
 |
| 1:对照组;2:FICZ组 图 5 Western blot检测FICZ作用Caco-2细胞12 h后KGFR蛋白的表达 |
在LoVo细胞(图 6A)和Caco-2细胞中(图 6B),AhR抑制剂CH223191能够显著抑制AhR的活性,并且CH223191能够逆转FICZ引起的KGFR下调(图 7)。
 |
| 1:对照组;2:FICZ处理组;3:FICZ+(10 μmol/L) CH223191处理组;4: FICZ+(50 μmol/L)CH223191处理组 A:在LOVO细胞中;B:在Caco-2细胞中 图 6 在LOVO细胞与Caco-2细胞中CH223191抑制FICZ活化AhR |
 |
| 1:FICZ处理组;2:FICZ+50 μmol/L CH223191 4处理组 图 7 AhR抑制剂逆转FICZ引起的KGFR下调 |
血清饥饿处理结肠癌上皮细胞24 h后,用KGF(120 ng/mL)、 KGF+FICZ(100 nmol/L)刺激细胞36 h。在LoVo细胞中,对照组、KGF处理组、KGF+FICZ处理组和FICZ处理组的平均细胞数为(2.4×105±0.67,4.7×105±0.87,3.1×105±0.67,2.2×105±0.63),在Caco-2细胞中,对照组、KGF处理组、KGF+FICZ处理组和FICZ处理组的平均细胞数为(2.4×105±0.59,4.1×105±0.66,2.6×105±0.62,2.6×105±0.63)。表明,KGF能够促进结肠癌细胞增殖(1.9倍;Caco-2:1.6倍);FICZ能够降低KGF对癌细胞的增殖作用(LoVo:34%;Caco-2:37%)。
3 讨论本实验揭示了AhR和结肠癌细胞增殖之间有着紧密的联系。实验发现FICZ活化的AhR能够下调结肠癌上皮细胞表面的KGFR受体,从而降低癌细胞对KGF增殖的敏感性。研究证明KGF是一种重要的生长因子,其表达的增加与肿瘤的增殖密切相关[5, 6]。本研究显示在结直肠癌组织中KGF和KGFR显著的高表达。同时我们也发现另一种保守的核转录因子AhR也是高表达的。这一结果和Lin等[7]发现AhR在肺癌组织中过表达是一致的。这些结果表明AhR与肿瘤细胞的增殖可能有着密切的联系,同时癌组织中AhR的高表达可以以使得癌细胞对环境中AhR的各种配体敏感性增强,也使其可能成为干预癌细胞增殖的一个靶向分子。当前国内外对AhR的研究主要集中在炎症和肿瘤两个方面,在炎症方面,AhR具有显著的抗炎作用[8, 9]。在抗肿瘤方面,研究表明被配体活化的AhR能够通过下调细胞周期蛋白的表达来抑制多种癌细胞的增殖[10, 11, 12]。FICZ作为AhR内源性配体,在炎性损伤中具有显著的保护作用。本实验发现FICZ能够从mRNA和蛋白水平下调结肠癌上皮 细胞表面KGFR受体的表达。当前研究已经证明KGFR 抑制剂可能对癌症的治疗具有潜在的治疗作用[6]。人的FGFR1和鼠的FGFR2的表达受转录因子E2F1的直接调控[3],E2F1是一种调控细胞增殖的核转录因子,受到磷酸化的视网膜母细胞瘤蛋白(pRb)的调控。已有研究报道MAPK和细胞周期蛋白能够磷酸化Rb调节KGFR的表达[3]。因此配体活化的AhR可能是通过影响MAPK或周期蛋白的表达来调节Rb的磷酸化,进而影响E2F1的转录活性,最终调节KGFR的表达。传统AhR的抑制剂主要包括两种:黄酮3′-羟化酶(MNF)和6,2′,4′三甲氧基黄酮(TMF)[13]。近年,CH223191 作为一种新的AhR 抑制剂广泛的运用于研究当中[14, 15]。本实验揭示了CH223191 能够逆转FICZ引起的KGFR下调,说明FICZ引起的KGFR下调依赖于AhR;发现FICZ能够降低KGF对结肠癌上皮细胞的增殖作用。FICZ通过活化AhR从而下调KGFR的表达,并进一步减弱肠道癌细胞的增殖。该实验从体外研究了FICZ通过AhR下调结直肠细胞表面KGFR受体,降低了结直肠癌细胞对KGF增殖的敏感性。
| [1] | Yin X F, Chen J, Mao W, et al. A selective aryl hydrocarbon receptor modulator 3,3'-Diindolylmethane inhibits gastric cancer cell growth[J]. J Exp Clin Cancer Res, 2012, 31: 46. |
| [2] | Watanabe M, Ishiwata T, Nishigai K, et al. Overexpression of keratinocyte growth factor in cancer cells and enterochromaffin cells in human colorectal cancer[J]. Pathol Int, 2000, 50(5): 363-372. |
| [3] | D'Amici S, Ceccarelli S, Vescarelli E, et al. TNFalpha modulates Fibroblast Growth Factor Receptor 2 gene expression through the pRB/E2F1 pathway: identification of a non-canonical E2F binding motif[J]. PLoS One, 2013, 8(4): e61491. |
| [4] | Frauenstein K, Sydlik U, Tigges J, et al. Evidence for a novel anti-apoptotic pathway in human keratinocytes involving the aryl hydrocarbon receptor, E2F1, and checkpoint kinase 1[J]. Cell Death Differ, 2013, 20(10): 1425-1434. |
| [5] | Torres C, Perales S, Alejandre M J, et al. Serum cytokine profile in patients with pancreatic cancer. Pancreas[J], 2014, 43(7): 1042-1049. |
| [6] | Kesinger J W, Mehta M, Lerner M R, et al. Oncolytic potential of a novel KGFR tyrosine kinase inhibitor using a KGFR-selective breast cancer xenograft model[J]. Anticancer Res, 2015, 35(1): 47-52. |
| [7] | Lin P, Chang H, Tsai W T, et al. Overexpression of aryl hydrocarbon receptor in human lung carcinomas[J]. Toxicol Pathol, 2003, 31(1): 22-30. |
| [8] | Di-Meglio P, Duarte J H, Ahlfors H, et al. Activation of the aryl hydrocarbon receptor dampens the severity of inflammatory skin conditions[J]. Immunity, 2014, 40(6): 989-1001. |
| [9] | Ji T, Xu C, Sun L, et al. Aryl Hydrocarbon Receptor Activation Down-Regulates IL-7 and Reduces Inflammation in a Mouse Model of DSS-Induced Colitis[J]. Dig Dis Sci, 2015, 60(7):1958-1966. |
| [10] | Brinkman A M, Wu J, Ersland K, et al. Estrogen receptor alpha and aryl hydrocarbon receptor independent growth inhibitory effects of aminoflavone in breast cancer cells[J]. BMC Cancer, 2014, 14: 344. |
| [11] | Chang C C, Sue Y M, Yang N J, et al. 3-Methylcholanthrene, an AhR agonist, caused cell-cycle arrest by histone deacetylation through a RhoA-dependent recruitment of HDAC1 and pRb2 to E2F1 complex[J]. PLoS One, 2014, 9(3): e92793. |
| [12] | Xu G, Liu J, Yoshimoto K, et al. 2,3,7,8-tetrachlorodibenzo-p-dioxin (TCDD) induces expression of p27(kip1) and FoxO3a in female rat cerebral cortex and PC12 cells[J]. Toxicol Lett, 2014, 226(3): 294-302. |
| [13] | Murray I A, Flaveny C A, DiNatale B C, et al. Antagonism of aryl hydrocarbon receptor signaling by 6,2',4'-trimethoxyflavone[J]. J Pharmacol Exp Ther, 2010, 332(1): 135-144. |
| [14] | Choi E Y, Lee H, Dingle R W, et al. Development of novel CH223191-based antagonists of the aryl hydrocarbon receptor[J]. Mol Pharmacol, 2012, 81(1): 3-11. |
| [15] | Gadupudi G, Gourronc F A, Ludewig G, et al. PCB126 inhibits adipogenesis of human preadipocytes[J]. Toxicol In Vitro, 2015, 29(1): 132-141. |



