2.563003 贵州 遵义,遵义医学院第一附属医院:急诊科
2.Department of Emergency, First Affiliated Hospital, Zunyi Medical University, Zunyi, Guizhou Province, 563003, China
心血管疾病是严重威胁中老年健康的常见疾病。目前基础研究显示,慢性炎症是动脉粥样硬化性相关心血管疾病的主要病理机制。在动脉损伤和疾病中,血管平滑肌细胞(vascular smooth muscle cells,VSMCs)经历特异性的形态和功能改变,即细胞收缩表型和合成表型的转换,且细胞表型转换过程中,VSMCs涉及炎症激活,分泌多种促炎症介质,包括细胞因子、趋化因子和黏附分子,进而促进血管病理生理发展、疾病进展和最终不良临床事件发生。因此,识别调节VSMCs炎症反应机制对于动脉粥样硬化性心血管疾病研究具有重要意义。心肌素(myocardin)是一种潜在的肌源性共激活剂,特异性表达于成熟VSMCs和心肌组织中,涉及VSMCs表型调节和分化[1],是维持VSMCs自稳态所必需的因子[2]。本课题组先前研究显示,降钙素基因相关肽(calcitonin gene related peptide,CGRP)通过调节VSMCs表型改变而抑制体外培养的VSMCs增殖,但对于CGRP是否调节VSMCs炎症激活及相关机制尚未明确。本实验拟通过观察CGRP对体外培养的VSMCs中心肌素表达和炎症激活的影响,探讨CGRP对VSMCs炎症的调控作用。
1 材料与方法 1.1 材料雄性SD大鼠42只,体质量约100 g(约4周龄),购自遵义医学院实验动物中心(清洁级,批号ZMC201304Q)。IL-1β、CGRP、CGRP8-37(CGRP受体拮抗剂)以及抗大鼠心肌素抗体、IL-6抗体购自美国Abcam公司。高表达心肌素的腺病毒载体和干扰心肌素腺病毒载体由上海生物工程公司协助构建。其余试剂由遵义医学院中心实验室提供。
1.2 VSMCs培养与鉴定参考课题组前期实验方法[3]培养细胞,采用组织块贴壁法培养VSMCs;细胞免疫化学法对VSMCs中的α-actin进行鉴定;实验选用3~6代状态良好的VSMCs。
1.3 VSMCs分组培养与处理培养的VSMCs按实验要求分为对照组、IL-1β组、心肌素高表达组、心肌素干扰组和CGRP8-37组,其中IL-1β组为加入IL-1β处理;CGRP组为同时给予IL-1β 和CGRP处理;心肌素高表达组和心肌素干扰组为分别应用携带心肌素表达质粒或心肌素干扰质粒的腺病 毒载体转染VSMCs 24 h后再给予IL-1β处理; CGRP8-37组为给予IL-1β和CGRP处理的同时加入CGRP受体拮抗剂CGRP8-37。所有分组中IL-1β的应 用浓度为10 ng/mL,CGRP应用浓度为3.5×10-7 mol/L,CGRP8-37应用浓度为10.0×10-7 mol/L。
1.4 心肌素和炎症相关蛋白IL-6的检测采用Western blot检测各组细胞心肌素和炎症相关蛋白IL-6蛋白变化。方法简介:收集经CGRP处理后不同时间点VSMCs,提取细胞总蛋白,以50 μL上样,10%十二烷基硫酸钠(SDS)-聚丙烯酰胺凝胶电泳后将蛋白转移至硝酸纤维素膜上,用TBST配置的5%脱脂奶粉封闭2 h,分别封闭膜与IL-6(1 ∶1 000)单克隆抗体和心肌素多克隆抗体(1 ∶100)共孵育,4 ℃过夜,再与二抗共同孵育2 h(1 ∶5 000),显色曝光,实验重复3次。以β-actin 作为内参,利用伯乐凝胶成像系统分析各条带光密度值,计算各条带与内参条带的比值作为蛋白含量半定量分析。
1.5 统计学分析应用SPSS 16.0软件进行统计学分析。所有参数用x±s表示,组间比较采用单因素方差分析和t检验。检验水准α=0.05。
2 结果 2.1 VSMCs培养情况在VSMCs培养实验中,分离的胸主动脉组织块静置培养3~5 d后,光学显微镜下观察见组织块边缘有梭形排列的少量细胞生长,换液后继续培养至1周左右时细胞数目明显增多,呈放射性生长;传代培养后细胞呈单层或多层重叠生成,即典型“峰-谷”样生长。取第4~5代培养细胞行α-SMA和DAPI免疫荧光双染色鉴定,结果阳性细胞胞浆为绿色,胞核为蓝色;同时免疫细胞化学法染色α-SMA,阳性细胞细胞质为棕褐色,这提示培养细胞为VSMCs。
2.2 心肌素对炎症激活的VSMCs中IL-6表达的影响如图 1,在对照组VSMCs中,IL-6水平持续低水平表达,与基线0 h比较,各时间点IL-6水平无明显变化;以IL-1β诱导VSMCs炎症激活后,IL-1β组细胞IL-6表达水平逐渐增加,细胞培养24、48 h和72 h时IL-6水平较同时间点对照组增加(P<0.05);但心肌素高表达组中,以高表达心肌素的腺病毒载体转染VSMCs后再加入IL-1β处理,24、48 h和72 h时IL-6水平较IL-β组显著降低(P<0.05),而与对照组水平类似。
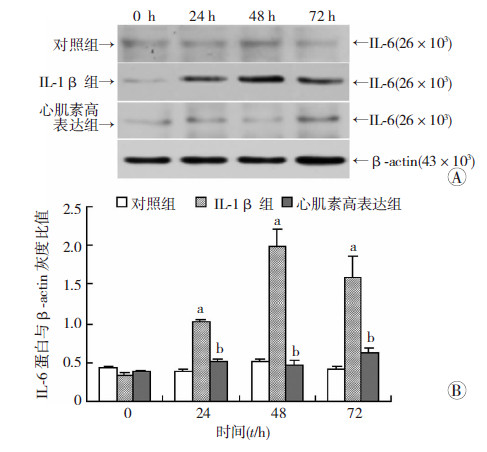 |
| A:Western blot检测VSMCs内IL-6蛋白水平;B:半定量分析(n=3, ±s);a:P<0.05,与对照组同时间点比较;b:P<0.05,与IL-1β组同时间点比较 图 1 不同分组处理对VSMCs中IL-6表达的影响 |
如图 2和表 1,在IL-1β组中,IL-1β处理VSMCs后细胞内IL-6表达水平显著增加,表现为24、48 h和72 h时IL-6水平均高于基线水平(P<0.05),而心肌素水平无显著变化;在CGRP组中,CGRP处理VSMCs后各个时间点细胞内心肌素水平较同时间点IL-1β组心肌素水平显著增加(P<0.05),而各个时间点细胞内IL-6表达水平较同时间点IL-1β组水平显著降低(P<0.05)。
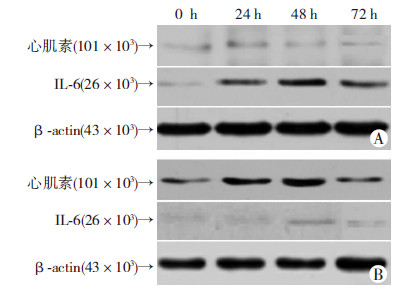 |
| A:对照组;B:CGRP组 图 2 Western blot检测CGRP对VSMCs中心肌素和IL-6表达的影响 |
| (与内参灰度比值,x±s,n=3) | ||||
| 时间点 | 对照组 | CGRP组 | ||
| 心肌素 | IL-6 | 心肌素 | IL-6 | |
| 0 h | 0.21±0.01 | 0.34±0.02 | 0.45±0.01 | 0.18±0.01 |
| 24 h | 0.25±0.03 | 0.77±0.03a | 1.17±0.03a | 0.23±0.01b |
| 48 h | 0.19±0.01 | 1.35±0.04a | 2.04±0.05a | 0.28±0.02b |
| 72 h | 0.28±0.02 | 1.04±0.04a | 0.96±0.02a | 0.20±0.02b |
| a:P<0.05,与同组0 h比较;b:P<0.05,与对照组同时间点比较 | ||||
如图 3和表 2,在CGRP组VSMCs中,CGRP抑制IL-1β诱导的细胞IL-6蛋白表达,表现为细胞培养的24、48和72 h时IL-6蛋白水平与基线水平比较,差异无统计学意义;但心肌素干扰组VSMCs中,CGRP处理后各个时间点IL-6水平较CGRP组显著升高(P<0.05);同样地,在CGRP8-37组VSMCs中,各个时间点细胞IL-6蛋白表达水平与CGRP组比较亦显著增加(P<0.05),与心肌素干扰组水平类似。
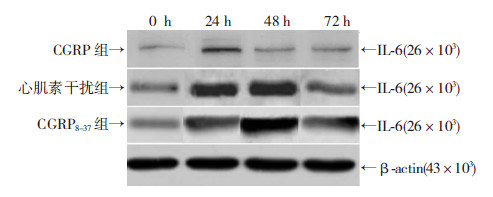 |
| 图 3 Western blot检测抑制心肌素表达或CGRP8-37处理对VSMCs中IL-6表达的影响 |
| (与内参灰度比值,x±s,n=3) | |||
| 时间点 | CGRP组 | 心肌素干扰组 | CGRP8-37组 |
| 0 h | 0.36±0.01 | 0.48±0.01 | 0.42±0.01 |
| 24 h | 0.51±0.01 | 1.74±0.04a | 1.56±0.03a |
| 48 h | 0.29±0.01 | 1.68±0.03a | 1.84±0.03a |
| 72 h | 0.31±0.01 | 0.98±0.02a | 1.15±0.02a |
| a: P<0.05,与同时间点的CGRP组比较 | |||
动脉粥样硬化是一种多因素共同作用的慢性炎症性血管疾病,其发展涉及包括VSMCs和浸润的免疫细胞等相互作用。在这一过程中,除了收缩静止的VSMCs进行表型转换而成为增殖迁移细胞并分泌细胞外基质外,VSMCs还涉及炎症激活过程,释放一系列炎症细胞因子和趋化因子,并吸收氧化脂质,与浸润炎症细胞相互作用,促进炎症和病变进展。本研究结果显示,在体外培养的VSMCs中,CGRP通过促进细胞心肌素蛋白表达,抑制IL-1β诱导的细胞炎症激活反应,这进一步阐明了CGRP对VSMCs生物学功能的调节作用。
早在2001年,Wang等[4]在小鼠胚胎心脏cDNA数据库中筛选新的心脏特异性基因时偶然发现一种心肌特异性蛋白,并命名为心肌素(myocardin)。研究显示,心肌素与血浆反应因子密切相关,在血管损伤疾病中心肌素表达减少[5, 6, 7],负性调节VSMCs增殖[8],而在心肌梗死后抑制成肌纤维细胞分化而减轻梗死组织纤维化[9];且抑制心肌素相关血浆反应因子将降低肺脏纤维化和促进间质细胞凋亡[10]。Lovren等[11]研究显示,在ApoE基因缺陷的小鼠中,腺病毒高表达miR-145能够促进VSMCs中心肌素的表达,从而维持细胞收缩表型并减轻动脉粥样硬化病变进展。新近研究显示,心肌素也是VSMCs炎症激活的负性调节剂[12];与野生型小鼠相比,心肌素杂合子小鼠来源的VSMCs中心肌素表达水平降低伴随着炎症激活显著增加[12];在体外培养的人冠状动脉VSMCs中,高表达心肌素显著抑制一系列炎症细胞因子、趋化因子和黏附分子的表达,且抗炎症介质表达亦增加,同时心肌素降低细胞氧化脂质吸收和白细胞趋化作用,抑制巨噬细胞在动脉粥样硬化病变的聚集[12]。本实验结果显示,在体外培养的VSMCs中,以高表达心肌素的腺病毒载体转染细胞后,再加入IL-1β激活细胞炎症反应,结果显示作为VSMCs炎症激活的代表性炎症因子IL-6表达水平较单纯IL-1β处理的细胞组显著降低,差异具有统计学意义,这表明心肌素具有抑制VSMCs炎症激活的作用。继之,应用CGRP处理IL-1β激活的VSMCs后,细胞中心肌素水平较对照组显著升高,且伴随着IL-6水平降低;而给予心肌素干扰后,则消除CGRP诱导的IL-6水平降低,这提示CGRP具有抑制IL-1β诱导培养的VSMCs炎症激活的作用,且这一作用可能是通过促进细胞中心肌素表达增加实现的。目前认识到,动脉粥样硬化发生与发展中VSMCs的炎症激活是关键事件之一,细胞激活后发生表型改变,促进细胞增殖和迁移,并可能表达巨噬细胞标记等,从而促进动脉粥样硬化进展。因此阐明CGRP抗VSMCs炎症激活作用以及在血管稳态和抗动脉粥样硬化中的作用具有重要现实意义,且心肌素可能作为CGRP抗动脉粥样硬化的作用靶点。
CGRP是一种广泛分布于神经和心血管系统的血管活性肽。生理条件下,CGRP需要与降钙素受体样受体/受体活性修饰蛋白1(receptor activity modifying protein 1,RAMP1)组成的复合受体结合才能发挥作用。研究显示,CGRP涉及三叉神经和偏头痛等疾病[13, 14],并在心血管系统自我稳态调节和血管结构中具有重要作用[15]。Kroeger等[16]研究显示,在肝脏中,CGRP通过减少促炎症介质(如可诱导的cAMP早期抑制因子)而发挥抗炎症作用。本研究结果显示,应用CGRP受体阻断剂CGRP8-37处理后阻断CGRP上调VSMCs心肌素表达作用和抗IL-1β诱导细胞炎症激活作用,提示CGRP是通过与其受体结合后发挥作用的。
总之,本研究发现,CGRP通过促进体外培养的VSMC的心肌素表达而抑制细胞炎症激活反应,这为以慢性炎症为主要发病机制的动脉粥样硬化性心血管疾病的防治提供了新的靶点和治疗策略。但研究也存在一定局限性,如未深入探讨CGRP与心肌素表达的相关信号通路和机制等,这需要进一步深入研究。
| [1] | Zheng X L. Myocardin and smooth muscle differentiation [J]. Arch Biochem Biophys, 2014, 543: 48-56. |
| [2] | Huang J, Wang T, Wright A C, et al. Myocardin is required for maintenance of vascular and visceral smooth muscle homeostasis during postnatal development[J]. Proc Natl Acad Sci U S A, 2015, 112(14): 4447-4452. |
| [3] | 陈攀科, 石蓓, 龙仙萍, 等. CGRP修饰大鼠MSCs对血管平滑肌细胞增殖及表型转化的影响[J]. 中国病理生理杂志, 2013, 29(10): 1777-1782. |
| [4] | Wang D, Chang P S, Wang Z, et al. Activation of cardiac gene expression by myocardin, a transcriptional cofactor for serum response factor[J]. Cell, 2001, 105(7): 851-862. |
| [5] | Minami T, Kuwahara K, Nakagawa Y, et al. Reciprocal expression of MRTF-A and myocardin is crucial for pathological vascular remodelling in mice[J]. EMBO J, 2012, 31(23): 4428-4440. |
| [6] | Starke R M, Ali M S, Jabbour P M, et al. Cigarette smoke modulates vascular smooth muscle phenotype: implications for carotid and cerebrovascular disease[J]. PLoS One, 2013, 8(8): e71954. |
| [7] | van-der-Veer E P, de-Bruin R G, Kraaijeveld A O, et al. Quaking, an RNA-binding protein, is a critical regulator of vascular smooth muscle cell phenotype[J]. Circ Res, 2013, 113(9): 1065-1075. |
| [8] | Talasila A, Yu H, Ackers-Johnson M, et al. Myocardin regulates vascular response to injury through miR-24/-29a and platelet-derived growth factor receptor-beta[J]. Arterioscler Thromb Vasc Biol, 2013, 33(10): 2355- 2365. |
| [9] | Lei H, Wu D, Wang J Y, et al. C1q/tumor necrosis factor-related protein-6 attenuates post-infarct cardiac fibrosis by targeting RhoA/MRTF-A pathway and inhibiting myofibroblast differentiation [J]. Basic Res Cardiol, 2015, 110(4): 35. |
| [10] | Sisson T H, Ajayi I O, Subbotina N, et al. Inhibition of myocardin-related transcription factor/serum response factor signaling decreases lung fibrosis and promotes mesenchymal cell apoptosis[J]. Am J Pathol, 2015, 185(4): 969-986. |
| [11] | Lovren F, Pan Y, Quan A, et al. MicroRNA-145 targeted therapy reduces atherosclerosis[J]. Circulation, 2012, 126(11 Suppl 1): S81-S90. |
| [12] | Ackers-Johnson M, Talasila A, Sage A P, et al. Myocardin regulates vascular smooth muscle cell inflammatory activation and disease [J]. Arterioscler Thromb Vasc Biol, 2015, 35(4): 817-828. |
| [13] | Diener H C. CGRP as a new target in prevention and treatment of migraine[J]. Lancet Neurol, 2014, 13(11): 1065- 1067. |
| [14] | Capuano A, Greco M C, Navarra P, et al. Correlation between algogenic effects of calcitonin-gene-related peptide (CGRP) and activation of trigeminal vascular system, in an in vivo experimental model of nitroglycerin-induced sensitization [J]. Eur J Pharmacol, 2014, 740: 97-102. |
| [15] | Mai T H, Wu J, Diedrich A, et al. Calcitonin gene-related peptide (CGRP) in autonomic cardiovascular regulation and vascular structure[J]. J Am Soc Hypertens, 2014, 8(5): 286-296. |
| [16] | Kroeger I, Erhardt A, Abt D, et al. The neuropeptide calcitonin gene-related peptide (CGRP) prevents inflammatory liver injury in mice[J]. J Hepatol, 2009, 51(2): 342-353. |



