2400038 重庆,第三军医大学:西南医院全军感染病研究所
2Institute of Infectious Diseases,Southwest Hospital,Third Military Medical University,Chongqing,400038,China
近年来,丙型肝炎病毒(hepatitis C virus,HCV)感染已成为不可忽视的公共卫生问题。聚乙二醇干扰素(pegylated interferon,PEG-IFN)联合利巴韦林(ribavirin,RBV)是目前抗HCV的标准疗法[1, 2]。HCV基因型是影响HCV患者抗病毒治疗应答的最重要因素[3]。目前HCV 1型和2/3型感染者临床上均有标准的治疗方案,但HCV 6型感染者的治疗方式及疗程还需进一步摸索和优化,有研究提示HCV 6型感染者治疗方式可以参照HCV 2/3型的标准联合抗病毒方案[4]。本研究系统收集了第三军医大学西南医院全军感染病研究所2010年5月至2014年10月应用PEG-IFN联合RBV治疗的所有门诊和住院的HCV 6型和2/3型感染者的临床资料进行回顾性分析,从治疗过程中各个时间点的应答情况以及早期治疗应答对最终取得持续病毒学应答 (sustained virological response,SVR)的预测情况两方面来比较HCV 6型感染者与HCV 2/3型感染者治疗效果,探索HCV 6型感染者的临床治疗方法。
1 对象与方法 1.1 研究对象系统收集重庆西南医院感染病专科医院2010年5月至2014年10月所有门诊和住院期间应用PEG-IFN联合RBV治疗的慢性丙型肝炎6型感染者和2/3型感染者的临床资料(年龄、性别、HCV RNA水平、ALT水平、腹部彩超结果、感染途径、治疗过程),并按照以下治疗方式严格进行筛选入组:利巴韦林每日用量针对体质量<65 kg、65~85 kg、>85 kg的患者分别 为800、1 000 mg、1 200 mg;派罗欣皮下注射180 μg/周; 佩乐能每周皮下注射1.5 μg/kg;所有患者完成24周规定疗程并且有6个月以上随访的完整资料;排除HBV、HIV、糖尿病、高血压、自身免疫性肝病等疾病;满足上述条件者作为本研究的入组对象。本研究已经通过西南医院伦理委员会批准。
1.2 疗效评价根据丙型肝炎治疗原则:快速病毒学应答(rapid virological response,RVR)是指治疗4周时,HCV RNA水平低于最低检测限;早期病毒学应答(early virological response,EVR)是指治疗12周时,HCV RNA水平低于最低检测限;持续病毒学应答(sustained virological response,SVR)是指疗程结束后,随访24周以上,HCV RNA水平低于最低检测限;结束疗程后未获得ETVR者计为未获得SVR。
1.3 统计学方法应用SPSS 18.0进行统计学分析,计量资料以x ±s 表示。对基线计量资料比较采用t检验,率的比较采用χ2检验。对疗效评价采用非劣效检验,即当试验组非劣于对照组时,认为试验成功。经临床专家商讨,非劣效性界值△=15%,P<0.05作为统计学检验水准。
2 结果 2.1 HCV 6型、2/3型感染者入组病例筛选标准和流程
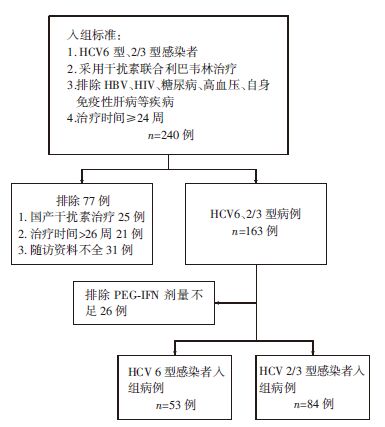
符合条件的入组病例共137例,我们分析其实验室检查结果,利用HCV基因型不同将病例分为2组,分别为HCV 6型感染者组,共53例;HCV 2/3型感染者组,共84例。见图 1。
|
| 图 1 HCV 6型、2/3型感染者入组病例筛选流程 |
选取了符合24周规定标准疗法且有6个月及以上随访资料的HCV感染者共137例入组。HCV 6型感染者53例,HCV 2/3型感染者共84例。如表 1所示,HCV 6型和2/3型感染者年龄及性别分布、治疗前血清HCV RNA与ALT水平以及应用PEG-IFN种类均无统计学差异。但吸毒史在HCV 6型感染者中的比例高于HCV 2/3型感染者所占的比例。
| 基本资料 | HCV 6型 | HCV 2/3型 | P |
| 病例数量 | 53 | 84 | |
| 年龄(±s) | 36.3±11.6 | 35.3±9.9 | |
| 年龄≥40岁[n(%)] | 17(32.1) | 16(19.0) | 0.102 |
| 性别[男,n(%)] | 26(49.1) | 44(52.4) | 0.729 |
| 吸毒史[n(%)] | 29(54.7) | 21(25.0) | 0.001 |
| 治疗前ALT≥100 IU/L[n(%)] | 22(41.5) | 41(48.8) | 0.482 |
| 治疗前HCV RNA≥2×106 copy/mL[n(%)] | 39(73.6) | 55(65.5) | 0.350 |
| PEG-IFN α-2a 治疗[n(%)] | 30(56.6) | 50(59.5) | 0.859 |
| PEG-IFN α-2b 治疗[n(%)] | 23(43.4) | 34(40.5) | 0.859 |
本研究入组的137例HCV感染者,均在治疗开始后24周及48周有完整的HCV RNA检测结果。其中HCV 6型感染者有46例(86.8%)获得了SVR,HCV 2/3型感染者有76例(90.5%)获得了SVR,两组率差95%可信区间为:(-0.147 6,0.073 6),其下限0.14小于非劣效性界值0.15,非劣效性检验成立,可以认为HCV 6型感染者获得SVR的率非劣于HCV 2/3型感染者。HCV 6型感染者获得RVR为88.7%,HCV 2/3型感染者获得的RVR为89.3%,2组率差95%可信区间为:(-0.113 9,0.101 9),可认为HCV 6型感染者获得RVR的率非劣于HCV 2/3型感染者;HCV 6型感染者与HCV 2/3型感染者获得EVR分别是 94.3%、96.4%,2组率差95%可信区间为:(-0.095 0,0.053 0),因此HCV 6型感染者获得EVR的率非劣于HCV 2/3型感染者。
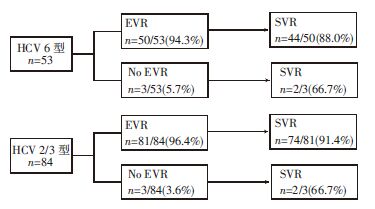
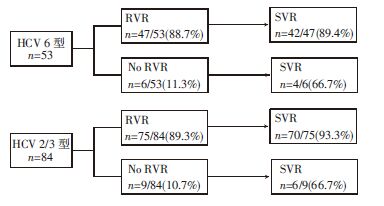
2.4 HCV 6型和HCV 2/3型感染者RVR、EVR对最终SVR的预测在137例入组患者中,我们均取得了其治疗第4、12周时的HCV RNA结果。针对这137例患者RVR,EVR对最终获得SVR的预测作用进行分析。HCV 6型感染者RVR对最终获得SVR的阳性预测值(获得RVR后,继续规范治疗足量疗程,最终达到SVR的百分率)为89.4%,而HCV 2/3型感染者RVR对最终获得SVR的阳性预测值为93.3%,率差95%可信区间为:(-0.143 6,0.065 6),可以认为HCV 6型感染者RVR对SVR的阳性预测值非劣于HCV 2/3型感染者。6例未能达到RVR的HCV 6型感染者,最终获得SVR的有4例,即RVR对SVR的阴性预测值(未能达到RVR,但治疗结束后最终获得SVR)为66.7%,2/3型感染者的RVR对SVR的阴性预测值也是66.7%(图 2)。HCV 6型与2/3型感染者EVR对最终SVR的阳性预测分别为88.0%、91.4%,率差95%可信区间为:(-0.142 8,0.074 8),可以认为HCV 6型感染者EVR对SVR的阳性预测值非劣于HCV 2/3型感染者;未能达到EVR的两组感染者,EVR对SVR的阴性预测值均为66.7%(图 3)。
|
| 图 2 RVR对SVR的预测值 |
|
| 图 3 EVR对SVR的预测值 |
聚乙二醇干扰素联合利巴韦林治疗是目前HCV感染者的最佳治疗方案,它的治疗应答主要取决于HCV感染的基因型。HCV分为6个基因型,其中1、2型和3型呈全世界分布,而4、5型主要分布在非洲,6型主要流行于亚洲。由于世界经济及医疗卫生的格局,HCV 4、5、6型的研究甚少,主要的研究集中在HCV 1、2/3型。在已有的报道中,HCV基因1型的SVR率可达到40%~50%,HCV 2/3型能达到70%~80%[5]。近年来,HCV 6型感染者主要出现在我国西南地区[6, 7],因此,有关HCV 6型感染者的疗效预测和疗程优化需要的进一步研究并确定。近
年来,有研究分别比较了HCV 1、2/3、6型的抗病毒治疗效果,认为HCV 6型感染者的治疗应答率高于HCV 1型[8],和2/3型感染者的治疗应答率无差异[9],也有研究对HCV 6型抗病毒治疗24周和48周的疗效做了比较,认为二者的疗效没有统计学差异[4]。鉴于目前已有的报道认为HCV 6型感染者应用聚乙二醇干扰素联合利巴韦林治疗24周可以取得和HCV 2/3型相近的疗效。我们收集了西南医院全军感染病研究所2010年5月至2014年10月所有门诊和住院期间应用PEG-IFN联合RBV治疗的HCV 6型感染者和2/3型感染者的临床资料进行回顾性分析,经过严格的入组筛选,最终确定入组HCV 6型感染者53例,HCV 2/3型感染者84例。通过治疗学应答来比较2组的疗效,用以指导临床。
本研究的结果显示HCV 6型感染者与HCV 2/3型 感染者获得SVR的比例分别为86.8%、90.5%,率差95%可信区间为:(-0.147 6,0.073 6);HCV 6型感染者获得RVR的比例是88.7%、HCV 2/3型感染者获得RVR的比例是89.3%,率差95%可信区间为:(-0.113 9,0.101 9);另外,HCV 6型感染者与HCV 2/3型感染者获得EVR的比例分别是94.3%、96.4%,率差95%可信区间为:(-0.095 0,0.053 0);根据非劣效性检验结果,可认为采用24周聚乙二醇干扰素联合利巴韦林治疗HCV 6型感染者获取SVR、RVR以及EVR的率非劣于HCV 2/3型感染者。同样,根据非劣效性检验结果,HCV 6型感染者RVR、EVR对SVR的阳性预测值非劣于HCV 2/3型感染者。这些结果进一步证实了HCV 6型感染者与HCV 2/3型感染者一样,对PEG-IFN联合RBV的联合疗法比较敏感,所以我们可以认为,对绝大多数HCV 6型感染者的临床抗病毒治疗方案中,我们可以采取和HCV 2/3型一样的方案,应用24周的联合抗病毒治疗即可。通过上面的结果得知,HCV 6型和2/3型患者在病毒学应答过程中,获得RVR的比例更接近于获得SVR的比例,另外RVR对SVR的阳性预测值也要高于EVR对SVR的阳性预测值。这说明RVR是HCV抗病毒治疗最终实现SVR的一个重要因素,它对SVR的预测价值要高于EVR,临床上采取治疗时应该把RVR纳入一个长期的疗效评估指标。为了排除其它基线指标可能对病毒学应答的影响,影响我们结果的准确性。本研究比较了HCV 6型感染者与HCV 2/3型感染者的基本资料特征,均无统计学差异。吸毒史在HCV 6型感染者中所占比例54.7%高于HCV 2/3型感染者所占的比例25.0%(P=0.001),这与已报道的静脉药瘾是HCV 6型感染者一个重要特点相吻合[10]。但吸毒史究竟对HCV的抗病毒治疗各个阶段以及最终实现SVR有无影响,以及吸毒的时间点对病毒学应答的影响,需要进一步扩大样本量进行探讨。由于本研究是临床回顾性研究,可能存在选择偏倚,在今后的研究中,可采用多中心研究,利用多家医院临床数据资料进行分析,以减少偏倚。
综上所述,采用聚乙二醇干扰素联合利巴韦林治疗HCV 6型感染者的疗效非劣于2/3型感染者,故我们可以把24周的标准PEG-IFN联合RBV疗法作为临床上HCV 6型的标准治疗方案。
| [1] | European Association for the Study of Liver. EASL Clinical Practice Guidelines: management of hepatitis C virus infection[J]. J Hepatol, 2014, 60(2): 392-420. |
| [2] | Marino Z, van-Bommel F, Forns X, et al. New concepts of sofosbuvir-based treatment regimens in patients with hepatitis C[J]. Gut, 2014, 63(2): 207-215. |
| [3] | Ghany M G, Strader D B, Thomas D L, et al. Diagnosis, management, and treatment of hepatitis C: an update[J]. Hepatology, 2009, 49(4): 1335-1374. |
| [4] | Thu-Thuy P T, Bunchorntavakul C, Tan-Dat H, et al. A randomized trial of 48 versus 24 weeks of combination pegylated interferon and ribavirin therapy in genotype 6 chronic hepatitis C[J]. J Hepatol, 2012, 56(5): 1012-1018. |
| [5] | Afdhal N H, Mc-Hutchison J G, Zeuzem S, et al. Hepatitis C pharmacogenetics: state of the art in 2010[J]. Hepatology, 2011, 53(1): 336-345. |
| [6] | Zhou Y, Wang X, Mao Q, et al. Changes in modes of hepatitis C infection acquisition and genotypes in southwest China[J]. J Clin Virol, 2009, 46(3): 230-233. |
| [7] | Yan Z, Fan K, Wang Y, et al. Changing pattern of clinical epidemiology on hepatitis C virus infection in southwest China[J]. Hepat Mon, 2012, 12(3): 196-204. |
| [8] | Hui C K, Yuen M F, Sablon E, et al. Interferon and ribavirin therapy for chronic hepatitis C virus genotype 6: a comparison with genotype 1[J]. J Infect Dis, 2003, 18(7): 1071-1074. |
| [9] | Zhou Y Q, Wang X H, Hong G H, et al. Twenty-four weeks of pegylated interferon plus ribavirin effectively treat patients with HCV genotype 6a[J]. J Viral Hepat, 2011, 18(8): 595-600. |
| [10] | Pybus O G, Barnes E, Taggart R, et al. Genetic history of hepatitis C virus in East Asia[J].J Virol, 2009, 83(2): 1071-1082. |



