胸主动脉夹层由于累及部位不同,治疗策略也不尽相同。主动脉夹层的经典分型方法主要有Stanford分型和DeBakey分型两种,早期腔内治疗的病例选择主要局限于Stanford B型或DeBakey Ⅲ型夹层,两者的共同特点是夹层只累及降主动脉,支架植入不影响头臂动脉的血供。随着腔内治疗技术的进步以及杂交技术的应用,腔内治疗的适应证大大扩展[1]。为了更好地适应治疗方式的选择,Ishimaru在2002年按照胸主动脉各部位与头臂动脉分支的关系将其分为0~4 5个区域[2],但遗憾的是这一分区方法并未包括升主动脉的主要部分。为了细化治疗策略,我们将升主动脉的中段(冠状动脉开口远端2 cm至无名动脉开口近端2 cm的区域)划分为-1区。新的胸主动脉细化分区更加有利于对胸主动脉夹层腔内治疗方式的个体化选择,使腔内治疗的适应证大大拓宽,从而减少开放手术所带来的重大创伤,加速患者的康复,减少并发症和病死率。
1 资料与方法 1.1 临床资料2009年1月至2015年1月,共对我科收治的208例患者进行了腔内治疗,其中166例进行了单纯的支架植入术,另外42例采用了杂交手术,在建立血管旁路后完成了腔内支架植入。其中夹层破口位于-1区4例、0区6例、1区6例、2区20例、3区和4区172例。年龄35~76(57.1±18.3)岁,男性119例,女性89 例,有突发性胸背痛症状的176例,腹痛症状为主的19例,症状不典型者14例。其中178例伴有不 同程度高血压,接受正规降压治疗的117例,占56.3%。以上患者在术前常规心脏超声检查中均未见明显的主动脉瓣关闭不全。
1.2 胸主动脉分区按照胸主动脉各部位与头臂动脉分支的关系,在Ishimaru主动脉分区基础上增加-1区,将胸主动脉分为-1区、0区、1区、2区、3区和4区。如图 1所示。
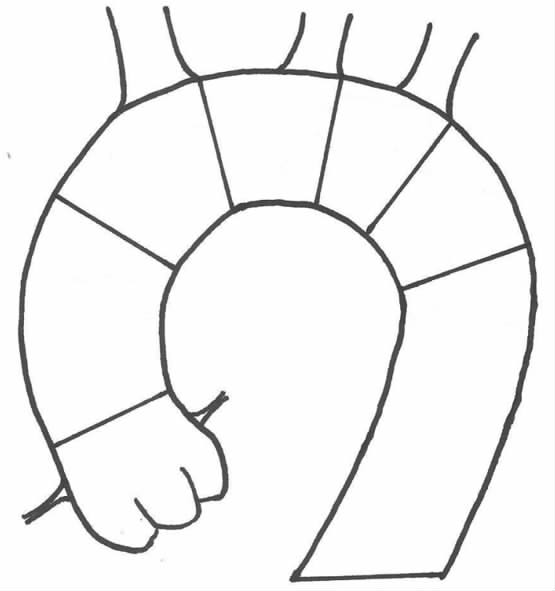 |
| 图 1 主动脉分区示意图 |
根据夹层破口所在的不同区域,采用腔内隔绝或腔内技术加血管旁路的杂交手术进行综合治疗。所有患者术前检查及术后复查均采用东芝320动态容积CT扫描,术中使用设备为西门子Artis Zee Biplane血管造影机。
1.3.1 夹层破口位于4区均采用单一的腔内支架隔绝术(图 2),共113例。
 |
| 图 2 夹层破口位于4区患者的术前(A)与腔内隔绝术后(B)造影观察 |
采用部分或完全隔绝左锁骨下动脉开口的方式进行腔内治疗(图 3)共56例;对部分左椎动脉优势的患者,先建立左锁骨下动脉至左颈总动脉人工血管旁路,再行支架隔绝左锁骨下动脉开口及夹层破口(图 4),共2例。
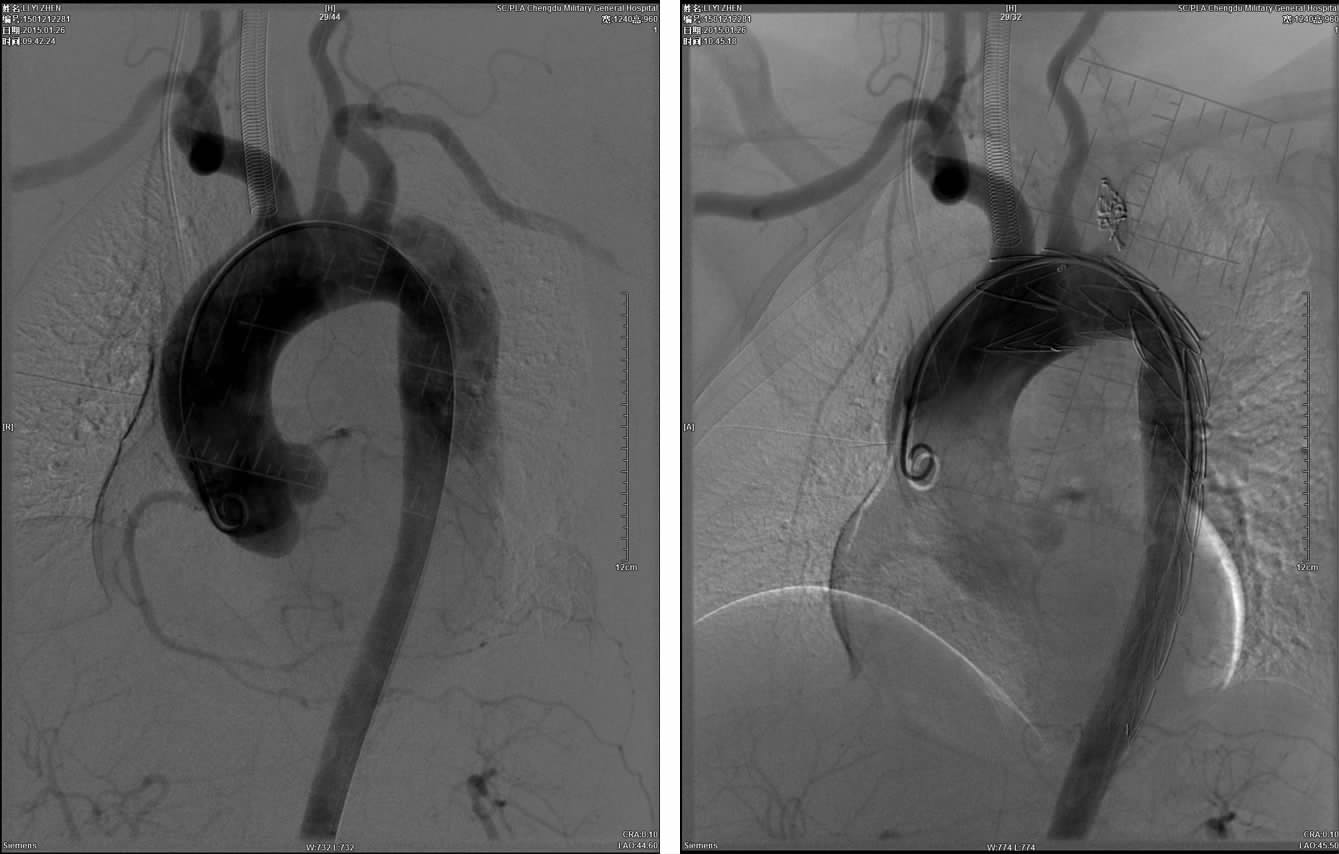 |
| 图 3 夹层破口位于3区患者的术前(A)与腔内隔绝术并封闭锁骨下动脉开口后(B)造影对照观察(方式1) |
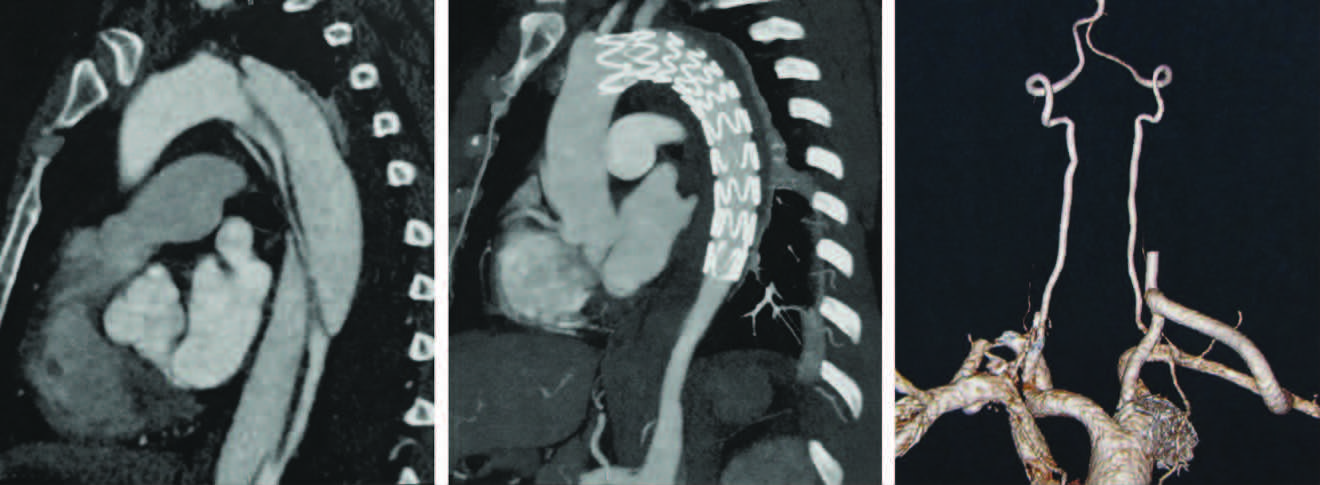 |
| 图 4 夹层破口位于3区患者的术前(A)、腔内隔绝后(B)与左颈总动脉-左锁骨下动脉旁路CT表现(C)(方式2) |
如果破口位于左锁骨下动脉开口后端,可采用单纯腔内隔绝的方式,将支架的带膜区紧贴着左颈总动脉释放(图 3),共3例;对部分左椎动脉优势的患者,可采用图 4的方式,共1例。如果破口位于左锁骨下动脉开口前端,则先建立左右颈总动脉的旁路,再进行支架腔内隔绝,覆盖左锁骨下动脉及左颈总动脉(图 5),共16例。
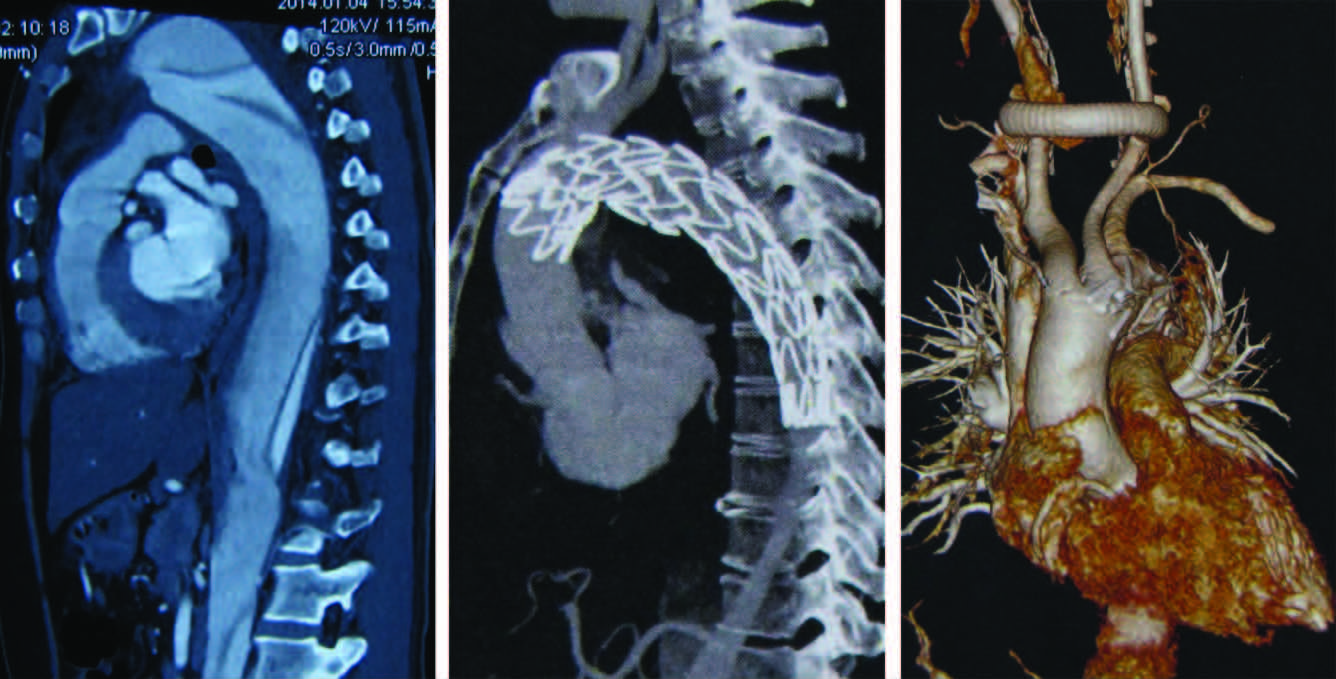 |
| 图 5 夹层破口位于2区患者的术前(A)、腔内隔绝后(B)与左右颈总动脉间旁路CT表现(C) |
在侧壁钳钳夹部分主动脉壁的情况下完成人工血管跟主动脉之间的端侧吻合,再将人工血管的另一端与颈总动脉进行端端吻合,在非体外循环情况下建立升主动脉至左右颈总动脉的旁路,再行支架腔内隔绝,覆盖主动脉所有分支(图 6),共3例,部分破口靠后的患者也可采用图 5的方式,共3例。
 |
| 图 6 夹层破口位于1区患者的术前(A)与腔内隔绝术及升主动脉至左右颈总动脉旁路术后(B)造影观察 |
在体外循环辅助下采用三分叉人工血管分别将升主动脉与3个主要分支吻合,重建主动脉弓,再用支架腔内隔绝,覆盖主动脉所有分支(图 7),共2例;部分患者也可采用图 6的方式,共4例。
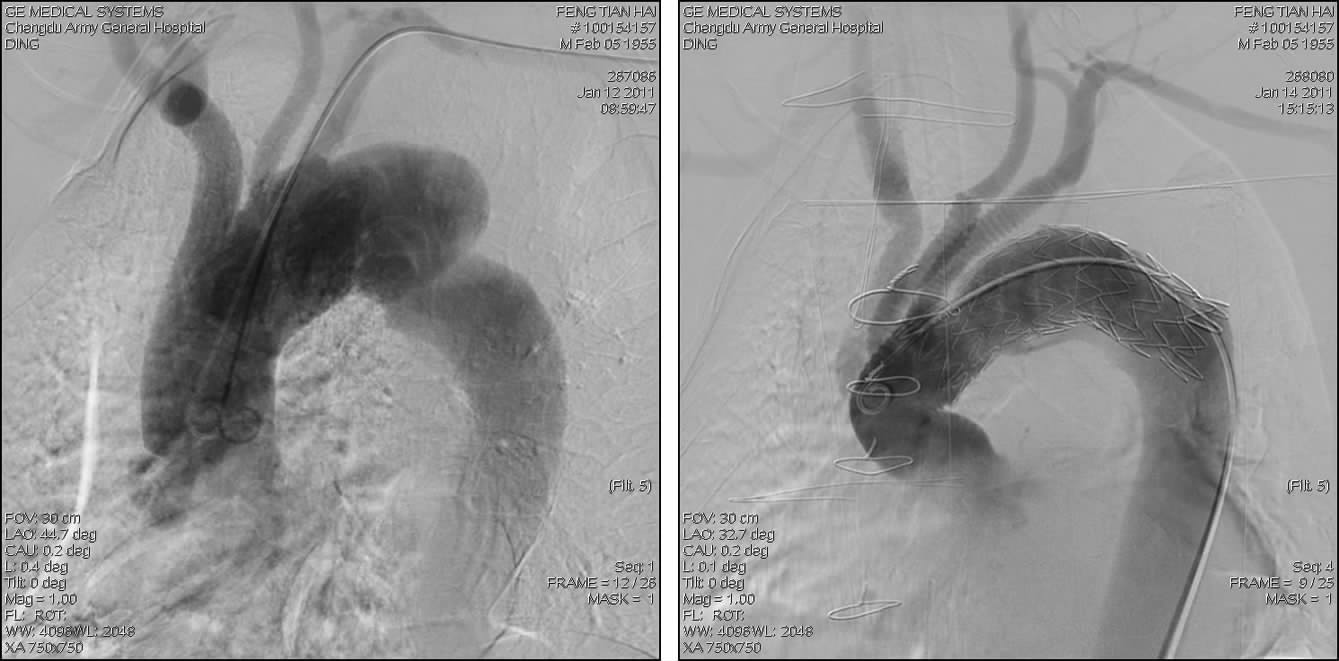 |
| 图 7 夹层破口位于0区患者的术前(A)与腔内隔绝及升主动脉置换术后(B)造影观察 |
大部分可采用与0区相同的办法(图 7),共3例;如果破口距冠状动脉及无名动脉开口有一定距离,且夹层累及的范围比较局限,夹层影响的范围距离冠状动脉及无名动脉开口均有 1 cm 以上的距离,可以考虑单纯支架腔内隔绝(图 8),共1例。
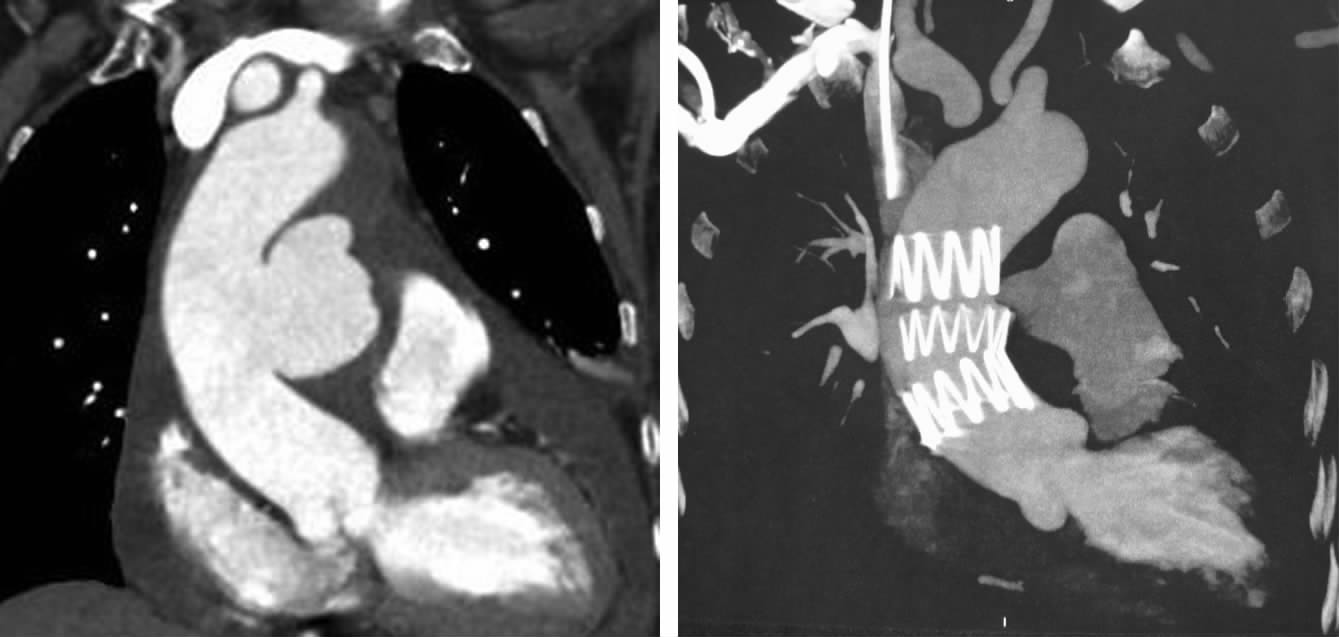 |
| 图 8 夹层破口位于-1区患者的术前(A)与腔内隔绝术后(B)造影观察 |
以上患者如果夹层累及升主动脉,或者夹层虽未累及升主动脉,但是经控制血压等处理后胸痛症状仍然明显,则在完成必要的术前准备后急诊或第2天完成手术,其余患者均在完善术前检查后3 d内完成手术。对于个别合并主动脉瓣关闭不全的患者,如果夹层累及升主动脉及主动脉弓则直接行开放手术,如果夹层仅累及主动脉弓以远部位,则先行夹层的腔内治疗,后期再考虑主动脉瓣置换。
2 结果所有208例患者均顺利完成主动脉腔内支架植入术,其中42例患者建立了头臂血管旁路。手术方式见表 1。166例单纯腔内隔绝的患者手术时间1~2.6 h,平均1.6 h,术中失血5~30 mL,平均16.5 mL,住院时间8~15 d,平均11.5 d,无围术期死亡。42例杂交手术患者手术时间1.9~4.5 h,平均2.8 h,术中失血50~450 mL,平均150 mL,住院时间13~18 d,平均16.2 d,无围术期死亡,其中1例出现Ⅰ型内漏,因渗漏量极少,当时未予处理,半年复查时内漏消失。另1例出现Ⅱ型内漏,造影剂从支架远端流入,流量较少,流速较慢,患者家属拒绝再加放1枚支架,观察随访。1例患者术后1个月时支架远端主动脉内膜再次发生破裂,重新植入1枚支架后痊愈。所有患者于出院前,术后半年及术后1年常规复查、随访,20例患者术后1年失访,失访的患者主要分布在较边远的地区,未能按时来复查,且电话号码因故变更,无法取得联系。其余患者术后半年至1年复查时情况良好,支架及旁路内血流通畅,1例Ⅰ型内漏者术后半年复查内漏消失,另1例Ⅱ型内漏者内漏仍存在,但假腔未见扩大,患者也无明显症状,因患者要求未作特殊处理,该患者已随访4年,假腔未见明显变化。所有患者所使用的支架长度145~200 mm,直径28~40 mm,平均34.5 mm。支架直径的选择在锚定区主动脉直径的基础上加大10%~15%。
| (例) | ||||||
| 治疗方式 | 夹层破口所在区域 | |||||
| -1区 | 0区 | 1区 | 2区 | 3区 | 4区 | |
| TEVAR(图 2、图 3、图 8) | 1 | 0 | 0 | 3 | 56 | 113 |
| LSA-LCCA bypass+TEVAR(图 4) | 0 | 0 | 0 | 1 | 2 | 0 |
| RCCA-LCCA bypass+TEVAR (图 5) | 0 | 0 | 3 | 16 | 0 | 0 |
| AA-RCCA-LCCA bypass+TEVAR(图 6) | 0 | 4 | 3 | 0 | 0 | 0 |
| AAR+bypass+ TEVAR(图 7) | 3 | 2 | 0 | 0 | 0 | 0 |
| 总计 | 4 | 6 | 6 | 20 | 59 | 113 |
| TEVAR (thoracic endovascular repair):腔内修复;Bypass:血管旁路;LSA(left subclavian artery):左锁骨下动脉;LCCA(left common carotid artery):左颈总动脉;RCCA(right common carotid artery):右颈总动脉;AA (ascending aorta): 升主动脉;AAR(ascending aorta replacement):升主动脉置换 | ||||||
常规的主动脉分型方法,不管是Stanford 还是DeBakey分型方法,对主动脉夹层治疗方式的选择具有重要意义,以往认为只要夹层破口不涉及升主动脉或主动脉弓——即Stanford B型或DeBakey Ⅲ型,均可进行单纯的腔内支架隔绝治疗,腔内修复技术已经逐步成为Stanford B型主动脉夹层安全有效的治疗方式[3, 4];而涉及升主动脉或主动脉弓的夹层则多需要在体外循环下进行开放手术,手术时间长、创伤大、并发症多、死亡率相对较高。尽管近年来外科技术在不断进步,但是对累及弓部的主动脉夹层进行开放的主动脉弓重建手术仍有较高的死亡率[5]。随着腔内治疗技术的进步、杂交技术的兴起以及杂交手术室的推广,涉及升主动脉或主动脉弓的夹层也可以进行腔内治疗。为了便于手术方式的选择,Ishimaru在2002年按照胸主动脉各部位与头臂动脉分支的关系将其分为Z0、Z1、Z2、Z3、Z4 5个区域[2],遗憾的是不知什么原因,Ishimaru只将升主动脉远端划为0区,并未将升主动脉中段进行分区。我们认为升主动脉夹层只要破口离冠状动脉和无名动脉有一定距离,同样可以通过腔内的方式或结合杂交技术进行治疗,因此我们将升主动脉中段划分为“-1区”。杂交技术包含了外科血管旁路和支架腔内修复[6],杂交技术和开放手术相比有不少优势[7, 8, 9],首先,大部分杂交技术避免了体外循环,尤其对年老体弱不能承受开放手术者适用,尽管夹层破口位于0区的患者在进行升主动脉置换并与3根头臂血管建立旁路的时候也需要体外循环辅助,但是避免了常规全弓置换术时深低温停循环对机体造成的巨大打击,降低了术后并发症的发生率;其次,杂交技术增加了近端锚定,扩大主动脉弓腔内修复的适应证;第三,杂交技术相比于开放手术创伤更小。因此,杂交手术不仅简化了手术方式、缩短了手术时间,同时大大减少了手术创伤,降低了并发症和死亡率[10]。虽然,涉及主动脉分支的夹层也有人通过烟囱技术或开窗技术来解决,但是这两项技术目前尚处于探索之中,近远期效果都有待于进一步验证,而杂交技术效果确切,适应证更广。在我们完成的208例患者中,166例进行了单纯的腔内隔绝,42例采用了杂交技术,均取得了满意的效果。42例杂交手术患者中2例出现早期内漏,术后半年复查时其中1例Ⅰ型内漏者内漏消失,另1例Ⅱ型内漏者内漏仍存在,但假腔未见扩大,患者也无明显症状,因患者及家属的要求未作特殊处理,该患者已随访4年,假腔未见明显变化。在以往,升主动脉病变单纯采用腔内技术隔绝的病例较为少见。我们有1例升主动脉夹层的患者,虽然破口有3 cm,但距离冠状动脉和无名动脉开口各有2 cm的距离,且病变较为局限,破口近远端的主动脉直径均为35 mm,且主动脉瓣没有反流。我们选用了一款COOK公司直径40 mm,长度81 mm的带膜支架进行腔内修复,同样取得了满意的效果。该患者至今已随访1年,一般情况良好,CT造影检查提示支架近远端均未见造影剂外溢。类似病例国外也有个案报道[11]。
由此可见,只要我们仔细评估、综合判断,胸主动脉各区域的夹层,都有结合腔内方式进行治疗的机会,而胸主动脉分区对主动脉夹层腔内修复个体化治疗方案的选择具有重要的意义。
| [1] | Kent W D, Appoo J J, Bavaria J E, et al. Results of type II hybrid arch repair with zone 0 stent graft deployment for complex aortic arch pathology[J]. J Thorac Cardiovasc Surg, 2014, 148(6): 2951-2955. |
| [2] | Mitchell R S, Ishimaru S, Ehrlich M P, et al. First International Summit on Thoracic Aortic Endografting: roundtable on thoracic aortic dissection as an indication for endografting[J]. J Endovasc Ther, 2002, 9(suppl 2): Ⅱ98-Ⅱ105. |
| [3] | Wilkinson D A, Patel H J, Williams D M, et al. Early open and endovascular thoracic aortic repair for complicated type B aortic dissection[J]. Ann Thorac Surg, 2013, 96(1): 23-30. |
| [4] | Weidenhagen R, Bombien R, Meimarakis G, et al. Management of thoracic aortic lesions—the future is endovascular[J]. Vasa, 2012, 41(3): 163-176. |
| [5] | Patel H J, Nguyen C, Diener A C, et al. Open arch reconstruction in the endovascular era: analysis of 721 patients over 17 years[J]. J Thorac Cardiovasc Surg, 2011, 141(6): 1417-1423. |
| [6] | Kuratani T, Sawa Y. Current strategy of endovascular aortic repair for thoracic aortic aneurysms[J]. Gen Thorac Cardiovasc Surg, 2010, 58(8): 393-398. |
| [7] | Antoniou G A, Mireskandari M, Bicknell C D, et al. Hybrid repair of the aortic arch in patients with extensive aortic disease[J]. Eur J Vasc Endovasc Surg, 2010, 40(6): 715-721. |
| [8] | Eagleton M J, Greenberg R K. Hybrid procedures for the treatment of aortic arch aneurysms[J]. J Cardiovasc Surg(Torino), 2010, 51(6): 807-819. |
| [9] | Lotfi S, Clough R E, Ali T, et al. Hybrid repair of complex thoracic aortic arch pathology: long-term outcomes of extra-anatomic bypass grafting of the supra-aortic trunk[J]. Cardiovasc Interv Radiol, 2013, 36(1): 46-55. |
| [10] | Goksel O S, Guven K, Karatepe C, et al. Debranching solutions in endografting for complex thoracic aortic dissections[J]. Arq Bras Cardiol, 2014, 103(2): 154-160. |
| [11] | Metcalfe M J, Karthikesalingam A, Black S A, et al. The first endovascular repair of an acute type A dissection using an endograft designed for the ascending aorta[J]. J Vasc Surg, 2012, 55(1): 220-222. |



