腹腔镜手术(laparoscopic surgery,LS)是目前普遍开展的一种微创手术,为了充分暴露组织结构及开放手术视野,术中通常需要建立CO2气腹(pneumoperitoneum,Pp)[1]。然而,气腹可造成组织缺血再灌注损伤(ischemia/reperfusion injury,I/RI)[2, 3],其中氧化应激反应及细胞凋亡是肾I/RI的重要机制[4]。为减轻CO2 气腹的损伤,近年来有学者提出了CO2气腹缺血预处理(ischemic preconditioning,IP)的方法,即利用气腹前短暂快速充气、放气过程产生预先缺血的效果以提高机体抗损伤的能力[5, 6, 7],其中,文献采用的缺血预处理方案的次数仍各有异。本研究旨在比较气腹前给予不同缺血预处理次数对气腹所致肾脏氧化应激损伤及细胞凋亡的影响,以进一步探讨缺血预处理的最佳治疗方案,为临床减轻腹腔镜手术肾脏损伤提供实验指导。
1 材料与方法 1.1 材料丙二醛、超氧化物歧化酶、总抗氧化物能力、考马斯亮蓝蛋白定量检测试剂盒(南京建成生物工程研究所,中国),小鼠抗大鼠Bcl-2、Bax单克隆抗体(Santa Cruz,美国),小鼠抗大鼠β-actin抗体 、HRP偶联山羊抗小鼠IgG、超敏二步法抗小鼠免疫组化检测试剂盒(中杉金桥生物技术,中国),超敏型ECL检测试剂盒、BCA蛋白含量检测试剂盒、全蛋白抽提试剂盒(南京凯基生物科技发展有限公司,中国),凝胶配置试剂盒(碧云天生物技术研究所,中国),化学分光光度计(Shimadzu公司,日本),Olympus显微镜 (Olympus公司,日本),凝胶图像分析系统 (Kodak公司,美国)。
1.2 方法 1.2.1 动物模型制备及肾脏标本收集清洁级健康雄性SD大鼠30只,6~7周龄,体质量(200±10)g,由重庆医科大学实验动物中心提供,分为5组(n=6):假手术(Sham)组,气腹(Pp)组,缺血预处理1次(IP1)组,缺血预处理3次(IP3)组,缺血预处理5次(IP5)组。所有大鼠术前禁食12 h,自由饮水。10%水合氯醛3 mL/kg腹腔注射麻醉后,平卧位固定,腹部备皮。Pp组在脐部下方腹壁作1 cm长切口至腹膜,用气腹针插入腹腔内深度约1 cm,并作荷包缝合固定气腹针闭合腹腔,连至气腹机,以10 mmHg压力建立CO2气腹,持续时间60 min。IP1、IP3及IP5组在建立CO2气腹前行不同缺血预处理,即以10 mmHg压力充气5 min放气5 min,分别连续1、3、5次,余步骤同Pp组。Sham组接受假手术,即只插入气腹针,不建立CO2气腹,持续时间60 min。各组大鼠气腹结束后恢复灌注,关腹,于(24±2)℃环境下保暖60 min后,0.85%生理盐水心脏灌注至肾脏苍白后立即分离出双侧肾脏,肾脏纵切为两部分,其中一部分置于4%多聚甲醛溶液中固定,及时制成石蜡切片,以备HE染色及免疫组织化学染色;另一部分于-80 ℃低温冰箱保存,用于氧化应激及Western blot检测。
1.2.2 肾脏组织病理学观察大鼠肾脏标本经4%多聚甲醛溶液固定24 h后,常规乙醇梯度脱水、二甲苯透明及石蜡包埋,4 μm连续切片后行HE染色,光学显微镜下观察肾脏组织病理学变化。
1.2.3 肾脏氧化应激指标检测取-80 ℃冻存的肾脏组织150 mg,冰水浴条件下以0.9%生理盐水为稀释液制备成10%肾脏组织匀浆,4 ℃低温离心机3 000 r/min 离心15 min,取上清液后考马斯亮蓝法(Bradford法)行蛋白定量,采用化学分光光度法按试剂盒说明书检测各项氧化应激生化指标:超氧化物歧 化酶(SOD),丙二醛(MDA)及总抗氧化能力(T-AOC)。
1.2.4 免疫组化分析肾脏中凋亡相关蛋白表达石蜡切片常规脱蜡至水,0.01 mol/L PBS(pH 7.4)冲洗;0.01 mol/L枸橼酸缓冲液(pH 6.0)浸泡,微波修复使抗原充分暴露;室温冷却后3%H2O2去离子水室温孵育20 min以阻断内源性过氧化氢酶,PBS冲洗;滴加一抗(Bcl-2、Bax均按 1 ∶500稀释)于组织上,4 ℃孵育过夜,次日室温下复温30 min,PBS冲洗;滴加试剂1(Polymer helper)37 ℃孵育20 min,PBS冲洗;滴加试剂2(poly-HRP anti-mouse IgG)37 ℃孵育20 min,PBS冲洗;DAB显色,光镜下观察阳性染色反应,苏木精复染、梯度酒精脱水、透明、中性树胶封片。 同时采用PBS代替一抗作阴性对照,余步骤相同。应用Image-Pro Plus软件进行免疫组化图像分析,分别测定Bcl-2、Bax的累积光密度(integrated optical density,IOD)。
1.2.5 Western blot定量检测肾脏中凋亡相关蛋白表 达取-80 ℃冻存的肾脏组织100 mg置于预冷的玻璃匀浆器中,加入1 mL冷Lysis Buffer(含5 μL磷酸酶抑制剂、1 μL蛋白酶抑制剂和5 μL 100 mmol/L PMSF), 冰水浴匀浆,4 ℃低温离心机14 000 r/min离心15 min,取上清液即为全蛋白提取物,BCA法行蛋白定量检测。每个样本取含70 μg总蛋白变性后进行蛋白电泳(浓缩胶5%、分离胶12% SDS-PAGE),蛋白分离后湿转至PVDF膜(Millipore,美国),5%脱脂奶粉封闭液室温封闭2 h,置于一抗(小鼠抗大鼠Bcl-2、Bax单克隆抗体,稀释倍数均为 1 ∶200)中4 ℃孵育过夜,次日TBST洗膜10 min×3次后置于二抗(HRP标记山羊抗小鼠IgG,稀释倍数1 ∶4 000)中室温孵育2 h,TBST洗膜,ECL化学发光显影后凝胶成像系统拍照。Image-Pro Plus软件进行图像分析,以条带的灰度值代表蛋白的表达量,用Bcl-2 (Bax )/β-actin比值代表蛋白定量表达水平,Bcl-2/Bax比值代表细胞抗凋亡水平。
1.2.6 统计学方法采用SPSS 19.0统计软件进行分析;计量资料用x±s表示,完全随机设计资料的多个样本均数比较用单因素方差分析(ANOVA),组间两两比较采用LSD检验;检验水准α=0.05。 2 结果 2.1 肾脏组织病理学评估
光镜观察显示(图 1),Sham组肾小管上皮细胞形态规则,刷状缘完整;Pp组见大量肾小管上皮细胞肿胀、空泡变性,部分细胞刷状缘脱落,核深染、裸露,严重者可见核固缩、核碎裂、核溶解,肾小管管腔扩张明显,可见坏死、崩解的上皮细胞,部分肾间质炎症细胞浸润;与Pp组相比,IP1、IP3及IP5组肾小管损伤减轻,仅表现为部分肾小管上皮细胞肿胀,刷状缘消失,个别肾小管管腔可见脱落细胞及碎片。
 |
| A:Sham组;B: Pp组;C:IP1组;D:IP3组;E:IP5组 图 1 不同次数的缺血预处理后CO2气腹模型大鼠肾脏组织光镜观察 (HE×200, n=6) |
与Sham组相比,Pp组及各IP组MDA水平显著升高,SOD及T-AOC水平显著降低(P<0.05);而与Pp组相比,IP1、IP3及IP5组MDA显著减少,SOD及T-AOC显著增加(P<0.05),其中IP3组MDA低于IP1、IP5组(与IP1组比较,P<0.05;与IP5组比较,P>0.05),SOD高于IP1、IP5组(P<0.05),T-AOC高于IP1、IP5组(与IP1组比较,P<0.05;与IP5组比较,P>0.05,图 2)。
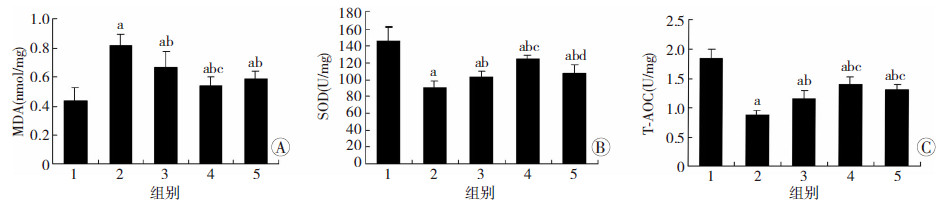 |
| 1:Sham组, 2:Pp组, 3:IP1组, 4:IP3组, 5:IP5组; a: P<0.05,与Sham组比较;b: P<0.05,与Pp组比较;c: P<0.05,与IP1组比较;d: P<0.05,与IP3组比较 图 2 不同次数的缺血预处理对CO2气腹模型大鼠肾组织MDA含量(A)、SOD活性(B)及T-AOC活性(C)的影响 (n=6) |
Sham组肾皮质可见少量Bcl-2、Bax表达;Pp组和各IP组肾皮质可见大量Bcl-2、Bax表达,其中Bcl-2定位表达于近曲小管和远曲小管上皮细胞胞质内,而肾小球无明显表达,Bax主要分布于近曲、远曲肾小管上皮细胞胞质,肾小球也有少量表达(图 3)。经半定量分析,Pp组Bcl-2、Bax IOD值显著高于Sham组(P<0.05);而与Pp组相比,各IP组Bcl-2 IOD值均升高,其中IP3组显著升高,差异有统计学意义(IP1、IP3组与Pp组比较,P<0.05;IP5组与Pp组比较,P>0.05)。与Pp组相比,各IP组Bax IOD值降低,其中IP3组降低最明显,差异有统计学意义(IP1、IP3组与Pp组比较,P<0.05;IP5组 与Pp组比较,P>0.05,图 4)。
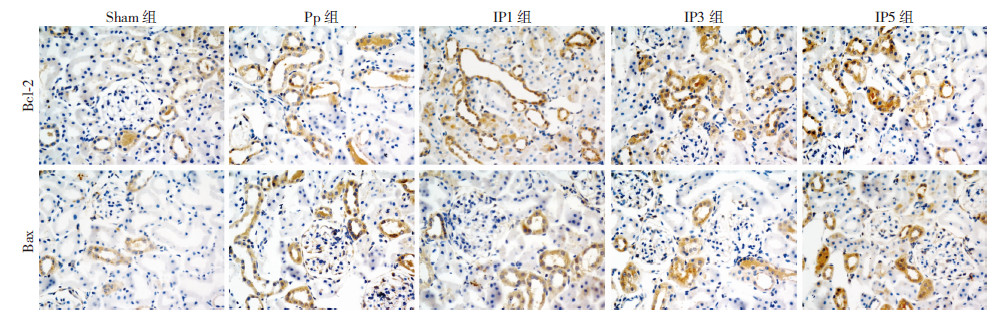 |
| 图 3 免疫组化检测缺血预处理对CO2气腹模型大鼠肾脏Bcl-2、Bax蛋白表达的影响 (二步法 ×400,n=6) |
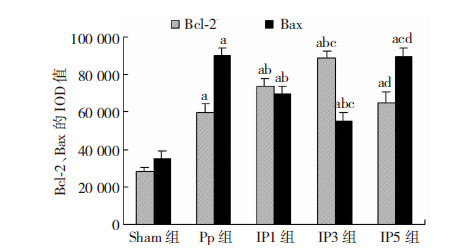 |
| a: P<0.05,与Sham组比较;b: P<0.05,与Pp组比较;c: P<0.05,与IP1组比较;d: P<0.05,与IP3组比较 图 4 各组大鼠肾组织Bcl-2、Bax的IOD值比较 |
与Sham组比较,Pp组及各IP组Bcl-2、Bax蛋白的表达均升高;与Pp组相比,各IP组Bcl-2表达升高(P<0.05),Bax表达降低(P<0.05),Bcl-2/Bax比值显著升高(P<0.05);各IP组间比较,IP3组Bcl-2/Bax比值升高最明显(P<0.05,图 5)。
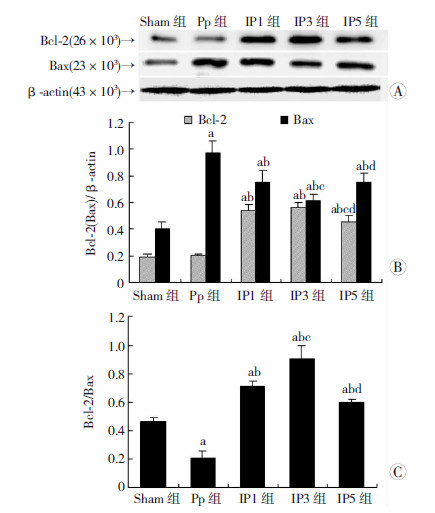 |
| A:不同次数的缺血预处理对肾脏Bcl-2、Bax蛋白表达的影 响;B:各组大鼠肾组织Bcl-2(Bax)/β-actin值的比较;C:各 组大鼠肾组织Bcl-2/Bax值的比较;a: P<0.05,与Sham组比较;b: P<0.05,与Pp组比较;c: P<0.05,与IP1组比较;d: P<0.05,与IP3组比较 图 5 Western blot检测缺血预处理对CO2气腹模型大鼠肾脏Bcl-2、Bax蛋白表达的影响 (n=6) |
相比于传统开腹手术,腹腔镜手术具有多项优越性,已成为外科重要的诊断和治疗手段[8]。术中建立CO2气腹压迫肾脏血管,使肾脏处于低氧低灌注状态,而术后气腹的解除增加肾脏血流灌注及供氧,造成组织缺血再灌注损伤[9, 10]。大量实验研究显示,CO2气腹缺血预处理对肾脏缺血再灌注损伤有确切的保护作用,其效应常于一次或反复多次短暂缺血再灌注循环后观察获得。然而,预处理方案中循环次数各文献报道不一。Yilmaz等[11]首次提出CO2气腹缺血预处理时采用充放气1次的IP方案,张豪杰等[7]则是在气腹前交替2次充气放气,而Altindis等[12]的预处理方法是充气5 min放气5 min,连续3次后再建立CO2气腹。由于缺血预处理方案的最佳循环次数还未确定,本实验旨在探讨气腹前给予不同缺血预处理次数对气腹所致肾脏缺血再灌注损伤的影响及其机制。
我们通过建立大鼠CO2气腹模型证实,气腹可造成肾I/RI,其组织病理学表现为肾小管上皮细胞肿胀、空泡变性、甚至坏死、崩解,刷状缘脱落,管腔扩张,肾间质炎症细胞浸润;而经预处理后,虽然同样存在上述改变,但损伤程度明显减轻,表明缺血预处理对肾脏I/RI存在保护作用。
目前认为,氧化应激反应与细胞凋亡是腹腔镜手术肾I/RI的重要机制。本研究显示:建立CO2气腹后,肾组织中MDA水平增高、SOD及T-AOC活性下降。 其中,MDA是组织细胞氧化应激损伤程度的重要标志;SOD是生物体内最佳且最重要的氧自由基清除剂,T-AOC由酶促和非酶促抗氧化系统共同组成,其值高低反映整体抗氧化应激防御体系能力强弱。三者的变化提示,CO2气腹致肾脏缺血再灌注后,机体内氧化应激反应即被激活,氧自由基及其活性衍生物生成增多,由此造成脂质过氧化产物增加,抗氧化物被消耗及总抗氧化能力降低[13]。而经缺血预处理后,肾组织中MDA水平明显降低,SOD及T-AOC活性增加,说明缺血预处理可能通过积极启动内源性抗损伤机制,使机体对缺血再灌注损伤产生主动性适应反应,上调酶性抗氧化物SOD水平,增加机体总抗氧化能力T-AOC,促进组织及时清除氧自由基,减少脂质过氧化产物MDA的生成,最终减弱CO2气腹所致肾I/RI。本实验在缺血再灌注前给予不同预处理次数,发现其对肾组织损伤程度明显不同。以10 mmHg压力充气5 min 放气5 min,连续1次的CO2气腹缺血预处理方案即可通过减弱氧化应激反应对大鼠肾脏缺血再灌注损伤产生保护作用,但不能明显改善因CO2气腹造成的肾脏损伤,与Yilmaz等[11]的研究结果相一致;而连续3次缺血预处理的保护作用显著增强,继续增加预处理次数(5次)保护效果反而有所下降。这表明适当范围内增加缺血预处理次数对肾脏I/RI有一定保护作用,呈次数依赖性,但继续盲目增加预处理次数,并不能产生累加性保护效果,其机制尚待进一步研究。
研究表明,缺血再灌注损伤后,肾组织内细胞凋亡信号通路激活,导致肾损伤[14, 15]。本实验结果显示,建立CO2气腹后,肾组织中Bcl-2及Bax表达均上调,Bcl-2/Bax比值下降;而经缺血预处理后,Bcl-2表达上调,Bax表达下调,且Bcl-2/Bax比值显著增高。Bcl-2与Bax是目前已知的凋亡调控过程中功能相互对立的一对最重要的调控基因,其编码的蛋白产物Bcl-2/Bax比值决定着细胞命运,检测其含量对研究肾缺血再灌注损伤中细胞凋亡具有重要意义。由此我们推断,CO2气腹的建立可诱导肾组织中Bcl-2及Bax蛋白表达,使Bcl-2/Bax比值下降,细胞凋亡增加,肾组织损伤加重;而缺血预处理通过预适应积极启动自身保护机制,上调Bcl-2蛋白表达,下调Bax蛋白表达,使Bcl-2/Bax比值明显增高,减少缺血再灌注后肾脏细胞凋亡,最终减轻其损伤程度。另外,实验也提示,预处理1次则能通过上调Bcl-2蛋白表达,下调Bax蛋白表达,增高Bcl-2/Bax比值对肾脏缺血/再灌注后细胞凋亡发挥保护作用,验证了杨旭凯等[16]的观点。且增加预处理次数(3次)后其对抗细胞凋亡作用更加明显,继续增加预处理次数(5次),其保护作用反而减弱。
综上所述,CO2气腹可致肾脏缺血再灌注损伤,而在建立气腹前行3次缺血预处理能够通过增强机体抗氧化能力,减少细胞凋亡,显著减弱CO2气腹诱导肾脏缺血再灌注损伤,其保护机制可能与缺血预处理直接降低氧化应激状态下的活性氧的生成,上调Bcl-2抗凋亡蛋白,下调Bax凋亡蛋白表达有关。
| [1] | Litynski G S, Paolucci V. Origin of laparoscopy coincidence or surgical interdisciplinary thought[J]. World J Surg, 1998, 22(8): 899-902. |
| [2] | Kiray S, Onalan G, Karabay G, et al. Antioxidant prophylaxis for cellular injury in ovarian surface epithelium resulting from CO2 pneumoperitoneum in a laparoscopic rat model[J]. Arch Gynecol Obstet, 2011, 284(3): 765-772. |
| [3] | Sammour T, Mittal A, Loveday B P, et al. Systematic review of oxidative stress associated with pneumoperitoneum[J]. Br J Surg, 2009, 96(8): 836-850. |
| [4] | Yiannakopoulou ECh, Nikiteas N, Perrea D, et al. Effect of laparoscopic surgery on oxidative stress response: systematic review[J]. Surg Laparosc Endosc Percutan Tech, 2013, 23(2): 101-108. |
| [5] | Sahin D A, Haliloglu B, Sahin F K, et al. Stepwise rising CO2 insufflation as an ischemic preconditioning method[J]. J Laparoendosc Adv Surg Tech A, 2007, 17(6): 723-729. |
| [6] | Murry C E, Jennings R B, Reimer K A. Preconditioning with ischemia a delay of lethal cell injury in ischemic myocardium[J]. Circulation, 1986, 74(5): 1124-1136. |
| [7] | 张豪杰, 王国民, 孙立安, 等. 大鼠CO2气腹模型中不同气腹压力对肾的影响及缺血预处理的作用[J]. 复旦学报: 医学版, 2007, 34(3): 251-254, 363. |
| [8] | 刘彩云, 王长友, 毕敬涛. 腹腔镜胆囊切除术对机体氧化应激的影响[J]. 中国综合临床, 2006, 22(2): 158-159. |
| [9] | 朱以祥, 王卫星. 气腹预处理对腹腔镜手术大鼠肝脏保护作用的实验研究[J]. 微循环学杂志, 2008, 18(1): 11-12. |
| [10] | 于金玲, 朱江帆. 腹腔镜手术CO2气腹导致的肝缺血再灌注损伤及其对策[J]. 中国微创外科杂志, 2007, 7(1): 67-69. |
| [11] | Yilmaz S, Koken T, Tokyol C, et al. Can preconditioning reduce laparoscopy-induced tissue injury?[J]. Surg Endosc, 2003, 17(5): 819-824. |
| [12] | Altindis M, Yilmaz S, Polat C, et al. Sequential periods of preconditioning decrease laparoscopy-related elevations in hepatic TNF-alpha and IL-6 levels in rats[J]. J Laparoendosc Adv Surg Tech A, 2004, 14(6): 380-383. |
| [13] | Koksal H, Kurban S. Total oxidant status, total antioxidant status, and paraoxonase and arylesterase activities during laparoscopic cholecystectomy[J]. Clinics (Sao Paulo), 2010, 65(3): 285-290. |
| [14] | 宣吉晴, 李明星. Bcl-2基因与肾缺血再灌注损伤[J]. 泸州医学院学报, 2011, 34(3): 314-316. |
| [15] | 刘晶晶, 赵砚丽, 程会平, 等. 缺血后处理对肾缺血再灌注损伤大鼠肾组织细胞凋亡及bcl-2和bax基因表达的影响[J]. 第四军医大学学报, 2007, 28(21): 1960-1963. |
| [16] | 杨旭凯, 程彦斌. 缺血预处理对急性肾缺血再灌注细胞凋亡、增殖及Bcl-2蛋白表达的影响[J]. 第四军医大学学报, 2003, 24(10): 884-886. |



