钆塞酸二钠(gadolinium ethoxybenzyl diethylene-triaminepentaacetic acid,Gd-EOB-DTPA,商品名:普美显)是一种顺磁、亲水、离子性且可溶于水的肝细胞造影剂[1, 2],已作为一种全球化的肝脏磁共振(magnetic resonance,MR)增强对比剂广泛使用[3, 4, 5]。Gd-EOB-DTPA能够提供给药后几分钟内的血管和给药20 min以后特殊的肝细胞摄取期图像[6]。肝细胞期肝脏病灶和肝实质的信号对比明显,因此Gd-EOB-DTPA通常被用来作为肝癌的一种MR检测手段[7]。由于Gd-EOB-DTPA注射速率慢、剂量小、浓度高等特殊性,MR增强动脉期图像与常规MR造影剂动脉期图像强化效果不同,采集时相的把握和采集方法的选择成为研究的一个热点。
动脉相是MR动态成像首过时相,对如肝细胞癌和肝血管瘤等腹部占位病变性质的鉴别诊断非常重要。Gd-EOB-DTPA肝脏动态增强动脉期图像依然存在几个问题:第一,Gd-EOB-DTPA注射剂量和体积分别为常规MR钆剂的1/4(0.025 mmol/kg Gd-EOB-DTPA vs 0.1 mmol/kg Gd-DTPA) 和1/2 (0.1 mL/kg Gd-EOB-DTPA vs 0.2 mL/kg Gd-DTPA)[8];第二,Gd-EOB-DTPA注射剂量较小,动脉期注射时间很短(5~10 s),MR序列动脉期扫描时间为15 s左右,准确抓住动脉期难度较大;第三,Gd-EOB-DTPA的T1弛豫效应为常规钆剂的2倍,不适当的动脉期扫描会诱导K空间中心的信号迅速提高,由边缘震荡效应产生伪影[9]。目前的研究表明,Gd-EOB-DTPA肝脏MR动脉期扫描推荐使用非稀释的造影剂,注射速率为1 mL/s或2 mL/s,运用MR荧光示踪技术观察造影剂的动脉循环流程,选适当扫描开始时间点的采集方式合适[6, 10, 11, 12, 13, 14]。注射速率过慢将影响肝脏动脉期的强化效果,Gd-EOB-DTPA联合MR荧光示踪技术对注射速率低于2 mL/s的动脉期图像采集方法所得动脉期图像的质量差异性比较尚少见报道。
本研究主要比较Gd-EOB-DTPA注射速度分别为1 mL/s和1.5 mL/s肝脏动脉期图像质量,比较低于2 mL/s 注射速度所得动脉期图像质量的差异性,探讨是否有将造影剂的注射速率选择在大于1 mL/s,小于2 mL/s的必要性,权衡优化Gd-EOB-DTPA肝脏动态增强动脉期的扫描方式以提高动脉期图像质量。
1 资料与方法 1.1 临床资料回顾性分析从2012年12月至2013年9月在西南医院放射科接受3.0T Gd-EOB-DTPA肝脏肿瘤特异性检查的826例患者,该检查项目经本院伦理委员会批准。动脉期图像入选标准:①无MRI检查禁忌证;②无磁共振Gd-EOB-DTPA肝脏检查史;③动脉期图像可用于临床诊断;④Gd-EOB-DTPA注射后用20 mL生理盐水冲洗;⑤Gd-EOB-DTPA注射速率为1 mL/s和1.5 mL/s;⑥成功且完成磁共振Gd-EOB-DTPA肝脏动态增强检查。排除标准:①重复本项检查患者(n=58);②不适当的动脉期图像采集时间:过早(n=85),过晚(n=48);③注射后因紧张、咳嗽或呼吸困难等原因无法配合完成动脉期图像采集(n=39);④没有完成检查(n=26);⑤生理盐水注射剂量非20 mL(n=258);⑥Gd-EOB-DTPA注射速度非1 mL/s和1.5 mL/s (n=206)。总共106例纳入本研究。
1.2 MR技术所有患者行3.0T MRI检查,使用Siemens Trio 3.0T(Siemens Trio,Erlangen,Germany)超导型磁共振扫描仪,线圈为8通道体表线圈。患者体位为头先进 仰卧位,18G留置针连接肘静脉与高压注射器(Spectris Solaris EP,MR Injection System,Medrad,ST1011765,US),匀速注射。所有患者分为两组:第1组,造影剂和生理盐水注射速度为1.0 mL/s 52例;第2组,造影剂和生理盐水注射速度为1.5 mL/s 54例,两组患者造影剂注射后均加20 mL生理盐水以相同的注射速度冲洗。扫描序列:冠状位2次闭气半傅立叶采集单次激发快速自旋回波序列 (half-fourier acquisition single- short turbo spin-echo,haste) [重复时间(TR)1 000 ms,回波时间(TE)91 ms,翻转角(FA)150°,矩阵(matrix)320×256,视野(FOV)358 mm×358 mm,层厚(slice thickness)6 mm,扫描时间(scan time)22~26 s]:轴位2次闭气T2 haste(TR 1 000 ms,TE 88 ms,FA 150°,矩阵350×267,FOV 350~390 mm×262~292 mm,层厚6 mm,扫描时间22~30 s),轴位单次闭气T1加权正反相位成像序列(TR 206 ms,TE 2.45、3.83 ms,FA 65°,矩阵256×192,FOV 350~390 mm×262~292 mm,层厚6 mm,扫描时间18 s)。单次闭气三维容积内插体部检查序列(three-dimensional volume interpolated breath-hold examination,3D-VIBE) (TR 3.42 ms,TE 1.45 ms,FA 9°,矩阵320×225,FOV=400~420 mm×280~300 mm,层厚2~2.5 mm,扫描时间15 s)给药前采集1次,给药后用MR荧光示踪技术示踪造影剂的位置(造影剂到达处MR图像血管呈现高信号),当腹主动脉上段信号强度增高(图 1)开始行3D-VIBE采集为动脉期,给药后60 s(门脉期)、180 s(平衡期)、10 min(肝胆期)和15 min(肝细胞期)用3D-VIBE序列采集。
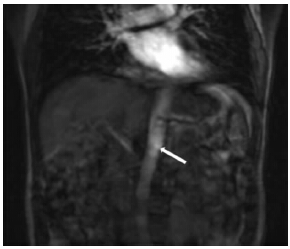 |
| ↑:示动脉期图像采集时刻,Gd-EOB-DTPA到达腹主动脉上段图 1 MR荧光示踪技术造影剂到达腹主动脉上段表现 |
所有肝脏动脉期图像在我院PACS系统上分析。
定量分析:增强前后分别测量肝脏实质、腹主动脉和肝总动脉信号强度值(signal intensity,SI),同时测量相应背景的信号标准差。用直径为10 mm左右感兴趣区域(regions of interest,ROI)在肝脏左中右段分别测量肝脏实质的SI 1次,取均值为SI实质,测量时避开肝脏肿瘤、大血管和结节区域。腹主动脉和肝总动脉用直径为5 mm左右的ROI在3个层面测量3次取均值分别为SI腹主和SI肝总。用直径为5 mm左右的ROI测量3个层面的背景信号标准差取平均值为背景信号的平均标准差SD背景。
定量指标的计算:信噪比(signal noise ratio,SNR)= SI/SD;强化率(contrast-enhancement ratio,CER)=SI增强前-SI增强后/SI增强前。其中SI增强前为注射Gd-EOB-DTPA前测量部位的信号强度,SI增强后为注射Gd-EOB-DTPA后对应部位的信号强度。
半定量分析:2名副高以上放射科医师对所有图像的肝脏实质、腹主动脉、肝总动脉和门静脉的强化程度以及图 像有无呼吸伪影5个项目进行半定量评分,评
估方法如下:①肝脏实质:1分=无强化,2分=强化效果一般,3分=强化效果好;②腹主动脉:1分=无强化,2分=强化效果一般(腹主动脉SI与肝脏实质SI接近),3分=强化效果好;③肝总动脉:1分=无强化,2分=强化效果一般,3分=强化效果好;④门静脉:1分=无强化,2分=强化效果一般,3分=强化效果好;⑤呼吸伪影:1分=严重,2分=一般,3分=无。若评估个体结果不一致,则讨论得出一致结果作为最后的半定量评分结果。
采用SPSS 18.0统计软件对所有数据进行统计学分析,结果以x±s形式表示。运用Mann-Whitney U检验比较两组患者的平均年龄和平均体质量有无区别,χ2检验比较两组患者性别、乙肝、肝硬化和原发性肝癌分布有无区别。用两个独立样本Wilcoxon秩和检验比较两组患者的肝脏实质、腹主动脉和肝总动脉的SNR及CER、半定量评分总分和各项得分有无区别。
2 结果 2.1 临床资料比较1 mL/s组和1.5 mL/s组年龄、性别、体质量、慢性乙型肝炎、肝硬化和原发性肝癌分布无统计学差异(P>0.05)。两组患者的临床资料基本一致。结果见表 1。
| 组别 | n | 年龄(岁) | 男性/女性 | 体质量 (kg) | 患者背景资料 | 肝脏恶性肿瘤(非原发性肝癌) | ||||||||
|
慢性乙型病 毒性肝炎 | 慢性丙型病 毒性肝炎 | 肝硬化 | 原发性 肝癌 | 肝血 管瘤 | 鼻咽癌 | 肝胆管型 细胞癌 | 乳腺癌 | 直肠癌 | 胆管 结石 | |||||
| 1 mL/s组 | 52 | 46.73±13.25 | 42/10 | 62.64±12.26 | 24 | 1 | 23 | 25 | 2 | 1 | 0 | 0 | 1 | 0 |
| 1.5 mL/s组 | 54 | 49.89±12.71 | 49/5 | 59.83±9.13 | 31 | 0 | 22 | 18 | 1 | 1 | 0 | 0 | 2 | 0 |
| P值 | 0.14a | 0.14b | 0.21a | 0.25b | 0.72b | 0.12b | ||||||||
a: P值通过 Mann-Whitney U检验计算;b:P值通过χ2检验计算
两组患者肝实质、腹主动脉和肝总动脉的SNR及CER无统计学差异(P>0.05,表 2)。
| 组别 | n | SNR | CER | ||||
| 肝实质 | 腹主动脉 | 肝总动脉 | 肝实质 | 腹主动脉 | 肝总动脉 | ||
| 1 mL/s组 | 52 | 124.23±22.99 | 316.43±82.89 | 229.64±49.41 | 0.15±0.06a | 2.74±1.13 | 2.42±0.87 |
| 1.5 mL/s组 | 54 | 131.90±24.75 | 318.60±82.01 | 227.28±61.78 | 0.17±0.09 | 2.77±0.89 | 2.32±0.69 |
| P值 | 0.08 | 0.72 | 0.99 | 0.17 | 0.73 | 0.73 | |
1 mL/s组患者腹主动脉强化评分高于1.5 mL/s组(P=0.005),肝总动脉评分和半定量总分也高于1.5 mL/s组(P值分别为0.007、0.003)。结果见表 3,图 2。
| 组别 | n | 腹主动脉强化评分 | 肝总动脉强化评分 | 肝脏实质强化评分 | 门静脉强化评分 | 呼吸伪影 | 总分 |
| 1 mL/s组 | 52 | 2.84±0.43 | 2.82±0.44 | 1.73±0.53 | 1.57±0.58 | 2.55±0.61 | 11.51±1.45 |
| 1.5 mL/s组 | 54 | 2.55±0.61 | 2.53±0.61 | 1.61±0.63 | 1.69±0.55 | 2.33±0.65 | 10.71±1.35 |
| P值 | 0.005 | 0.007 | 0.190 | 0.280 | 0.080 | 0.003 |
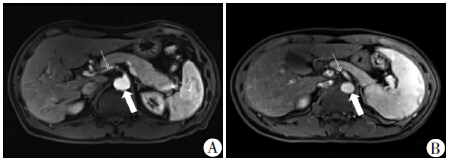 |
 :示腹主动脉; ↑:示肝总动脉 A:1 mL/s组;B:1.5 mL/s组图 2 不同注射速度钆塞酸二钠磁共振肝脏动态增强动脉期表现 :示腹主动脉; ↑:示肝总动脉 A:1 mL/s组;B:1.5 mL/s组图 2 不同注射速度钆塞酸二钠磁共振肝脏动态增强动脉期表现 |
本研究结果显示,在2组患者临床资料分布基本一致的前提下,注射速度为1 mL/s和1.5 mL/s组患者肝脏实质、腹主动脉和肝总动脉动脉期图像的SNR和CER没有统计学差异(P>0.05)。半定量评分结果显示,2名放射科医师一致认为注射速度为1 mL/s 组的腹主动脉强化 效果好于1.5 mL/s组(P=0.005),1 mL/s组肝总动脉强化效果好于1.5 mL/s组(P=0.007),1 mL/s组腹主动脉强化得分、肝总动脉强化得分、肝脏实质强化得分、门静脉强化得分、呼吸伪影5项总得分好于1.5 mL/s组(P=0.003),两组动脉期图像肝实质和门静脉强化得分无统计学差异(P>0.05),呼吸伪影严重程度也无统计学差异(P>0.05)。虽然定量评估Gd-EOB-DTPA动脉期图像各项指标显示注射速度为1 mL/s和1.5 mL/s组无统计学差异,但是半定量评分结果显示注射速度为1 mL/s组的肝脏动脉期图像明显优于注射速度为1.5 mL/s组,主要体现在腹主动脉和肝总动脉血管强化效果更好(图 2)。由于1 mL/s注射速度小于1.5 mL/s注射速度,因此理论上越低注射速度造影剂在血管停留的时间越长,采集时相把握越好,在没有严重的呼吸伪影的前提下获得的动脉期图像质量也就越好。这和本研究的半定量评分是一致的,也与以往文献[15]报道的结果一致。
动脉期是MR肝脏动态增强首过时相,对于疾病的定性诊断非常重要。常规MR造影剂的注射速度为3 mL/s[6],由于Gd-EOB-DTPA的高浓度和高T1弛豫效应,注射速度不应过快,关于Gd-EOB-DTPA注射速度和注射方法对动脉期图像质量的影响,国外有文献报道,但观点不一。Chung等[15]研究结果显示,利用Test-bolus法采集动脉期图像,运用SNR和肿瘤对比肝脏实质信噪比CNR评估动脉期图像,得到注射速度为1 mL/s和2 mL/s组动脉期图像质量均可满足诊断,无统计学差异。Zech等[16]研究结果显示,Gd-EOB-DTPA注射速度为1 mL/s较注射速度为2 mL/s能得到更好的主动脉峰值强化效果。Tamada等[6]研究结果显示非稀释Gd-EOB-DTPA注射速度为1 mL/s获得的动脉期图像质量优于非稀释Gd-EOB-DTPA注射速度为3 mL/s及稀释1/3 Gd-EOB-DTPA注射速度为3 mL/s获得的动脉期图像质量。以上研究结果认为Gd-EOB-DTPA注射速度不应过快,为1~2 mL/s,1 mL/s 注射速度动脉期图像的SNR和CNR较常规注射速度有优势,与2 mL/s动脉期图像质量对比差别观点不一,推荐使用MR荧光示踪方法示踪,但是没有对小于2 mL/s注射速度动脉期图像的强化效果归纳总结,也没有给出推荐Gd-EOB-DTPA的注射方法。本研究结果提示,注射速度小于2 mL/s两组动脉期图像定量评估结果没有统计学差异,但是诊断医师更愿意看到注射速度为1 mL/s的动脉期图像,因为1 mL/s组肝脏实质的SNR和CER都不太高,小于1.5 mL/s组,更能突出病灶和肝脏实质的对比。
本研究仍存在一定的局限性。首先,没有比较更多的注射速度,例如低于1 mL/s的注射速度动脉期图像的质量,因为注射速度越慢,造影剂在动脉血管的停留时间会更长。其次,对肝细胞癌动脉期图像的评估,Gd-EOB-DTPA的效果不如CT动态增强[17],注射速度越快对于病变的强化效果就越好,但是与肝脏实质的对比(信噪比)也就越差,由于Gd-EOB-DTPA的高T1弛豫效应的独特性以及前期研究报道,限制了其给药速度。因此,如何寻找一种注射方法使得Gd-EOB-DTPA动脉期的图像质量最接近于CT动态增强动脉期的图像质量,以达到在造影剂稀释比例和注射速率及时相采集之间寻找一个平衡点,优化肝脏动脉期图像质量的目标,值得深入研究。
综上所述,非稀释的Gd-EOB-DTPA以1 mL/s的速 度注射,MR荧光示踪法示踪,之后给予20 mL生理盐水冲洗得到的肝脏动脉期图像更能满足诊断的需求。
| [1] | Zeng M S,Ye H Y,Guo L,et al. Gd-EOB-DTPA-enhanced magnetic resonance imaging for focal liver lesions in Chinese patients:a multicenter,open-label,phase Ⅲ study[J]. Hepatobiliary Pancreat Dis Int,2013,12(6):607-616. |
| [2] | Reimer P,Rummeny E J,Shamsi K,et al. Phase Ⅱ clinical evaluation of Gd-EOB-DTPA:dose,safety aspects,and pulse sequence[J]. Radiology,1996,199(1):177-183. |
| [3] | Fujinaga Y,Ohya A,Tokoro H,et al. Radial volumetric imaging breath-hold examination (VIBE) with k-space weighted image contrast (KWIC) for dynamic gadoxetic acid (Gd-EOB-DTPA)-enhanced MRI of the liver:advantages over Cartesian VIBE in the arterial phase[J]. Eur Radiol,2014,24(6): 1290-1299. |
| [4] | Vogl T J,Kummel S,Hammerstingl R,et al. Liver tumors:comparison of MR imaging with Gd-EOB-DTPA and Gd-DTPA[J]. Radiology,1996,200(1):59-67. |
| [5] | Bluemke D A,Sahani D,Amendola M,et al. Efficacy and safety of MR imaging with liver-specific contrast agent:U.S. multicenter phase Ⅲ study[J]. Radiology,2005,237(1): 89-98. |
| [6] | Tamada T,Ito K,Yoshida K,et al. Comparison of three different injection methods for arterial phase of Gd-EOB-DTPA enhanced MR imaging of the liver[J]. Eur J Radiol,2011,80(3): e284-e288. |
| [7] | Kim J E,Kim S H,Lee S J,et al. Hypervascular hepatocellular carcinoma 1 cm or smaller in patients with chronic liver disease:characterization with gadoxetic acid-enhanced MRI that includes diffusion-weighted imaging[J]. AJR Am J Roentgenol,2011,196(6): W758-W765. |
| [8] | Hamm B,Staks T,Muhler A,et al. Phase I clinical evaluation of Gd-EOB-DTPA as a hepatobiliary MR contrast agent:safety,pharmacokinetics,and MR imaging[J]. Radiology,1995,195(3): 785-792. |
| [9] | Stadler A,Schima W,Ba-Ssalamah A,et al. Artifacts in body MR imaging:their appearance and how to eliminate them[J]. Eur Radiol,2007,17(5): 1242-1255. |
| [10] | Sun H Y,Lee J M,Shin C I,et al. Gadoxetic acid-enhanced magnetic resonance imaging for differentiating small hepatocellular carcinomas (< or =2 cm in diameter) from arterial enhancing pseudolesions:special emphasis on hepatobiliary phase imaging[J]. Invest Radiol,2010,45(2): 96-103. |
| [11] | Cruite I,Schroeder M,Merkle E M,et al. Gadoxetate disodium-enhanced MRI of the liver:part 2,protocol optimization and lesion appearance in the cirrhotic liver[J]. AJR Am J Roentgenol,2010,195(1): 29-41. |
| [12] | Motosugi U,Ichikawa T,Sou H,et al. Dilution method of gadolinium ethoxybenzyl diethylenetriaminepentaacetic acid (Gd-EOB-DTPA)-enhanced magnetic resonance imaging (MRI) [J]. J Magn Reson Imaging,2009,30(4):849-854. |
| [13] | Schmid-Tannwald C,Herrmann K,Oto A,et al. Optimization of the dynamic,Gd-EOB-DTPA-enhanced MRI of the liver:the effect of the injection rate[J]. Acta Radiol,2012,53(9): 961-965. |
| [14] | Haradome H,Grazioli L,Tsunoo M,et al. Can MR fluoroscopic triggering technique and slow rate injection provide appropriate arterial phase images with reducing artifacts on gadoxetic acid-DTPA (Gd-EOB-DTPA)-enhanced hepatic MR imaging? [J]. J Magn Reson Imaging,2010,32(2): 334-340. |
| [15] | Chung S H,Kim M J,Choi J Y,et al. Comparison of two different injection rates of gadoxetic acid for arterial phase MRI of the liver[J]. J Magn Reson Imaging,2010,31(2): 365-372. |
| [16] | Zech C J,Vos B,Nordell A,et al. Vascular enhancement in early dynamic liver MR imaging in an animal model:comparison of two injection regimen and two different doses Gd-EOB-DTPA (gadoxetic acid) with standard Gd-DTPA[J]. Invest Radiol,2009,44(6):305-310. |
| [17] | Kanata N,Yoshikawa T,Ohno Y,et al. HCC-to-liver contrast on arterial-dominant phase images of EOB-enhanced MRI:comparison with dynamic CT[J]. Magn Reson Imaging,2013,31(1): 17-22. |



