慢性细菌性前列腺炎(chronic bacterial prostatitis,CBP)是男科临床常见疾病,其发病率近年呈上升趋势[1]。目前利用动物模型研究CBP尚无公认的方法,在建模时有开腹前列腺直接注射[2]、经尿道逆行注入细菌[3]等方法,多采用开腹直接向大鼠前列腺组织注射大肠埃希杆菌的方法。我们在行开腹建立慢性细菌性前列腺炎模型时发现开腹手术耗费时间较长,大鼠开腹伤口易加大腹腔感染的概率,导致死亡率升高。而寻找稳定的符合疾病病理表现的动物模型是研究发病机制及治疗的重要前提。在超声引导下经直肠前列腺穿刺活检的临床实践[4]的启发下,本研究选择在超声引导下经腹直接向大鼠前列腺注射菌液的方式建立动物模型,以期创建一种新型、方便、安全的建模方式。
1 材料与方法 1.1 试剂与仪器采用标准致病大肠埃希菌(ATCC25922),37 ℃培养过夜,以比浊法用无菌生理盐水配成1.5 ×108/mL菌液,恒温震荡摇床、小动物超声仪、3%戊巴比妥钠、10%甲醛溶液、光学显微镜均由第三军医大学新桥医院中心实验室提供。
1.2 实验动物与分组成年SD大鼠36只,雄性,清洁级,体质量280~300 g,由第三军医大学动物实验中心提供。采用抽签法分为空白对照组、传统慢性细菌性前列腺炎模型(tradition chronic bacterial prostatitis model,TCBP)组、超声引导慢性细菌性前列腺炎模型(ultrasound chronic bacterial prostatitis model,UCBP)组,每组12只。
1.3 动物模型建立 1.3.1 传统慢性细菌性前列腺炎模型的建立[5]3%戊巴比妥钠(20 mg/kg)用1 mL无菌注射器腹腔注射,与大鼠腹部皮肤呈斜角30°进针,回抽无液体后将3%戊巴比妥钠注入大鼠腹腔,妥善麻醉后,固定头部及四肢,备大鼠下腹部皮肤,常规消毒铺巾,取大鼠下腹部1.5~2 cm切口,严格无菌操作,无齿镊提起膀胱,暴露前列腺两叶,用1 mL无菌注射器将1.5×108/mL菌液注射入前列腺各0.1 mL,空白对照组注入等量无菌生理盐水。逐层关闭切口,缝皮前用碘伏消毒皮肤。完毕后送回动物房,常规饲料喂养。
1.3.2 超声引导下慢性细菌性前列腺炎模型的建立3%戊巴比妥钠(20 mg/kg)用1 mL无菌注射器腹腔注射,与大鼠腹部皮肤呈斜角30°进针,回抽无液体后将3 %戊巴比妥钠注入大鼠腹腔,妥善麻醉后,固定头部及四肢,备大鼠下腹部皮肤,常规消毒铺巾,一名实验人员左手向左右两侧固定绷紧大鼠下腹部皮肤,右手使用小动物超声仪(Vevo 2100),探头频率21 MHz,以大鼠下腹部区域为声窗,待屏幕中显示大鼠前列腺影像后固定超声切面。另一实验人员双手操作使用1 mL无菌注射器在超声引导下穿刺入前列腺 组织,将1.5×108/mL菌液缓慢注射入前列腺各0.1 mL。 完毕后送回动物房,常规饲料喂养。
1.3.3 建模完成后大鼠的处理记录每只大鼠的建模时间,分别于第0、1、2、3、4周称量各组大鼠的体质量,所有大鼠喂养4周后,腹腔注射过量3%戊巴比妥钠处死所有大鼠,打开腹腔,取出大鼠前列腺组织,用于制作石蜡包埋切片。
1.4 石蜡切片及炎症评分将大鼠前列腺组织用10%福尔马林溶液固定24 h,常规石蜡包埋切片,并用HE染色,每个标本切8张切片,切片厚度为5 μm,光镜下观察大鼠的前列腺组织中的腺体、导管和间质的变化。根据Bahk等[6]的方法计算石蜡切片中的炎症评分:每张切片中随机取5个高倍视野,计算镜下视野中病变部位与整个视野的面积之比,无病变计0分,25%计1分,50%计2分,75%计3分,100%计4分。
1.5 统计学处理计量资料用x±s表示,采用SPSS 13.0统计软件进行单因素方差分析。
2 结果 2.1 大鼠体质量与建模时间建模手术时间,UCBP组建模时间(7.83±1.53)较TCBP组的建模手术时间(17.17±1.64)短(P < 0.05);建模完成后,空白对照组大鼠皮毛亮泽光滑,喜活动,食欲好。TCBP组及UCBP组大鼠在术后第1周食欲不佳,活动少,体质量增加幅度较小,在术后2~4周食欲与活动较术后第1周明显好转,体质量也稳步增加。术后空白对照组体质量与TCBP组、UCBP组相比差异有统计学意义(P < 0.05,表 1)。空白对照组大鼠无死亡,TCBP组大鼠死亡3只,UCBP组大鼠死亡1只。
| 组别 | 第0周 | 第1周 | 第2周 | 第3周 | 第4周 |
| 空白对照组 | 292.7±6.2 | 345.1±9.8 | 389.9±7.9 | 433.7±8.4 | 482.4±7.9 |
| TCBP组 | 292.3±8.7 | 305.1±9.6 a | 334.8±8.0 a | 370.8±9.4 a | 425.8±7.4 a |
| UCBP组 | 292.0±7.2 | 306.1±9.4 a | 335.5±9.7 a | 372.9±11.0 a | 428.7±8.8 a |
| a: P < 0.05,与空白对照组比较 | |||||
处死3组大鼠取其前列腺,在解剖过程中空白对照组前列腺与周围组织边界清晰无明显粘连,而TCBP组及UCBP组前列腺组织与周围粘连严重,有大量脂肪组织包裹前列腺与膀胱。大体标本可见TCBP组及UCBP组前列腺体积较空白对照组增大(图 1)。空白对照组前列腺炎颜色呈淡红色,触之柔软;TCBP组及UCBP组前列腺颜色呈充血的鲜红色且质地较空白对照组稍硬。HE染色可见空白对照组大鼠腺体多为不规则椭圆,腔隙大小不一,有皱襞,间质内少量结缔组织及纤维组织,间质内无炎性细胞浸润(图 2A)。TCBP组(图 2B)及UCBP组(图 2C)中可见腺上皮增生、腺体肿胀扩张,炎性细胞浸润腺腔及间质,可见纤维组织增生。TCBP组及UCBP组在炎症评分中所选指标均显著高于空白对照组(P < 0.05,表 2)。
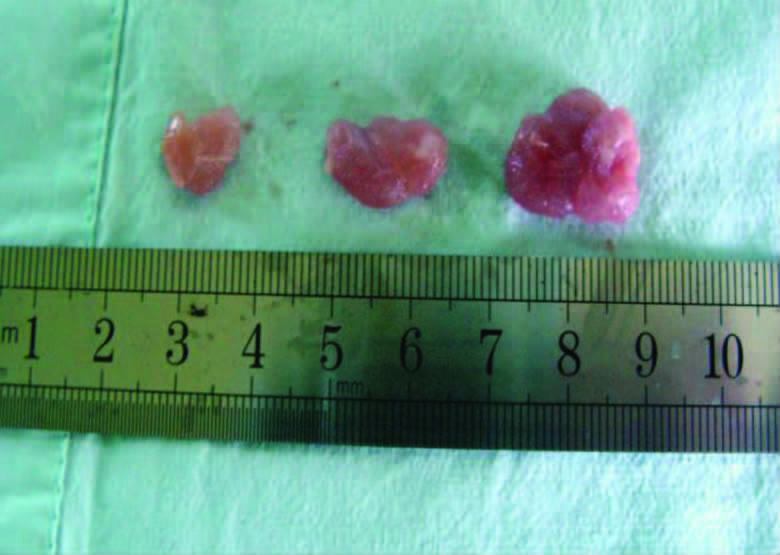 |
| 从左到右依次为空白对照组、TCBP组、UCBP组 图 1 各组大鼠前列腺组织大体观察 |
 |
| A:空白对照组;B:TCBP组;C:UCBP组 图 2 各组大鼠前列腺组织病理学观察 (HE ×400) |
| 组别 | 腺体形态改变 | 炎性细胞浸润 | 纤维组织增生 |
| 空白对照组 | 0.20±0.07 | 0.23±0.04 | 0.28±0.06 |
| TCBP组 | 3.22±0.31 a | 3.71±0.37 a | 3.80±0.29 a |
| UCBP组 | 3.24±0.36 a | 3.65±0.41 a | 3.70±0.33 a |
| a:P<0.05,与空白对照组比较 | |||
TCBP组建模过程中死亡大鼠见腹腔内肠道充气,大量腹腔积液液,手术切口处大量网膜覆盖,前列腺组织色暗红,其他组织未见明显异常,UCBP组内建模过程中死亡大鼠亦见腹腔内肠道充气,大量腹腔积液液,前列腺组织色暗红,其他组织未见明显异常,其余建模成功大鼠处死后观察大鼠腹腔内,未见腹腔脓肿、包块形成,未见膀胱充血等炎症表现,摘取大鼠肝、肾、脾、膀胱等组织制作切片光镜下观察,未见异常。
3 讨论慢性细菌性前列腺炎是泌尿外科临床工作中的常见感染性疾病[1],已被证明是前列腺被病原体持续或反复感染的一种下尿路感染[7]。构建一种稳定、可复制的慢性细菌性前列腺炎动物模型是深入研究慢性细菌性前列腺炎发生、发展不可缺少的工具。大鼠是前列腺炎造模及其实验研究的最常用动物之一,注射细菌等微生物感染是最广泛使用的前列腺炎造模方法[8, 9]。我们在前期研究中采用前列腺开放注射办法建立前列腺炎模型,但是在建模过程中发现传统的建模方式即直接开腹向大鼠前列腺注射细菌的建模方式容易造成大鼠死亡且模型的手术时间较长。
超声检查是目前诊断盆腔病变常用检查方法之一[10],超声引导下穿刺活检是在超声监视下利用自动弹射活检枪及活检针对感兴趣区域取材进行病理检查的一种方法,具有简便、安全等优点,在肝脏、前列腺、乳腺等占位性病变的诊断中应用较多[11, 12],且超声引导下穿刺活检能够实时动态显示血流及针尖的确切位置等情况,有效地避开血管、神经等组织,能快速并安全准确地到达指定位置,目前已广泛应用于临床[13]。
通过临床和文献的启发,我们使用超声引导下细针直接穿刺大鼠前列腺注射大肠埃希菌的方式建立慢性细菌性前列腺炎大鼠模型,在术后1 周内可以观察到,与空白对照组大鼠相比较其余两组大鼠精神、食欲差,体质量上升幅度明显较低,考虑为大肠埃希菌对大鼠机体造成影响所致,而从第2周开始两组建模组大鼠体质量逐渐回升,考虑为机体已逐渐适应,在随后的几周TCBP、UCBP组大鼠体质量及其增加幅度无明显差异(P>0.05)。在模型手术时间上UCBP组较TCBP组时间短且死亡的大鼠亦较TCBP组少。在病理变化及炎症评分上TCBP组和UCBP组无明显差异(P>0.05),但都显著高于空白对照组(P < 0.05),呈现慢性炎症改变。
综上所述,本研究成功地使用超声引导下细针直接穿刺大鼠前列腺注射大肠埃希菌建立了慢性细菌性前列腺炎大鼠模型。这种方式的优势在于可以避免开腹使大鼠受到手术的应激而增加死亡率,且可以降低模型建立的时间,具有稳定性,可复制性且快捷、安全的特点,有望在今后的研究中得到广泛的应用。但是本实验方法较传统建模方法而言亦有一定的缺点,在建模前需进行一定程度的训练来提高穿刺的准确率以及穿刺时使用力度的大小,并且相关超声仪器的使用亦需要学习,如何克服这些缺点使超声引导下建模更加完善将是我们下一步的研究目标。
| [1] | Kim H W, Ha U S, Woo J C, et al. Preventive effect of selenium on chronic bacterial prostatitis[J]. J Infect Chemother, 2012, 18(1): 30-34. |
| [2] | Nickel J C, Olson M E, Barabas A, et al. Pathogenesis of chronic bacterial prostatitis in an animal model[J]. Br J Urol, 1990, 66(1): 47-54. |
| [3] | 明爱民, 沈学成, 周占松, 等. 纳米细菌致Ⅲ型前列腺炎的实验研究[J]. 第三军医大学学报, 2009, 31(11): 1005-1008. |
| [4] | 谢峰, 金耀泉, 吴平, 等. 66例肝硬化患者超声引导下门静脉穿刺介入治疗后并发症发生的临床分析[J]. 第三军医大学学报, 2013, 35(16): 1767-1768. |
| [5] | 陈江川, 刘城城, 韩广玮, 等. 不同浓度大肠杆菌制作大鼠慢性细菌性前列腺炎模型探讨[J]. 局解手术学杂志, 2013, 22(5): 463-465. |
| [6] | Bahk T J, Daniels M D, Leon J S, et al. Comparison of angiotensin converting enzyme inhibition and angiotensin Ⅱ receptor blockade for the prevention of experimental autoimmune myocarditis[J]. Int J Cardiol, 2008, 125(1): 85-93. |
| [7] | Yoon B I, Bae W J, Choi Y S, et al. The anti-inflammatory and anti-microbial effects of anthocyanin extracted from black soybean on chronic bacterial prostatitis rat model[J]. J Sex Med, 2013, 10(Suppl 3): 245. |
| [8] | 文晓东. 慢性前列腺炎动物实验研究概况[J]. 甘肃中医, 2005, 18(5): 47-48, 封四. |
| [9] | 施新猷. 现代医学实验动物学[M]. 北京: 人民军医出版社, 2000: 479-480. |
| [10] | 黄泽君, 杨正春, 李芳, 等. 乳腺癌术后局部复发的超声表现[J]. 第三军医大学学报, 2012, 34(13): 1332-1335. |
| [11] | Hakime A, Barah A, Deschamps F, et al. Prospective comparison of freehand and electromagnetic needle tracking for US-guided percutaneous liver biopsy[J]. J Vasc Interv Radiol, 2013, 24(11): 1682-1689. |
| [12] | Suh H J, Moon H J, Kwak J Y, et al. Anaplastic thyroid cancer: ultrasonographic findings and the role of ultrasonography-guided fine needle aspiration biopsy[J]. Yonsei Med J, 2013, 54(6): 1400-1406. |
| [13] | 战勇, 于晓玲, 梁萍, 等.超声引导下穿刺活检在腹膜后病变中的应用价值[J].解放军医学院学报, 2014, 35(3): 204-207. |



