胆汁淤积是常见的临床综合征,其发病率和诊断率越来越高。多项研究表明,胆汁淤积的发生与肝细胞表面胆汁酸转运蛋白的异常表达密切相关[1, 2]。这些转运蛋白包括:钠依赖牛磺胆酸共转运体(Na+/taurocholate cotransporting polypeptide,NTCP)、阴离子转运多肽(organic anion transporting polypeptide,OATP)、胆盐输出泵(bile salt export pump,BSEP)、多药耐药蛋白2(multidrug resistance-2,MDR2)、多药耐药相关蛋白2(multidrug resistance-associated protein 2,MRP2)等。近年研究表明:MRP2在调控胆汁酸排泌方面发挥着重要的作用[3, 4]。人类原发性胆小管硬化性胆汁淤积症、Dubin-Johnson综合征等疾病与其减少密切相关。动物实验发现,肝细胞胆管膜面的Mrp2表达降低可导致胆汁淤积[5]。目前,MRP2的表达调控机制并不清楚。已有研究表明,RXRα与法尼酸受体FXR、CAR和孕烷受体PXR形成异二聚体参与MRP2基因转录的调控[6, 7]。
Ezrin(EZR)为细胞膜-细胞骨架连接蛋白,主要表达于上皮细胞,尤其在小肠、胃、肺、胰腺、肾脏、肝脏中高表达[8]。Ezrin主要由3个结构域组成:①氨基端高度保守的球形结构,即FERM区;②α螺旋区;③伸向胞浆的羧基端,其中有一个可与F-action相连接的高度保守的氨基酸序列,而Ezrin的磷酸化位点也位于此区,参与Ezrin蛋白的活化[9]。骨架蛋白EZR主要在肝细胞胆管膜面表达,其异常表达或分布异常将导致细胞正常生理功能的异常。近年研究表明,EZR即能参与细胞的生长和信号转导,有可接受胞外信号,使细胞骨架重排[10]。因此,我们建立了EZR表达缺失的HepG2细胞,并研究其表达缺失对肝细胞胆管膜面的胆汁酸转运蛋白MRP2的影响,旨在为临床治疗胆汁淤积提供新的线索。
1 材料与方法 1.1 材料HepG2细胞购自中科院上海细胞研究所;DMEM培养基、胎牛血清、Opti-MEM Ⅰ Reduced Serum Medium购自Gibco公司;X-tremeGENE HP DNA Transfection Reagen、蛋白酶抑制剂、磷酸酶抑制剂购自Roche公司;Streptavidin Agarose Resins、EZ-Link Sulfo-NSS-SS-Biotin购自Pierce Biotechnology公司;EZR、MRP2购自Epitomics公司;羊抗兔二抗购自Pierce Biotechnology公司;Ezrin-shRNA质粒由上海吉凯基因化学技术有限公司提供。
1.2 方法 1.2.1 Ezrin-shRNA-HepG2稳转细胞株的建立参考文献[11]的方法,转染Ezrin-shRNA#1、Ezrin-shRNA#2、Ezrin-shRNA#3及Control质粒。操作过程根据X-tremeGENE HP DNA Transfection Reagen说明书完成。X-tremeGENE HP DNA Transfection Reagen:DNA复合物=3 ∶1。常规培养细胞24 h,更换新鲜的10% FBS-DMEM培养基并用1 000 μg/mL G418进行阳性筛选7 d后,挑选单克隆稳定转染细胞株,继续用500 μg/mL G418持续筛选3周,获得稳定转染细胞株,扩大培养。提取细胞RNA,筛选出能够有效抑制EZR基因表达的细胞株。
1.2.2 RT-qPCR按TRIzol说明书提取细胞RNA。逆转录为cDNA后进行RT-qPCR扩增。PCR反应体系:20 μL体系中5′端和3′端引物各0.4 μL(10 μmol/L)、dNTPs 1.6 μL(2.5 μmol/L)、Template 1 μL(10 ng/μL)、Taq polymerase 0.2 μL、5×Taq Buffer 4 μL、ddH2O 12.4 μL,反应条件:94 ℃ 5 min,94 ℃ 30 s,55 ℃ 30 s,72 ℃ 2 min 30个循环,72 ℃ 10 min。引物序列见表1。
| 基因 | 引物序列(5′→3′) | 长度(bp) |
| MRP2 | 上游:CTCACTTCAGCGAGACCCG下游:CCAGCCAGTTCAGGGGTTT | 191 |
| EZR | 上游:TTGTGGCTTGCTCTGTGCT下游:AACACCGAACGACACACGA | 261 |
| GAPDH | 上游:CCACGAAACTACCTTCAACTCC下游:CTTTGGTATCGTGGAAGGACTC | 252 |
按EZ-Link Sulfo- NSS-SS-Biotin说明书进行操作。冰冷的PBS液清洗细胞后,6孔板每孔加入1 mL Biotin Solution,4 ℃反应1 h,使膜蛋白充分Biotin化,加入2.5 mL/孔的冰冷反应终止液洗涤2次。按照文献[11]的方法提取总膜蛋白,进行蛋白免疫印迹实验。
1.2.4 蛋白免疫印迹按照文献[11]的方法提取细胞总蛋白,并进行SDS-PAGE电泳,上样量为20 μg/孔。浓缩胶60 V电泳1 h,分离胶100 V电泳2 h,常规湿法转膜80 min,含5%脱脂奶粉的TBST室温封闭2 h,一抗(EZR 1 ∶20 000,Na+-K+-ATPase 1 ∶50 000)4 ℃孵育过夜,用TBST吸取一抗后加入相应的二抗(1 ∶50 000),室温孵育1 h。ECL化学发光,凝胶成像系统显影。
1.3 统计学方法数据以 x±s表示,采用SPSS 13.0统计软件行t检验。
2 结果 2.1 成功建立并筛选了EZR表达缺失的HepG2细胞稳转细胞株将Ezrin-shRNA#1、Ezrin-shRNA#2、Ezrin-shRNA#3、Ezrin-shRNA#4及control质粒转染HepG2细胞后,筛选稳转细胞。提取各株细胞的RNA,RT-qPCR检测EZR基因的表达情况,结果表明Ezrin-shRNA#3、Ezrin-shRNA#4质粒能够有效抑制HepG2细胞EZR基因的表达(P<0.01),其中Ezrin-shRNA#3效果最优,抑制率达70%,在后续实验中选择使用Ezrin shRNA#3-HepG2。
2.2 EZR表达缺失对HepG2细胞MRP2总蛋白的表达无明显影响Ezrin shRNA#3-HepG2的EZR mRNA表达缺失最显著,因此,选择提取Ezrin shRNA#3-HepG2细胞总蛋白,检测EZR表达缺失对HepG2细胞MRP2总蛋白的表达影响。蛋白免疫印迹检测结果显示,与对照组相比,Ezrin shRNA#3-HepG2组细胞MRP2表达增高,但差异无统计学意义(图1)。这提示EZR表达缺失对HepG2细胞MRP2总蛋白的表达无明显影响。
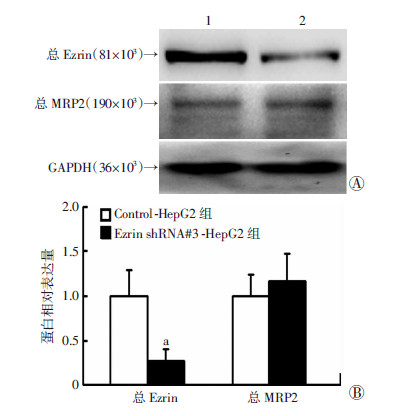 |
| A: 蛋白免疫印迹检测结果 1:Control-HepG2组;2:Ezrin shRNA#3-HepG2组;B:半定量分析结果 a:P<0.01,与Contorl-HepG2组比较 图 1 蛋白免疫印迹检测MRP2总蛋白在Ezrin shRNA#3-HepG2 中的表达 |
为进一步明确胆汁淤积时EZR蛋白与MRP2蛋白的关系,我们提取生物素化的Ezrin-shRNA#3-HepG2和Control-HepG2细胞的总膜蛋白,检测EZR表达缺失与MRP2膜蛋白的关系。结果表明:与Control-HepG2细胞相比,Ezrin-shRNA#3-HepG2细胞膜表面的MRP2表达量明显增高(P<0.01,图2),而胞浆中的MRP2膜蛋 白的表达量也明显增高(P<0.01,图3)。表明EZR表达缺失能够明显上调HepG2细胞MRP2总膜蛋白的表达。
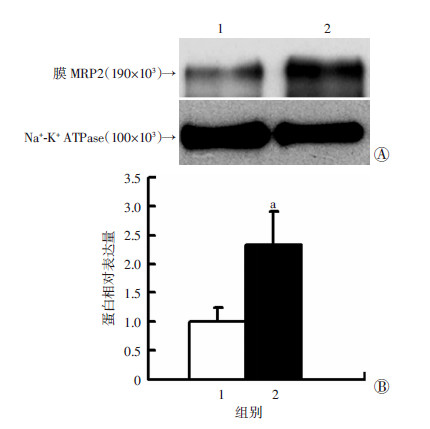 |
| 1:Control-HepG2组;2:Ezrin shRNA#3-HepG2组 A: 蛋白免疫印迹检测结果;B:半定量分析结果 a:P<0.01,与Contorl-HepG2组比较 图 2 蛋白免疫印迹检测MRP2膜蛋白在Ezrin shRNA#3-HepG2 细胞胞膜上的表达 |
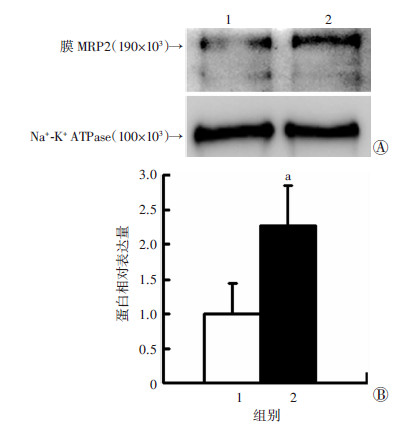 |
| 1:control-HepG2组;2:Ezrin shRNA#3-HepG2组 A: 蛋白免疫印迹检测结果;B:半定量分析结果 a:P<0.01,与Contorl-HepG2组比较图 3 蛋白免疫印迹检测MRP2膜蛋白在Ezrin shRNA#3-HepG2 细胞胞浆中的表达 |
MRP2为一种ATP依赖的胆酸转运蛋白,分布于肝细胞胆管膜面,主要以各种胆盐以及利福平、普伐他汀等药物为底物,是维持肝脏正常生理功能的重要蛋白[12]。胆汁淤积时,MRP2表达降低后,机体能够相应地作出适应性反应以代偿MRP2的功能,但是这种代偿功能并不能完全取代MRP2的作用保护肝脏处于正常状态。因此,胆酸转运蛋白MRP2在维持正常的肝细胞功能方面发挥着极其重要的作用。动物模型表明,Mrp2在胆汁淤积发生时其肝脏mRNA、总蛋白水平并未发生明显变化,而肝细胞胆管膜面Mrp2的定位表达却显著减少[13]。这可能提示胆汁淤积下肝细胞胆管面膜MRP2的表达下降主要是转录后调控。但是目前该调控机制尚不清楚。
ERM家族蛋白作为细胞骨架相关蛋白,主要包括EZR、RDX和MSN,是将细胞表面蛋白与细胞内部其他分子之间连接起来的桥梁。EZR又称艾兹蛋白,主要分布在极性化细胞的表面,参与细胞形态维持、运动、黏附、信号传递和生存等多种功能。最近的研究表明,ERM家族具有调节肝细胞表面胆汁酸转运蛋白的作用[14]。在胆道梗阻、药物性肝损、原发性硬化性胆管炎、自身免疫性肝炎等原因引起的胆汁淤积中,均发现EZR蛋白表达下降或分布异常。在肠上皮Caco-2细胞中,骨架蛋白Ezrin还可与Mrp2、F-action相互作用[15]。我们的前期研究表明[11],该家族的另一成员RDX影响胆酸转运蛋白BSEP在HepG2细胞的定位表达。MRP2属于功能性蛋白,本身不具备运动转移功能。而文献[11]与本研究结果均表明:胆汁淤积时,MRP2在肝细胞胆管膜面的定位表达减少。我们前期关于RDX的研究中并未发现其与MRP2的定位表达具有相关性。因此,我们猜测ERM家族另一锚定蛋白EZR可能与MRP2的定位表达有关。
为了验证该假设,本研究构建了Ezrin表达缺失的HepG2稳转细胞,对MRP2总蛋白进行检测,明确了Ezrin表达缺失对MRP2总蛋白无影响,从而进一步验证了我们关于MRP2转录后调控的推测。而通过生物素化反应检测MRP2膜蛋白的表达变化,则初步确认了在HepG2细胞中,Ezrin表达缺失后,MRP2膜蛋白表达增高。Ezrin为锚定蛋白,主要是通过与其他蛋白形成复合物,促进蛋白在细胞的定位表达,我们怀疑Ezrin表达缺失后,原定位于细胞膜的MRP2蛋白从胞膜解离进入胞浆,从而导致胞浆中MRP2膜蛋白表达增高。因此,该研究为后续研究胆汁淤积时MRP2的转录后调控机制提供了可能的方向。
| [1] | Keppler D. The roles of MRP2, MRP3, OATP1B1, and OATP1B3 in conjugated hyperubinemia[J]. Drug Metab Dispos, 2014, 42(4): 561-565. |
| [2] | Gossard A A, Talwalkar J A. Cholestatic liver disease[J]. Med Clin North Am, 2014, 98(1): 73-85. |
| [3] | Wagner M, Zollner G, Trauner M. New molecular insights into the mechanisma of cholestasis[J]. J Hepatol, 2009, 51(3): 565-580. |
| [4] | Sekine S, Yano K, Saeki J, et al. Oxidative stress is a triggering factor for LPS-induced Mrp2 internalization in the cryopreserved rat and human liver slices[J]. Biochem Biophys Res Commun, 2010, 399(2): 279-285. |
| [5] | Anakk S, Watanabe M, Ochsner S A, et al. Combined deletion of Fxr and Shp in mice induces Cyp17a1 and results in juvenile onset cholestasis[J]. J Clin Invest, 2011, 121(1): 86-95. |
| [6] | 吴晓平, 张保新, 张晓娟, 等.多耐药相关蛋白MRP2与核受体RXRα、RARα在人阻塞性胆汁淤积肝组织中的表达变化[J]. 胃肠病学和肝病学杂志, 2011,20(8): 769-770. |
| [7] | Chen W, Cai S Y, Xu S, et al. Nuclear receptor RXRalpha: RARalpha are repressors for human MRP3 expression[J]. Am J Physiol Gastrointest Liver Physiol, 2007, 292(5): G1221-G1227. |
| [8] | Neisch A L, Fehon R G. Ezrin, Radixin and Moesin: key regulators of membrane-cortex interactions and signaling[J]. Curr Opin Cell Biol, 2011, 23(4): 377-382. |
| [9] | Niggli V, Rossy J. Ezrin/radixin/moesin: versatile controllers of signaling molecules and of the cortical cytoskeleton[J]. Int J Biochem Cell Biol, 2008, 40(3): 344-349. |
| [10] | Maniti O, Carvalho K, Picart C. Model membranes to shed light on the biochemical and physical properties of ezrin/radixin/moesin [J]. Biochimie, 2013, 95(1): 3-11. |
| [11] | 封欣婵, 柴进, 程英, 等. Radixin定点突变过表达对HepG2细胞膜转运蛋白Bsep的影响[J]. 第三军医大学学报, 2014, 36(10): 1002-1007. |
| [12] | Ren L, Hong S H, Cassavaugh J, et al. The actin-cytoskeleton linker protein ezrin is regulated during osteosarcoma metastasis by PKC[J]. Oncogene, 2009, 28(6): 792-802. |
| [13] | Rost D, Kloeters-Plachky P, Stichl A. Retrieval of the rat canalicular conjugate export pump Mrp2 is associated with a rearrangement of actin filaments and radixin in bile salt-induced cholestasis[J]. Eur J Med Res, 2008, 13(7): 314-318. |
| [14] | Nakano T, Sekine S, Ito K, et al. Correlation between apical localization of Abcc2/Mrp2 and phosphorylation status of ezrin in rat intestine[J]. Drug Metab Dispos, 2009, 37(7): 1521-1527. |
| [15] | Yang Q, Onuki R , Nakai C, et al. Ezrin and radixin both regulate the apical membrane localization of ABCC2 (MRP2) in human intestinal epithelial Caco-2 cells[J]. Exp Cell Res, 2007, 313(16): 3517-3525. |



