急性肝衰竭 (acute liver failure,ALF)是在原来无肝病基础上发生的肝功能急剧受损,短期内发生以肝性脑病、凝血功能障碍为主要临床表现的临床综合征。其起病急,疾病进展迅猛,死亡率在60%~90%,且救治相当困难,肝移植是目前唯一有效的治疗措施 [1, 2]。然而,急性肝衰竭又是可逆的,部分患者无需肝移植、经内科综合治疗后能自然存活。另外,供肝来源困难、肝移植费用高等因素也决定了大多数ALF患者不可能接受肝移植治疗。因此,哪些患者需要肝移植、何时进行肝移植成为肝病内、外科医师需要解决的难题。为优化ALF患者的临床治疗路径、特别是为适时选择肝移植治疗提供帮助,国内外学者多年来一直希望能根据患者的临床表现与常规实验室检查结果构建1个预测系统或模型来有效预测ALF患者的短期预后。
为了预测肝硬化患者经颈静脉肝内门体分流术(transjugular intrahepatic portosystemic shunt,TIPS)治疗的预后及评估不同阶段肝硬化患者的短期生存率,2000年Mayo[3]临床小组首次提出了终末期肝病模型(the model for end-stage liver disease,MELD)。MELD 评分近年也被用于评估急性肝衰竭与慢加急性肝衰竭患者的近期预后。随着临床肝病学者对肝病规律认识的深入,近年来又在MELD模型基础上,发展出MELD 评分结合血清钠浓度(MELD with incorporation of sodium,MELD-Na)、MELD 综合评分(integrated MELD,IMELD)、英国终末期肝病模型(united kingdom model for end-stage liver disease,UKELD)等预后评分模型[4, 5, 6]。
然而,上述4种预测模型在评估急性肝衰竭患者短期预后时均存在不同的缺陷。MELD、MELD-Na、IMELD与UKELD等模型都是基于欧美终末期肝病与肝衰竭患者的临床资料分析结果而建立的。然而,欧美国家肝病与肝衰竭的病因主要以药物、特别是对乙酰氨基酚中毒和酒精为主,我国则主要为HBV感染为主,因此尚不清楚上述4种模型是否适用于我国ALF患者的短期预后评估。为此,我们在对我院收治的224例ALF患者的临床资料进行回顾性分析基础上,构建了一种能预测ALF患者短期预后的新Logistic回归模型,并比较了其与上述4种模型对ALF患者3个月死亡危险性评估的优劣。
1 资料与方法 1.1 研究对象筛选224例2000年1月至2012年12月间第三军医大学西南医院感染科住院部收治的住院患者,其诊断均符合我国2012 年《肝衰竭诊疗指南》中制订的ALF临床诊断标准[7],排除慢性肝衰竭,慢加急性肝衰竭及肝癌等恶性肿瘤所致的肝衰竭。研究采用回顾性病例对照研究,记录每例患者住院期间以及3个月后的病情转归,其中存活组为55例,179例死亡者为对照组。234例病例中,男性118例,女性116例,年龄为(36.9±17.8)岁。以上资料的获取均取得患者知情以及西南医院伦理委员会的同意。
1.2 方法从每份病历中录入患者入院时或入院后达到急性肝衰竭诊断标准时的人口学与临床资料及实验室检查结果,主要有性别、年龄、丙氨酸氨基转移酶(ALT)、门冬氨酸氨基转移酶(AST)、总胆红素(TBIL)、白蛋白(ALB)、国际标准化比率(INR)、白细胞(WBC)、血红蛋白(HGB)、血小板(PLT)、血钠(Na+)、血糖(Glu)、血肌酐(Cr)、腹水(Ascites)、肝性脑病(HE)、上消化道出血(UGIH)、急性肾功能不全(ARI)、细菌或真菌感染(Infections)等相关指标。根据预后分为存活组与死亡组。
1.3 构建Logistic回归模型使用SPSS 19.0统计软件对数据进行分析,计量资料用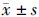 表示,Wilcoxon秩和检验和卡方检验分别检测两组间计量资料和计数资料的差异。统计学方法应用Logistic多因素回归分析法,以两组间有显著差异的指标为自变量(纳入标准:P<0.05),以患者3个月的结局为应变量,通过Forward Stepwise (Likelihood Ratio)法变量逐步筛选,纳入标准:P<0.05,剔除水准:P>0.1,最后通过Logistic系数及常数项构建模型。使用MedCalc 12. 3.0 软件对各评分系统之间AUC 的比较进行分析。
表示,Wilcoxon秩和检验和卡方检验分别检测两组间计量资料和计数资料的差异。统计学方法应用Logistic多因素回归分析法,以两组间有显著差异的指标为自变量(纳入标准:P<0.05),以患者3个月的结局为应变量,通过Forward Stepwise (Likelihood Ratio)法变量逐步筛选,纳入标准:P<0.05,剔除水准:P>0.1,最后通过Logistic系数及常数项构建模型。使用MedCalc 12. 3.0 软件对各评分系统之间AUC 的比较进行分析。
根据文献中的公式计算MELD、MELD-Na、 IMELD、UKELD四种模型评分[4, 5, 6],分别如下:MELD= 9.57×Ln(Cr)+3.78×Ln(TB)+11.2×Ln (INR)+6.43×病因(胆汁淤积或酒精为0,病毒或其他为1);MELD-Na=MELD+1.59×(135-Na+) ( Na+范围: 120~135mmol/L);IMELD=MELD+(年龄×0.3)-(0.7×Na+)+100;UKELD=5×[1.5×Ln (INR)+0.3×Ln (Cr)+0.6×Ln (TB)-13×Ln (Na+)+70]。应用受试者工作特征曲线法(receiver operating characteristic,ROC)检验模型对ALF患者3个月死亡危险性的预测能力,曲线下面积( area under the curve of ROC,AUC)在0.8~0.9为预测准确性佳,具有较好的临床应用价值,>0.7为有临床应用价值,<0.7则预测能力很差,>0.9认为具有较高临床应用价值。根据ROC曲线的敏感度,特异度以及约登指数决定各评分对ALF患者3个月死亡危险性预测的灵敏度、特异性、阳性及阴性预测值。
2 结果 2.1 病因分布病毒性肝炎仍是导致我国急性肝衰竭的主要原因。共有107例(45.72%)患者为病毒性肝炎,其中79例(33.76%)为乙肝病毒感染,12例(5.13%)为戊肝病毒感染,3例甲肝病毒感染,1例为乙肝和戊肝重叠感染,1例为甲肝和戊肝重叠感染,1例为乙肝和丙肝重叠感染; 59例(25.12%)患者为不明原因所致肝衰竭;药物性肝衰竭共55例(23.50%),包括抗结核药物24例(10.25%),中草药20例(8.54%),免疫抑制剂所致5例,非甾体类抗炎药所致3例,抗生素所致2例,丙硫氧嘧啶所致1例;原发性甲亢所致4例,自身免疫性肝炎2例;其他病毒感染包括巨细胞病毒感染3例,EBV感染2例,单纯疱疹病毒感染2例。
2.2 患者的基线特征本组234例患者中,55例患者经非肝移植的内科 治疗后存活时间超过3个月,3个月存活率为23.50%,179例患者在入院后3个月内死亡,病死率为76.50%。对存活组与死亡组患者达到ALF诊断标准时的基线特征进行比较。分析结果发现,年龄、性别、丙氨酸氨基转移酶、门冬氨酸氨基转移酶、血糖、血红蛋白及上消化道出血在两组间的分布并无统计学差异(P>0.05),而总胆红素、国际标准化比率、白蛋白、白细胞、血小板、血钠、血肌酐、腹水、肝性脑病、急性肾功能不全及细菌或真菌感染11项因素与ALF预后存在相关性,两组间分布存在统计学差异(P<0.05,表 1)。
| 指标 | 存活组 (n=55) | 死亡组 (n=179) | P值 |
| 年龄(岁) | 33.0±16.0 | 38.2±18.1 | 0.056 |
| 性别 | |||
| 男性 | 21(38.2%) | 97(54.2%) | |
| 女性 | 34(61.8%) | 82(45.8%) | 0.055 |
| ALT(IU/L) | 1 140.3±1 068.7 | 881.4±1275.4 | 0.174 |
| AST(IU/L) | 811.2±723.2 | 838.2±1202.0 | 0.875 |
| TB(mg/dL) | 18.2±10.1 | 24.7±10.4 | 0.000 |
| Alb(g/L) | 34.4±5.7 | 30.6±5.6 | 0.000 |
| INR | 2.3±0.7 | 3.4±2.0 | 0.000 |
| CR(mg/dL) | 0.8±0.3 | 1.1±0.8 | 0.020 |
| Na+(mmol/L) | 135.5±8.5 | 131.3±8.6 | 0.002 |
| GLU(mmol/L) | 5.4±2.5 | 5.1±2.6 | 0.478 |
| WBC×109/L | 7.6±2.8 | 10.9±6.4 | 0.000 |
| HGB(g/L) | 118.5±22.8 | 111.0±28.9 | 0.075 |
| PLT×109/L | 155.7±83.9 | 125.5±75.9 | 0.019 |
| Ascites | 10(18.2%) | 78(43.6%) | 0.000 |
| HE | 9(16.4%) | 72(40.2%) | 0.001 |
| UGIH | 1(1.8%) | 11(6.7%) | 0.146 |
| ARI | 1(1.8%) | 21(11.7%) | 0.017 |
| Infections | 8(14.5%) | 82(45.8%) | 0.000 |
将表 1中对预后有显著影响的变量(P<0.05),进一步纳入Logistic多因素回归分析。经过先后5步筛选,最后筛选出TB、INR、Na+、Ascites、Infections 5个 与预后具有独立相关性的指标(表 2)。TB(OR 1.077,95%CI 1.028~1.130,P=0.002),INR(OR 2.555,95%CI 1.561~4.182,P=0.000),Na+(OR 0.938,95%CI 0.883~0.996,P=0.037),Ascites (OR 2.804,95%CI 1.140~6.892,P=0.025),Infections(OR 5.348,95%CI 2.268~12.610,P=0.000)。通过优势比可以看出血清Na+为ALF预后相关保护性因素,Na+指标值越高,死亡危险性将会降低,而TB、INR、腹水及感染为相关危险性因素,TB、INR指标值及发生腹水与感染并发症概率越高,ALF患者死亡危险性将会升高。通过Logistic系数及常数项构建预测急性肝衰竭3个月预 后的Logistic模型(the model for acute liver failure,MALF): P=1/[1+exp(-y)],y= 4.448+0.074×TB+ 0.938×INR-0.064×Na++1.031×腹水+1.677×感染;其中P值为患者预后的死亡概率,腹水与感染取值为0或1。此模型AUC为0.952(95%CI 0.907~0.997),准确度为95.29%,敏感度为98.03%,特异度为97.26%,阳性预测值为99.44%,阴性预测值为90.90%(表 3)。
| 变量 | 回归系数β | 标准误 | 统计量 | 优势比 | 95%可信区间 | P值 |
| TB | 0.074 | 0.024 | 9.512 | 1.077 | 1.028~1.130 | 0.002 |
| INR | 0.938 | 0.251 | 13.932 | 2.555 | 1.561~4.182 | 0.000 |
| Na+ | -0.064 | 0.031 | 4.347 | 0.938 | 0.883~0.996 | 0.037 |
| Ascites | 1.031 | 0.459 | 5.046 | 2.804 | 1.140~6.892 | 0.025 |
| Infections | 1.677 | 0.438 | 14.681 | 5.348 | 2.268~12.610 | 0.000 |
| Constant | 4.448 | 4.159 | 1.144 | 85.429 | 0.285 |
| 组别 | MELD | MELD-Na | IMELD | UKELD | MALF |
| 自然存活组 | 25.03±4.61 | 27.22±7.34 | 40.05±9.52 | 60.09±5.17 | 0.09±0.29 |
| 死亡/肝移植组 | 31.56±6.84 | 37.83±10.32 | 51.25±11.32 | 66.03±6.30 | 0.99±0.75 |
| P值 | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 |
| AUC | 0.783 | 0.825 | 0.793 | 0.841 | 0.952 |
| 95%可信区间 | 0.720~0.845 | 0.762~0.887 | 0.726~0.860 | 0.781~0.901 | 0.907~0.997 |
| 准确度 | 80.44% | 87.15% | 84.91% | 88.83% | 95.29% |
| 阳性预测值 | 84.21% | 87.12% | 88.81% | 86.89% | 99.44% |
| 阴性预测值 | 44.44% | 61.81% | 56.36% | 60.78% | 90.90% |
存活组的MELD、MELD-Na、IMELD、UKELD与MALF评分均 低于死亡组,均有统计学差异(P<0.05)。 MALF模型的AUROC值为0.952(95%CI 0.907~0.997),准确度为95.29%,均高于MELD 0.783(95%CI 0.720~0.845)、MELD-Na 0.825(95%CI 0.762~0.887)、IMELD 0.793(95%CI 0.726~ 0.860)、UKELD 0.841(95%CI 0.781~0.901)。MELD、MELD-Na、 IMELD、UKELD与MALF 5种预测模型AUC分析比较见表 4,新构建模型MALF与MELD、MELD-Na、IMELD、UKELD比较均具有统计学差异(P<0.001),故可以得出新建回归模型对ALF患者3个月死亡危险性评估准确性优于上述4种评分,但除了MELD 与MELD-Na(P=0.027)评分比较有显著差异外,其余均无统计学差异。虽然5个评分体系AUC 值均小于0.9,但>0.7,故认为在ALF患者3个月死亡危险性评估方面均具有一定的临床应用价值,其中新建模型应用价值最高。
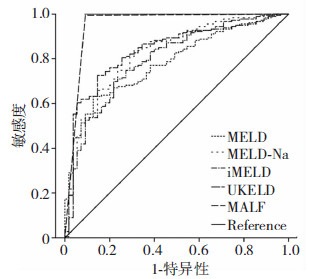 |
| 图 1 5种评分评估ALF短期预后的ROC曲线分析 |
| 评分 | MELD | MELD-Na | IMELD | UKELD | MALF | |||||
| Z值 | P值 | Z值 | P值 | Z值 | P值 | Z值 | P值 | Z值 | P值 | |
| MELD | 2.213 | 0.027 | 1.135 | 0.257 | 1.595 | 0.111 | 7.231 | <0.001 | ||
| MELD-Na | 1.093 | 0.274 | 0.598 | 0.550 | 5.417 | <0.001 | ||||
| IMELD | 0.563 | 0.573 | 6.545 | <0.001 | ||||||
| UKELD | 6.530 | <0.001 | ||||||||
ALF起病急,病情危重,进展迅速,死亡率极高[8]。因此,通过早期的临床生化指标及表现,在此基础上建立评估患者短期预后风险模型,及时有效的选择最佳治疗方案,对降低患者死亡率显得尤为重要[8]。自Pugh等[9]创建 Child-Pugh 评分以来,近年来已有MELD等多种评分系统用于预测肝衰竭患者的预后[3],且已有多篇研究证实了MELD 评分是预测肝衰竭预后的良好模型[10, 11]。随后Biggins等[4]在MELD评分基础上,考虑到肝储备功能受年龄及血清钠影响,建立了MELD-Na、IMELD评分,Barber等[6]也在此基础上建立了UKELD 模型。为了评价上述4种评分模型对我国ALF患者短期预后的评估能力,本研究使用了ROC 曲线以及AUC对以上4种评分系统对我国ALF患者短期预后的诊断价值进行分析,最后利用Logistic多因素回归构建了预测我国ALF患者3个月死亡危险性的新模型。
在本研究中,MELD评分在评估患者预后的AUROC为0.783,低于文献[12]报道的0.823。MELD-Na、IMELD评分用于终末期肝病预后评估后,证实其评估效果优于MELD评分[13, 14],从本研究得出,MELD-Na评分评估预后的AUC为0.825,明显高于MELD评分,且两者之间存在统计学差异(P=0.027),故认为MELD-Na评分预测我国ALF患者短期死亡危险性能力大于MELD评分,也说明血清钠的纳入,明显提高了评分预测准确性。IMELD评分评估预后的AUROC为0.793,稍高于MELD评分,无统计学差异(P=0.257)。UKELD 评分的ROC为0.841,虽均高于MELD、MELD-Na、IMELD评分,但均无统计学差异(P=0.111,0.550,0.573)。虽然4个评分体系AUC值均<0.9,但>0.7,故认为在在评估我国ALF患者3个月死亡危险性方面具有一定的临床应用价值。
但笔者认为MELD、MELD-Na、IMELD与UKELD等模型都是基于欧美终末期肝病与肝衰竭患者的临床资料分析结果而建立的。然而,与欧美国家主要以对乙酰氨基酚中毒和酒精所致急性肝衰竭不同,我国主要是以病毒性肝炎(45.72%)为主,尤为HBV感染(33.76%)为主,不明原因(25.12%)与抗结核药物(23.50%)所致ALF占一定的比例,因此上述4种模型并不能很好适用于我国急性肝衰竭患者的短期预后评估。且MELD-Na、IMELD与UKELD模型也仅仅是在原MELD评分基础上进行的局部修改,亦存在许多不足,比如其评价因素中仍没有纳入ALF病程中常见的并发症,例如肝性脑病、腹水、细菌或真菌感染、消化道出血、急性肾功能不全等,而上述并发症的出现并相互关联影响,都会加剧ALF患者病情恶化及缩短其生存时间,增加死亡风险[15]。故在临床应用上仍存在一定的局限性。因此为建立适用于我国ALF患者的短期预后评估模型,本研究选取了18个可能与ALF短期预后有关的重要临床指标并记录了入院时或入院后达到ALF诊断标准时出现并发症(腹水、消化道出血、肝性脑病、细菌或真菌感染、急性肾功能不全)等情况。统计方法应用了多因素Logistic 回归分析逐步排除了各指标之间的相关性,通过5个步骤逐渐提高模型判断准确率,筛选出了与ALF短期预后最具有相关性的5个独立预测因素。在单因素分析结果中,入院达到ALF诊断时的总胆红素、国际标准化比率、白蛋白、白细胞、血小板、血清钠、血清肌酐、肝性脑病、腹水、细菌或真菌感染以及急性肾功能不全11项指标与预后具有相关性( P<0.05),这与多数研究报道结果一致[16];在随后纳入的多因素分析中只有国际标准化比率、总胆红素、血清钠、腹水以及感染5个因素与预后有显著的统计学意义(P<0.05)。
急性肝功能衰竭时,肝脏对毒素、毒物的代谢能力明显减退,凝血功能障碍,免疫功能降低,容易合并众多并发症,而且相互关联。如腹水及真菌、细菌感染,是导致患者最终全身多脏器功能衰竭死亡的直接原因[17]。故本研究在多因素回归分析中首次将并发症腹水与感染筛选纳入了模型中,作为ALF短期死亡危险性判定的新指标。已有众多研究证明国际标准化比率、总胆红素及血清钠是独立性预测ALF患者预后的因素[4, 6]。本研究亦证明了这一观点,筛选出的5个独立性预测变量分别是达到ALF诊断标准时的总胆红素(OR 1.077,95%CI 1.028~1.130,P=0.002),国际标准化比率(OR 2.555,95%CI 1.561~4.182,P=0.000),血钠(OR 0.938,95%CI 0.883~0.996,P=0.037),腹水(OR 2.804,95%CI 1.140~6.892,P=0.025),感染(OR 5.348,95%CI 2.268~12.610,P=0.000)。从优势比来看,我们得出结论,血清Na+为ALF预后相关保护性因素,Na+指标值越高,危险性将会降低,而TB、INR、腹水及感染为相关危险性因素,TB、INR指标值及发生腹水与感染并发症概率越高,ALF患者死亡危险性将会升高。并且得出了计算评估ALF患者3个月死亡危险性模型:P=1/[1+exp(-y)],y=4.448+0.074×TB+0.938×INR-0.064×Na++1.031×腹水+1.677×感染;其中P值为患者预后的死亡概率,腹水与感染取值为0或1;此 回归模型AUROC值为0.952(95%CI 0.907~0.997),准确度为95.29%,均高于MELD、MELD-Na、IMELD、UKELD评分,且具有统计学差异(P<0.001)。故与国外4种模型相比,新建模型将并发症感染与腹水纳入了模型,提高了预后的准确率,其评估我国ALF患者3个月死亡危险性能力最佳,在临床上有较好预测价值。
然而,本研究仍存在诸多不足,首先,相对国外急性肝衰竭模型研究而言,样本量较少,原因之一是我国大部分急性肝衰竭患者经济条件较差,无法及时就医诊治,病情进展迅速,入院时已到了肝衰竭晚期,失去了治疗机会,故完整的急性肝衰竭病例较难收集,近10余年来,我们只收集到了234例具有完整资料的病例。再者,观察的临床指标仍需进一步增加,比如血氨水平、发病至肝性脑病发生的时间、乳酸脱氢酶等,有研究证明血氨水平是预测ALF短期预后的独立性因素[15]。且各临床指标及并发症的出现是动态变化的,不应取一个时间点决定性的预测短期预后。最后,关键有效的治疗措施的采取,如及时抗病毒治疗及早期联合应用糖皮质激素[18],与病情的进展及预后有密切关系,故本研究存在一定局限性。总之,目前对于我国急性肝衰竭患者短期预后风险预测方向研究尚少,已有的预后模型在临床上是否有较高的预测效能,有待进一步验证。
| [1] | Kantola T, Ilmakunnas M, Koivusalo A M, et al. Bridging therapies and liver transplantation in acute liver failure, 10 years of MARS experience from Finland[J]. Scand J Surg, 2011, 100(1): 8-13. |
| [2] | Canbay A, Tacke F, Hadem J, et al. Acute liver failure: a life-threatening disease[J]. Dtsch Arztebl Int, 2011, 108(42): 714-720. |
| [3] | Mayo M J, Parkes J, Adams-Huet B, et al. Prediction of clinical outcomes in primary biliary cirrhosis by serum enhanced liver fibrosis assay[J]. Hepatology, 2008, 48(5): 1549-1557. |
| [4] | Biggins S W, Kim W R, Terrault N A, et al. Evidence-based incorporation of serum sodium concentration into MELD[J]. Gastroenterology, 2006, 130(6): 1652-1660. |
| [5] | Kim W R, Biggins S W, Kremers W K, et al. Hyponatremia and mortality among patients on the liver-transplant waiting list[J]. N Engl J Med, 2008, 359(10): 1018-1026. |
| [6] | Barber K, Madden S, Allen J, et al. Elective liver transplant list mortality: development of a United Kingdom end-stage liver disease score[J]. Transplantation, 2011, 92(4): 469-476. |
| [7] | 中华医学会感染病学分会肝衰竭与人工肝学组, 中华医学会肝病学分会重型肝病与人工肝学组. 肝衰竭诊治指南(2012年版)[J]. 中华临床感染病杂志, 2012, 5(6): 321-327. |
| [8] | Bernal W, Auzinger G, Dhawan A, et al. Acute liver failure[J]. Lancet, 2010, 376(9736): 190-201. |
| [9] | Pugh R N, Murray-Lyon I M, Dawson J L, et al. Transection of the oesophagus for bleeding oesophageal varices[J]. Br J Surg, 1973, 60(8): 646-649. |
| [10] | Zaman M B, Hoti E, Qasim A, et al. MELD score as a prognostic model for listing acute liver failure patients for liver transplantation[J]. Transplant Proc, 2006, 38(7): 2097-2098. |
| [11] | Garg H, Kumar A, Garg V, et al. Clinical profile and predictors of mortality in patients of acute-on-chronic liver failure[J]. Dig Liver Dis, 2012, 44(2): 166-171. |
| [12] | Hsu C Y, Lin H C, Huang Y H, et al. Comparison of the model for end-stage liver disease (MELD), MELD-Na and MELDNa for outcome prediction in patients with acute decompensated hepatitis[J]. Dig Liver Dis, 2010, 42(2): 137-142. |
| [13] | Kim W R, Biggins S W, Kremers W K, et al. Hyponatremia and mortality among patients on the liver-transplant waiting list[J]. N Engl J Med, 2008, 359(10): 1018-1026. |
| [14] | Guy J, Somsouk M, Shiboski S, et al. New model for end stage liver disease improves prognostic capability after transjugular intrahepatic portosystemic shunt[J]. Clin Gastroenterol Hepatol, 2009, 7(11): 1236-1240. |
| [15] | 金坤, 李磊, 李宜, 等. MELD 相关评分系统对肝衰竭患者生存情况的评估价值[J]. 安徽医学, 2012, 33(11): 1439-1441. |
| [16] | Zhao P, Wang C, Liu W, et al. Causes and outcomes of acute liver failure in China[J]. PLoS One, 2013, 8(11): e80991. |
| [17] | Witkowski J A, Parish L C. The great imitator: malignant syphilis with hepatitis[J]. Clin Dermatol, 2002, 20(2): 156-163. |
| [18] | Zhang X Q, Jiang L, You J P, et al. Efficacy of short-term dexamethasone therapy in acute-on-chronic pre-liver failure[J]. Hepatol Res, 2011, 41(1): 46-53. |



