前列腺癌是泌尿系常见的恶性肿瘤之一,在欧美国家和地区发病率居首位,死亡率居第2位[1];在我国,虽发病率低于西方等国家,但近年来逐渐升高。前列腺癌目前的治疗多为多模式综合治疗,包括手术切除、放疗、内分泌治疗等,由于雄激素抵抗,手术及放疗对于晚期前列腺癌患者疗效不显著。前列腺癌易复发、侵袭和转移,因此积极寻求前列腺癌相关肿瘤标志物成为前列腺癌早期检测、靶向治疗和预防复发的关键[2]。精子相关抗原9(SPAG9),是癌睾丸抗原(CTA)家族成员之一,在睾丸组织中特异性表达[3]。目前主要观点认为,SPAG9主要是作为支架蛋白,辅助活化JNK信号通路,从而促进肿瘤的增殖、侵袭及转移,抑制肿瘤凋亡等。JNK信号通路的活化对于肿瘤的促进均有报道[4]。由此推测,在肿瘤中,SPAG9表达上调,可改变原有的基因调节模式,促进肿瘤的增殖、侵袭及转移等。本研究主要探讨SPAG9对前列腺癌细胞PC3侵袭、增殖及生长等生物学行为的影响。 1 材料与方法 1.1 细胞及主要试剂
人前列腺癌细胞PC3为本实验室保存,血清(Gibco,美国),DMEM培养基(Sigma,美国),兔抗人单克隆SPAG9抗体、兔抗人多克隆磷酸化ERK抗体、兔抗人多克隆ERK抗体、兔抗人多克隆磷酸化JNK抗体、兔抗人多克隆JNK抗体(CST,美国),鼠抗人单克隆GAPDH抗体、总蛋白提取试剂盒(北京中杉金桥生物技术有限公司)。TRIzol、逆转录试剂盒、RT-PCR试剂盒(TaKaRa,中国大连),SDS PAGE胶试剂盒(碧云天,中国上海)。转染试剂X-tremeGENE HP DNA Transfection Reagent(Roche,美国),M29真核表达载体及M29-SPAG9真核质粒由广州复能基因有限公司提供,SPAG9序列来源于NCBI网站(ID: 9043)。 1.2 细胞培养及病毒转染
人前列腺癌细胞PC3培养于10%的完全培养基,放在5% CO2、37 ℃孵箱培养,每3天更换培养基,当细胞长至90%融合时进行传代培养。按照5×105接种于6孔培养板,生长至90%融合时,分别以M29-SPAG9与M29转染PC3细胞(质粒均带有绿色荧光及抗性)。转染48 h后,加入G418(300 mg/mL)筛选并建立稳定转染细胞系,荧光显微镜下观察转染效果,PCR及Western blot检测转染效果。 1.3 qRT-PCR检测
用TRIzol提取细胞总RNA,以其为模板,逆转录cDNA,条件是42 ℃,2 min,37 ℃ 15 min,85 ℃ 5 s,按照qRT-PCR试剂盒(DRR037A)SYBR Green法步骤进行PCR扩增,qRT-PCR扩增程序:95 ℃预变性3 min,95 ℃变性10 s,60 ℃退火45 s,以GAPDH作为内参,扩增40个循环周期,每个标本3个复孔。人SPAG9引物序列为5′-AGTCATCAGCCCACAAAGTAGCAG-3′,5′-GATTCTCCACCTTCATCACCCATT-3′,扩增目的片段大小为173 bp。 1.4 Western blot检测
用蛋白裂解液提取细胞总蛋白,RCDC法检测蛋白浓度,经5%的浓缩胶和6%的分离胶SDS-PAGE电泳,每孔上样量为80 μg总蛋白。浓缩胶60 V电泳1 h,分离胶100 V电泳1 h,常规湿法转膜120 min,5%的BSA封闭1 h,免疫抗体反应 (稀释比例,一抗 SPAG9 1 ∶1 000,GAPDH 1 ∶500; 二抗:山羊抗鼠1 ∶5 000,山羊抗兔1 ∶5 000)。ECL化学发光,凝胶成像系统显影。 1.5 CCK-8法检测细胞增殖
取处于对数生长期的转染M29-SPAG9和对照组M29细胞消化成单细胞悬液,分别按照4 000个/孔接种于96孔板,每孔加入100 μL完全培养基,设置6个复孔。分别于0、24、48 h加入CCK-8检测试剂,每孔加入10 μL,再次置于孵箱培养2 h检测,于酶标仪上检测450 nm处各孔光密度值[D(450)]。 1.6 流式细胞术检测细胞周期
取处于对数生长期的转染M29-SPAG9和对照组M29细胞消化成单细胞悬液,分别按照5×105接种于6孔培养板,生长至90%融合时,消化成单细胞悬液,胰酶消化,收集各组细胞,预冷PBS清洗2~3次,重悬细胞于EP管中,于流式细胞仪上检测细胞周期情况。按细胞周期检测试剂盒说明进行操作,使用碧云天PI染色试剂盒操作说明。 1.7 Transwell体外迁移实验
PC3细胞接种至24孔板中并分别转染M29和SPAG9,每组设3个复孔。转染24 h后将细胞温和消
化下来,计数并接种至Transwell小室上室(约细胞1×105/孔),上室为无血清培养基,下室为含10%胎牛血清的培养基。培养24 h后弃掉培养基并用PBS清洗,4%多聚甲醛固定20 min,再用PBS清洗3遍,0.1%结晶紫染色15 min,棉签轻轻刮掉小室上室内的细胞,显微镜下随机选取10个视野倒置显微镜下观察并计数。
1.8 统计学处理
采用SPSS 13.0统计软件,计量数据以 x±s表示,两组间比较采用t检验或非参数秩和检验,两配对样本之间采用配对t检验。 2 结果 2.1 过表达SPAG9人PC3前列腺癌细胞的建立和鉴定
用M29-SPAG9(实验组)及空质粒M29(对照组)转染前列腺癌PC3细胞,48h后分别通过qRT-PCR和Western blot 来检测细胞中SPAG9的mRNA及蛋白水平的变化,结果显示,转染M29-SPAG9组与转染M29组比较,SPAG9表达量显著增高,mRNA表达量实验组(20.776 3±3.080 9),对照组(1.010 2±0.178 4),蛋白水平见图 1。证实SPAG9转染前列腺癌细胞PC3构建成功。
 |
| 1: M29组;2: M29-SPAG9组图 1 转染SPAG9对前列腺癌PC3细胞株中SPAG9蛋白 水平的影响 |
采用CCK-8法测定稳定转染前列腺癌细胞PC3的D(450),M29-SPAG9组CCK-8光密度值明显高于M29组(P<0.05,图 2),说明过表达SPAG9后促进前列腺癌细胞PC3的增殖。
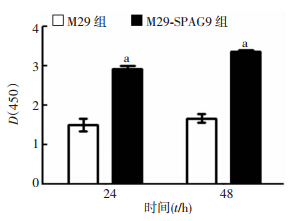 |
| a:P<0.05,与M29组比较图 2 过表达SPAG9对前列腺癌PC3细胞生长的影响 |
采用流式细胞术检测稳定转染后PC3的周期比值,转染M29-SPAG9后,与对照组相比,G2/S期的细胞比例增加,而G0/G1期的细胞比例减少(图 3),差异具有统计学意义(P<0.05),说明过表达SPAG9后促进前列腺癌细胞PC3的细胞周期。
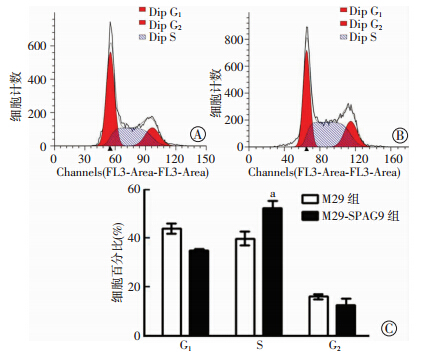 |
| A:M29组流式细胞术检测结果;B:M29-SPAG9组流式细胞术检测结果;C:两组细胞周期分布 a:P<0.05 ,与M29组比较 图 3 过表达SPAG9对PC3细胞周期的影响 |
用M29-SPAG9及M29质粒分别转染PC3细胞24 h 后,收集细胞采用Transwell检测PC3细胞穿膜能力。SPAG9组穿膜细胞数为(88.078±4.509)/视野,对照组穿膜细胞数为(54.333±4.582)/视野,SPAG9组细胞转移能力明显高于对照组(P<0.05),说明过表达SPAG9可明显促进前列腺癌细胞PC3的迁移能力(图 4)。
 |
| A: M29组;B: M29-SPAG9组 图 4 过表达SPAG9对PC3细胞迁移能力的影响 (结晶紫 ×200) |
Western blot检测结果显示,转染M29-SPAG9对磷酸化的ERK、JNK都有活化,而总的ERK和JNK没有变化(图 5),说明转染SPAG9活化了ERK和JNK信号通路,并通过此促进细胞的增殖和细胞周期。
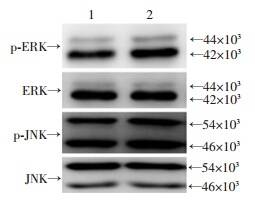 |
| 1: M29组;2: M29-SPAG9组 图 5 过表达SPAG9活化了ERK和JNK信号通路 |
研究证实,SPAG9在不同的肿瘤中均有增高,且促进肿瘤的侵袭、转移及增殖等生物学行为,如肾癌、肺癌、宫颈癌、乳腺癌、甲状腺癌、直肠癌等[5, 6, 7, 8, 9, 10]。近年,国外学者发现SPAG9不仅在肿瘤组织表达的阳性率超过80%(蛋白水平和RNA水平),而且该抗原免疫原性强,能引起肿瘤患者较强的体液免疫反应,产生相应抗体[11]。SPAG9抗体在卵巢上皮癌患者血清中的阳性检出率为67% ,并在活体内各种组织类型的早期阶段(Ⅰ~Ⅱ期)表现出高的抗SPAG9免疫活性,而健康人血清中完全没有。
Li等[12]报道,在前列腺癌148对标本中,免疫组化证实SPAG9阳性表达的占54例,阳性率36.5%,且SPAG9的表达与前列腺癌的分期分级密切相关。SPAG9在前列腺癌中的表达越高,前列腺癌恶性程度高,患者预后越差,这一现象提示我们SPAG9的表达与其侵袭、转移密切相关。因此,本研究采用在前列腺癌中相对SPAG9表达较低的PC3细胞,过表达SPAG9后,细胞穿膜数明显增加,其侵袭能力明显增强。这一想象表明,SPAG9促进前列腺癌的侵袭转移,加快其发生、发展。
既往研究[5, 6, 7, 8, 9, 10]表明,在肾癌、结肠癌、宫颈癌及肺癌中,干扰SPAG9后,细胞增殖减慢。在本实验中,过表达SPAG9后,PC3细胞增殖加快。此外,膀胱癌相关研究[13]表明,过表达SPAG9后,cyclin D1、B和E表达上调,细胞周期加快,提示过表达SPAG9可促进恶性肿瘤细胞的生长,且这一过程主要是通过调节周期相关蛋白来实现的。而cyclin D1在多种癌中表达上调,其作用主要使细胞从G1期进入G2/S期,从而加快细胞周期。本研究中,过表达SPAG9后,G2/S期细胞比例明显增加,说明在前列腺癌中,SPAG9通过对细胞周期的调控作用,促进其增殖和生长。
但是SPAG9如何促进了前列腺癌细胞的侵袭转移,目前仍不清楚。众所周知,MAPK信号通路与细胞生长的关系最为密切,参与调节细胞的增殖、分化和凋亡等多种进程[14]。文献[15]报道,通过氨基端序列分析发现,SPAG9与JNK相互作用蛋白具有结构同源性,通过N端JNK结合域与JNK结合而在MAPK信号通路发挥作用,也就是说,SPAG9在MAKP信号通路中正是作为 一种支架蛋白来起作用,参与人体多种生理功能[16]。那么在前列腺癌中,是否也是如此?本研究证实,PC3过表达SPAG9后,JNK及ERK信号通路明显活化。而这一实验结果说明SPAG9是通过JNK及ERK信号通路发挥促进肿瘤侵袭转移、增殖的作用。
本研究证实SPAG9不仅促进了前列腺癌侵袭转移及增殖,加快细胞周期,且发挥这一作用主要是通过JNK及ERK信号通路来实现的。因此,在前列腺癌中,SPAG9可能作为一个潜在的肿瘤标志物,有利于肿瘤早期的诊断及治疗,尚需进一步动物实验及临床标本证实 。
| [1] | Shaikhibrahim Z, Lindstrot A, Ochsenfahrt J, et al. Epigenetics-related genes in prostate cancer: expression profile in prostate cancer tissues, androgen-sensitive and -insensitive cell lines[J]. Int J Mol Med, 2013, 31(1): 21-25. |
| [2] | Thompson I M, Ankerst D P, Chi C, et al. Assessing prostate cancer risk: results from the Prostate Cancer Prevention Trial[J]. J Natl Cancer Inst, 2006, 98(8): 529-534. |
| [3] | Shankar S, Mohapatra B, Suri A. Cloning of a novel human testis mRNA specifically expressed in testicular haploid germ cells, having unique palindromic sequences and encoding a leucine zipper dimerization motif[J]. Biochem Biophys Res Commun, 1998, 243(2): 561-565. |
| [4] | Jagadish N, Rana R, Selvi R, et al. Characterization of a novel human sperm-associated antigen 9 (SPAG9) having structural homology with c-Jun N-terminal kinase-interacting protein[J]. Biochem J, 2005, 389(Pt 1): 73-82. |
| [5] | Garg M, Kanojia D, Khosla A, et al. Sperm-associated antigen 9 is associated with tumor growth, migration, and invasion in renal cell carcinoma[J]. Cancer Res, 2008, 68(20): 8240-8248. |
| [6] | Wang Y, Dong Q, Miao Y, et al. Clinical significance and biological roles of SPAG9 overexpression in non-small cell lung cancer[J]. Lung Cancer, 2013, 81(2): 266-272. |
| [7] | Garg M, Kanojia D, Suri S, et al. Small interfering RNA-mediated down-regulation of SPAG9 inhibits cervical tumor growth[J]. Cancer, 2009, 115(24): 5688-5699. |
| [8] | Sinha A, Agarwal S, Parashar D, et al. Down regulation of SPAG9 reduces growth and invasive potential of triple-negative breast cancer cells: possible implications in targeted therapy[J]. J Exp Clin Cancer Res, 2013, 32: 69. |
| [9] | Garg M, Kanojia D, Suri S, et al. Sperm-associated antigen 9: a novel diagnostic marker for thyroid cancer[J]. J Clin Endocrinol Metab, 2009, 94(11): 4613-4618. |
| [10] | Kanojia D, Garg M, Saini S, et al. Sperm associated antigen 9 expression and humoral response in chronic myeloid leukemia[J]. Leuk Res, 2010, 34(7): 858-863. |
| [11] | Garg M, Chaurasiya D, Rana R, et al. Sperm-associated antigen 9, a novel cancer testis antigen, is a potential targe |
| [12] | Li H, Peng Y, Niu H, et al. SPAG9 is overexpressed in human prostate cancer and promotes cancer cell proliferation[J]. Tumour Biol, 2014, 35(7): 6949-6954. |
| [13] | Kanojia D, Garg M, Saini S, et al. Sperm associated antigen 9 plays an important role in bladder transitional cell carcinoma[J]. PLoS One, 2013, 8(12): e81348. |
| [14] | Ando K, Uemura K, Kuzuya A, et al. N-cadherin regulates p38 MAPK signaling via association with JNK-associated leucine zipper protein: implications for neurodegeneration in Alzheimer disease[J]. J Biol Chem, 2011, 286(9): 7619-7628. |
| [15] | Chen F, Lu Z, Deng J, et al. SPAG9 expression is increased in human prostate cancer and promotes cell motility, invasion and angiogenesis in vitro[J]. Oncol Rep, 2014, 32(6): 2533-2540. |
| [16] | Andreeva A V, Kutuzov M A, Voyno-Yasenetskaya T A. Scaffolding proteins in G-protein signaling[J]. J Mol Signal, 2007, 2: 13. |



