2.400042 重庆,第三军医大学大坪医院野战外科研究所呼吸内科
活细胞工作站是研究者观察活细胞各种生命现象的重要工具,在利用活细胞工作站动态观察电活细胞生物学行为时,观察视野常常存在非动力性偏移,这对我们判断细胞生物学行为的变化产生较大的影响。但是,视野的偏移是一个长期存在的问题,是一种存在于显微镜镜头和样本之间的物理漂移。可能由系统本身的不稳定性或温度变化引起。在成像过程中,各种系统均不可能处于绝对恒温状态,故均不可避免的出现视野的偏移[1,2],如何解决这个问题显得十分关键。目前,各研究机构和实验室也采用了很多方法来矫正视野偏移。Lee等[3]采用人为添加标记点的方法矫正视野移动,但该方法操作复杂,且可能对细胞状态有影响。Husain等[4]开发了一个软件系统,并将其整合进入图像采集系统,控制偏移的产生。但该方法对于大部分实验室难以推广,技术要求高。Kim等[5]采用恒温材料制作培养体系,但造价昂贵,难以推广。另外,Carter等[2]也采用特殊的载物台减弱偏移。大部分的矫正方法都由于造价昂贵而难以推广,因此在目前硬件水平难有很大提升的情况下,找到一种简便可行的矫正方法很有必要。本研究采用不动点示踪结合数学矫正的方法,矫正由于视野移动造成的细胞运动速率和运动方向的偏差。具有无需提升固有的硬件和软件水平,简便、快速,只需做一次轨迹分析,即可利用数学公式进行矫正,且操作技术要求低的优点。
1 材料与方法 1.1 设备和软件采用的成像系统是由美国API公司生产的Deltavison活细胞工作站,它可使研究者了解细胞在正常生理生化条件下的各种状态变化,从而发现和确定细胞间相互作用、信号传导的过程,以及在外界条件干预下,细胞的迁移特性。细胞轨迹分析采用的软件为Bitplane公司提供的Iamris分析软件,通过对视野内细胞运动的追踪,软件会自动生成关于轨迹分析的各种数据,如:X/Y方向上的位移(Track displacement X/Y)、各个细胞在不同时间点的XY坐标(Position)、位移(Track displacement length)、轨迹长度(Track length)等。
1.2 图像采集的方法分离培养的大鼠表皮干细胞接种在10 cm塑料培养皿的趋电小室中,其中细胞接种面积大小为2 cm×5 cm。在电刺激的作用下,我们利用活细胞成像系统对细胞的运动能力及方向进行长时观察。我们共选择了10个视野的细胞进行追踪观察,每个视野约20个细胞。物镜放大倍数为20×(1pixel=0.794 2 μm),目镜为×10,我们设置每隔5 min对这10个视野采集1次图像,共观察2 h,程序运行完成后,我们共获得10个DV文件,每个DV文件对应1个视野24个时间点的图片。重复3次实验。
本研究采用200倍观察视野,因为在低倍下如果都能观察到明显漂移,那在高倍下的漂移现象就更明显,另外,在200倍下观察细胞大小合适,故选择200倍 进行观察。
1.3 轨迹追踪及细胞迁移分析方法单个的表皮干细胞的形态为近似椭圆形或多角形,故我们选取视野中形态近似椭圆的细胞进行轨迹追踪,使用软件为Bitplane公司的Imaris分析软件。各时间点追踪的中心为细胞核或不动点的形态中心。
视野中的不动点可以是培养皿底部的划痕、固定不动的杂质,也可以是电刺激系统盖玻片上的污渍。原则是固定在培养皿中不动,不会因为细胞的移动而移动,只会随着视野的移动而产生相同移动。对于不动点的形态、大小没有特殊要求。如果成像系统中不存在这样的不动点,我们也可以人为的用利器在培养皿底部加入这样的标记。
轨迹追踪得到的数据包括Track displacement X(Dx:起点到终点在X方向上的移动距离)、Track displacement Y(Dy:起点到终点在Y方向上的移动距离)、Track displacement length(Td:起点到终点的位移)、Track length(Tt:起点到终点的轨迹长度)、Positon(各个时间点的X/Y坐标)等。根据以上参数,我们得到4个用于评价细胞运动特征的指标,首先是反映在既定方向的定向迁移能力的指标:X轴迁移速率= Dx/t。其次是反映细胞定向迁移快慢的指标:位移速 率=Td/t。再次是反映细胞定向性的指标:cosθ=Dx/Td。 最后是反映细胞自身迁移能力的指标:迁移速度=Tt/t (图 1)。
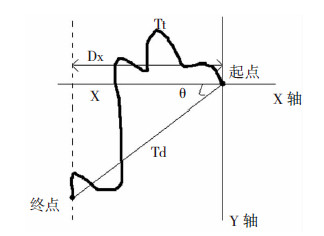 |
| 图 1 评价细胞运动特征的指标 |
利用Imaris的Track功能,在分析完成后,我们可以直接获得细胞及不动点在各时间点的原始坐标值。
1.4.2 获得不动点振幅将不动点的各时间点的 坐标值均减去第1个时间点的坐标值得到振幅,即:第n个时间点的振幅=Xn-X1。用相同的方法对视野中的3个不动点完成振幅计算,并计算出平均振幅,以此来矫正细胞的坐标。
1.4.3 获取目的细胞各时间点真实坐标值细胞各时间点的真实坐标值=细胞各时间点的原始坐标值-不同点各时间定的平均振幅。
1.4.4 利用真实坐标值进行系列计算获得X方向上的真实位移:Dx=Xn-X1(X:x方向的坐标值,n:终点,1:起点)。系统会自动把向右的Dx定义为正值,向左的Dx定义为负值。
获得Y方向上的真实位移:Dy=Yn-Y1(Y: y方向的坐标值,n:终点,1:起点)。
获得起点到终点的真实位移:总的位移2=X方向的位移2+Y方向的位移2,即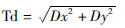
获得细胞运动的真实cosθ(图 2),Cosθ=Dx/Td。因为Dx是有正负的,运动方向与电场方向相同则为正,运动方向与电场方向相反则为负,故cosθ数值的正负可表示迁移方向。即0~1:运动与电场方向相反,向正极运动:-1~0:运动与电场方向相同,向负极运动。
 |
| 图 2 位移示意图 |
获得细胞运动的真实轨迹长度(Tt)。因为细胞运动轨迹和视野移动轨迹在方向上不重合,故不能直接相加减。但我们可以利用微积分的原理,将曲线轨迹分成N个小段(N为总的拍摄的时间点,如60个时间点就可分成60段),每条线段是一条直线,这样,我们再将小线段分解到X和Y方向上进行加减。
结合前期结论: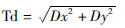 及Dx1,2=X2-X1,Dy1,2=Y2-Y1(Dx为细胞在相邻时间点之间X方向上的位移,Dy为细胞在相邻时间点之间Y方向上的位移),得到:Tt= Td1,2+Td2,3+……+Tdn-1,n(Tdn-1,n为相邻时间点之间的轨迹长度)(图 3)。
及Dx1,2=X2-X1,Dy1,2=Y2-Y1(Dx为细胞在相邻时间点之间X方向上的位移,Dy为细胞在相邻时间点之间Y方向上的位移),得到:Tt= Td1,2+Td2,3+……+Tdn-1,n(Tdn-1,n为相邻时间点之间的轨迹长度)(图 3)。
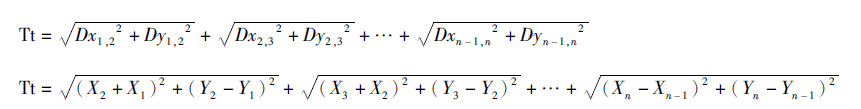
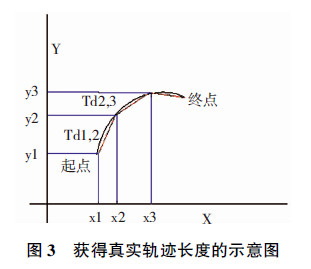 |
| 图 3 获得真实轨迹长度的示意图 |
所有数据利用SPSS 11.5软件进行配对t检验。
2 结果 2.1 不动点的确定及分析我们进行了3次重复实验,每次实验均选取3个不动点,利用Imaris软件分析发现,不动点的运动方向和位移在误差范围内均一致,说明视野中确实存在不动点,可用于视野移动的矫正(图 4)。
 |
| A~C:分别为3次重复实验(×200),红色箭头示选择的不动点;D~F:分别为3次重复实验的不动点在X和Y轴上的位移图 4 视野移动追踪的3次重复实验 |
我们对3次实验均进行2 h的观察,并利用不动点对3个重复的15个细胞进行了轨迹矫正。结果表明,不同批次的实验,其视野移动方向是不确定的,我们通过矫正成功的扣除了视野移动带来的影响(表 1,图 5~图 7)。
| 实验 次数 | 细胞 编号 | 校正前 X坐标 | 校正前 Y坐标 | 校正后 X坐标 | 校正后 Y坐标 |
| 1 | 1 | 139.42 | 274.16 | 150.27 | 272.71 |
| 2 | 156.27 | 287.72 | 167.12 | 286.28 | |
| 3 | 80.76 | 103.56 | 91.61 | 102.12 | |
| 4 | 172.94 | 196.86 | 183.79 | 195.42 | |
| 5 | 211.66 | 267.96 | 222.51 | 266.52 | |
| 2 | 1 | 303.99 | 226.62 | 306.81 | 225.99 |
| 2 | 305.84 | 190.87 | 308.66 | 190.24 | |
| 3 | 258.41 | 294.37 | 261.23 | 293.74 | |
| 4 | 277.21 | 198.25 | 280.03 | 197.62 | |
| 5 | 301.84 | 265.51 | 304.66 | 264.88 | |
| 3 | 1 | 184.93 | 232.55 | 187.62 | 236.34 |
| 2 | 14.60 | 129.33 | 17.30 | 133.12 | |
| 3 | 91.61 | 317.10 | 94.31 | 320.89 | |
| 4 | 217.13 | 134.44 | 219.82 | 138.24 | |
| 5 | 200.04 | 104.66 | 202.73 | 108.45 |
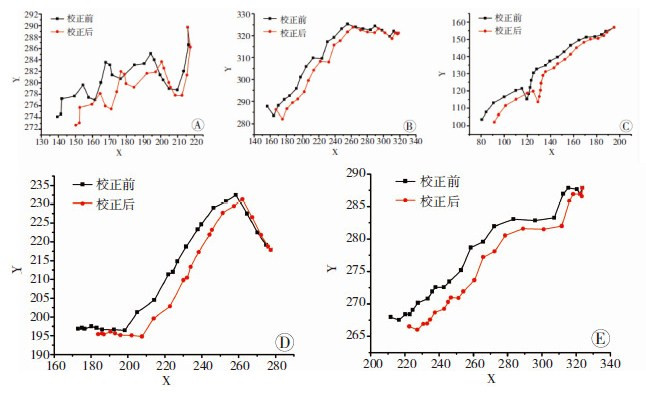 |
| A~E:随机选取的5个表皮干细胞图 5 第1次实验5个细胞矫正前后轨迹 |
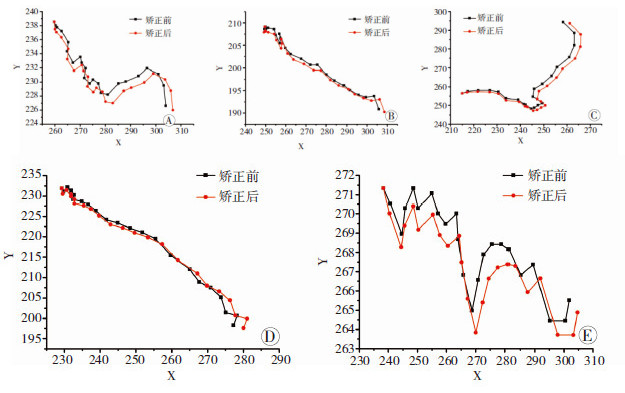 |
| A~E:随机选取的5个表皮干细胞图 6 第2次实验5个细胞矫正前后轨迹 |
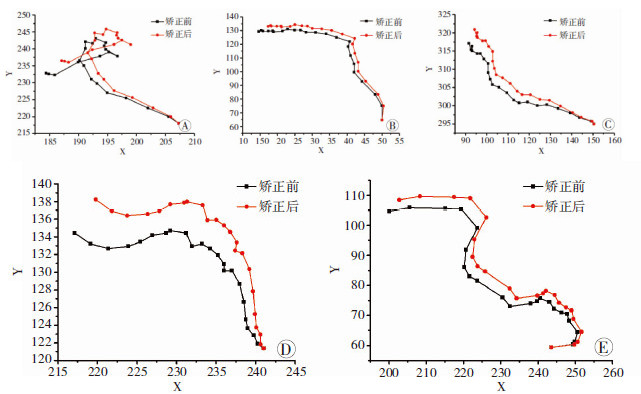 |
| A~E:随机选取的5个表皮干细胞图 7 第3次实验5个细胞矫正前后轨迹 |
迁移方向(cosθ)是反映细胞对外界刺激的关键性指标,从图 8~图 10可以看出,细胞运动的初期视野移动对运动方向的判断影响非常大,对15个细胞矫正前后的cosθ值进行配对t检验(P < 0.01),说明视野移动可对细胞迁移方向产生显著性影响。
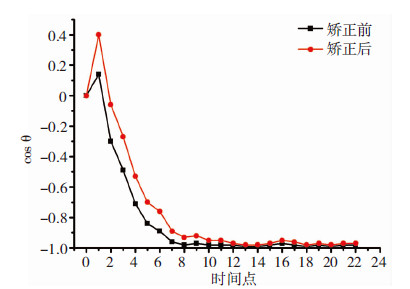 |
| 图 8 第1次实验第2个细胞矫正前后cosθ值比较 |
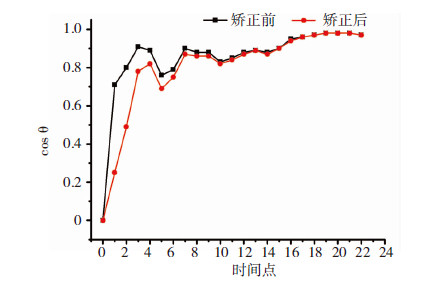 |
| 图 9 第2次实验第1个细胞矫正前后cosθ值比较 |
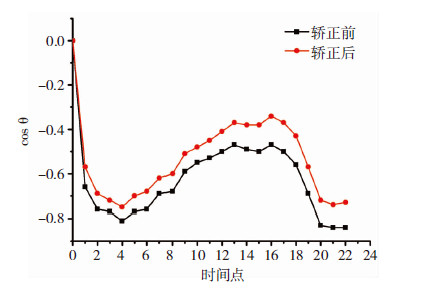 |
| 图 10 第3次实验第1个细胞矫正前后cosθ值比较 |
表皮干细胞定向迁移至创伤处进行创面修复是皮肤创面修复的重要机制,电刺激指导细胞定向迁移的重要作用可能是加速皮肤创面愈合的重要手段[1,6,7,8]。在体外观察电刺激指导表皮干细胞的迁移行为为揭示表皮干细胞参与创面修复的机制提供了重要证据。系统的视野移动对表皮干细胞在电场作用下的定向性判断产生显著干扰,特别是在运动初期,对细胞运动方向的判断会产生质的影响。并且,对于那种处于左右临界处的细胞,如果细胞感应刺激后应有向左的运动方向,但由于视野移动是向右的,则有可能我们得出的数据是细胞向右运动,造成实验结果的错误。本研究采用了不动点示踪结合数学矫正的方法去矫正视野移动产生的影响,从而纠正了对细胞运动方向的错误判断,提供了科学的数据,为我们进一步研究细胞的运动机制奠定了正确基础。虽然去除平台漂移是活细胞工作站应该具备的功能。但我们在研究中发现,其自带的纠正功能并不能完全实现“零漂移”,即从硬件水平上不能解决平台漂移的问题,这就需要对软件进行升级,或者自行纠正。然而升级软件成本高、耗时长,且效果并不明确。而我们提出的方法经济、实用,快速,很简便地解决了这个问题,因此具有一定的创新性。
综上所述,基于定点标记的数学模拟矫正是有效克服活细胞动态示踪非动力性细胞漂移的重要方法,是精确观察活细胞生命现象,揭示生物世界动态归路的重要技术路径。
| [1] | Li L, Gu W, Du J, et al. Electric fields guide migration of epidermal stem cells and promote skin wound healing[J]. Wound Rep Reg, 2012, 20(6): 840-851. |
| [2] | Carter A R, King G M, Ulrich T, et al. Stabilization of an optical microscope to 0.1 nm in three dimensions[J]. Appl Opt, 2007, 46(3): 421-427. |
| [3] | Lee S H, Baday M, Tjioe M, et al. Using fixed fiduciary markers for stage drift correction[J]. Opt Express, 2012, 20(11): 12177-12183. |
| [4] | Husain M, Boudier T, Paul-Gilloteaux P, et al. Software for drift compensation, particle tracking and particle analysis of high-speed atomic force microscopy image series[J]. J Mol Recognit, 2012, 25(5): 292-298. |
| [5] | Kim J, Shen M, Nioradze N, et al. Stabilizing nanometer scale tip-to-substrate gaps in scanning electrochemical microscopy using an isothermal chamber for thermal drift suppression[J]. Anal Chem, 2012, 84(8): 3489-3492. |
| [6] | Reid B, Vieira A C, Cao L, et al. Specific ion fluxes generate cornea wound electric currents[J]. Commun Integr Biol, 2011, 4(4): 462-465. |
| [7] | Zhao M. Electrical fields in wound healing-an overriding signal that directs cell migration[J]. Semin Cell Dev Biol, 2009, 20(6): 674-682. |
| [8] | Zhao M, Song B, Pu J, et al. Electrical signals control wound healing through phosphatidylinositol-3-OH kinase-gamma and PTEN[J]. Nature, 2006, 442(7101): 457-460. |



