400042重庆,第三军医大学大坪医院野战外科研究所:2放射科
2Department of Radiology,Institute of Surgery Research,Daping Hospital,Third Military Medical University,Chongqing,400042,China
慢性前列腺炎/慢性盆底疼痛综合征(CP/CPPS)在男性患者中有极高的发病率,早期研究指出该病在男性群体中的发病率达8.5%~56.5%[1]。而近期国内研究发现其在部分地区男性群体中的发病率达到了7.06%~8.37%,并且有5%左右的患者症状持续长达3个月以上[2]。同时在无症状人群中也发现有炎症证据的前列腺占据了比例高达21.1%,而这部分人群极有可能在发展为有症状的前列腺炎[3]。慢性前列腺炎病因并不明确,治疗效果不佳,对患者生活质量影响较大,对医师和患者都造成了极大的困扰。美国国立卫生研究院(National Institute of Health,NIH)定义的前列腺炎分类中,Ⅲb型前列腺炎为非炎症性慢性前列腺炎(CPⅢb),Ⅳ型前列腺炎为无症状性前列腺炎。其两者间的悖论就在于CP Ⅲb患者有尿频、尿急、会阴和盆底疼痛等下尿路症状,故又称之慢性盆底疼痛综合征,实验室检查却缺乏炎症证据;而Ⅳ型前列腺炎则恰恰相反,前列腺检查能够找到炎症证据,患者却无临床症状[4]。这使得临床上对前列腺炎的内涵和发生机制提出质疑。前列腺炎是否真的有“炎”而发生?CPⅢb的发病是否还有其他原因?我们在对慢性前列腺炎的系列研究中发现,CPⅢb患者常合并 有耻骨直肠肌痉挛,而且和患者临床症状之间存在着直接联系。本研究旨在探讨针对耻骨直肠肌痉挛的治疗效果,并探讨耻骨直肠肌痉挛在CPⅢb发生中的作用。
1 材料与方法 1.1 患者资料与分组我院泌尿外科2012年9月至2013年9月期间于门诊因尿频、尿急、夜尿增多以及盆底、会阴部疼痛等就诊的患者335例,经检查确诊为CPⅢb、排粪造影诊断有耻骨直肠肌痉挛的患者44例。年龄21~43(27.3±5.2)岁。患者填写IPSS和QoL评分表,并将其分为A、B 2组。A组患者给予α-受体阻断剂盐酸坦索罗辛(日本安斯泰来制药)0.2 mg,每日1次口服;B组患者在此基础上联合使用Cox-2抑制剂塞来昔布(美国辉瑞制药)200 mg,每日2次口服。治疗开始后2、4、6周随访,填写IPSS和QoL评分表,完成随访的患者有40例。
1.2 疗效评价所有患者的症状及治疗效果按照国际通用的IPSS评分进行评价,分析比较治疗前和治疗2、4、6周的病情变化,并参照文献设计的评价策略和标准对2组患者的尿频、尿急、疼痛和QoL进行定量评估,以更明确、直观地判定疗效。评价标准:以患者就诊时的(治疗前)症状计分为“0”,治疗开始后不同时间随访,症状好转为“+”,症状加重为“-”。好转与加重的程度依据“稍有改善”“改善”“明显改善”以及“稍有加重”“加重”“加重明显”分别计分“+1”“+2”“+3”分和“-1”“-2”“-3”分;没有改变仍记为“0”分。每组患者同期疗效评分之和即为疗效积分,最终分值越高说明疗效明显,分值越低说明疗效欠佳[5]。定义各组患者第6周(即慢性前列腺炎标准治疗疗程)疗效评分为最终治疗效果,进行统计学处理,作为2组疗效对比依据。
1.3 统计学分析计量资料以 ±s表示,各期均数比较采用成组t检验,其余采用秩和检验。采用SPSS 19.0统计软件进行分析。
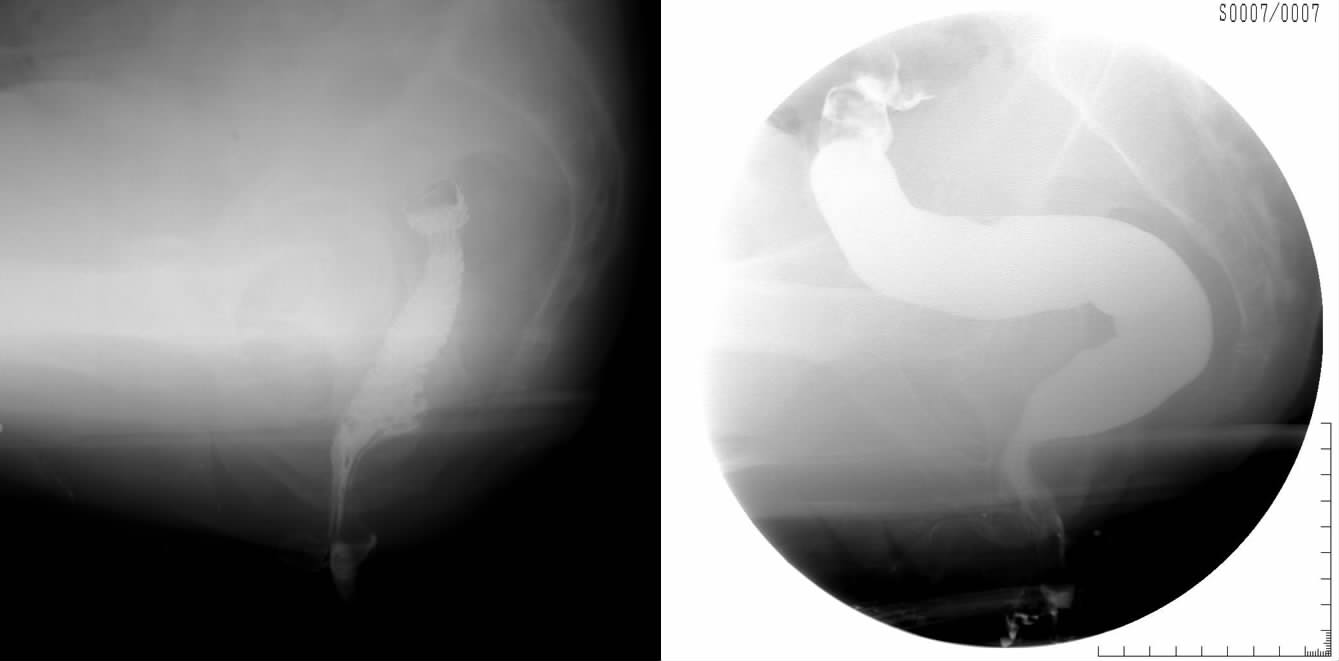
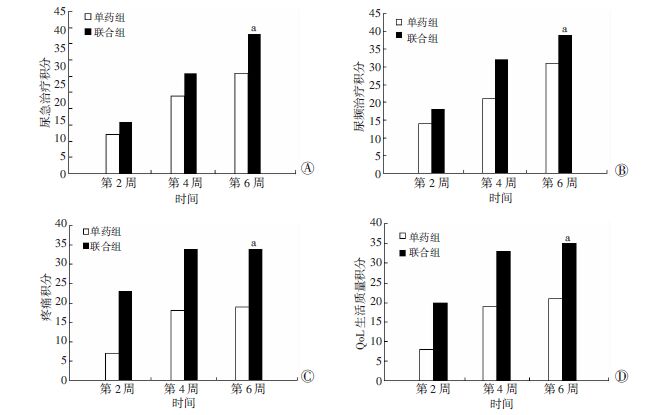
2 结果排粪造影结果见图 1,耻骨直肠肌痉挛患者表现为排便时耻骨直肠肌不能自然松弛,局部痉挛,压迫直肠肠壁形成切迹。2组Ⅲb型慢性前列腺炎患者的下尿路症状在治疗前IPSS评分及其中的中各单项症状评分、QoL评分基本一致,差异无统计学意义(P>0.05)。治疗后各随访时间点,IPSS评分差异无统计学意义(P>0.05)。单项症状评分发现在治疗2周时2组患者症状就有改善,第4周随访,2组患者症状持续好转,但是尿频、尿急和尿不尽3项症状评分,B组明显好于A组(P<0.05),第6周随访,2组患者症状稳定(表 1)。采用疗效评分比较2组患者在尿频、尿急、疼痛和生活质量方面的改善程度,可见联合Cox-2抑制剂治疗可明显提高CPⅢb的治疗效果,优于单用α-受体阻滞剂组(P<0.05,图 2)。
|
| A:正常对照;B:耻骨直肠肌痉挛患者 ↑:示典型耻骨直肠肌痉挛,即“鹅肠” 图 1 正常对照和耻骨直肠肌痉挛患者排粪造影表现 |
| 组别 | 症状 | 初始IPSS症状评分 | 治疗进展评分 | ||
| 第2周 | 第4周 | 第6周 | |||
| 单药组 | 尿频 | 3.95±0.97 | 3.20±0.84 | 2.85±0.60 | 2.60±0.64 |
| 联合组 | 4.00±0.90 | 3.00±0.60 | 2.00±0.50a | 1.15±0.68a | |
| 单药组 | 尿急 | 4.00±1.10 | 3.10±0.83 | 2.93±1.10 | 2.00±0.30 |
| 联合组 | 3.85±0.91 | 3.15±0.88 | 2.45±0.70a | 1.70±0.93 | |
| 单药组 | 尿不尽 | 3.55±1.14 | 3.12±0.67 | 2.25±0.73 | 1.35±0.99 |
| 联合组 | 3.50±1.15 | 2.27±0.80a | 1.55±0.69a | 1.35±0.79 | |
| 单药组 | 尿中断 | 1.65±1.25 | 1.00±0.80 | 0.95±0.76 | 0.90±0.63 |
| 联合组 | 1.45±0.75 | 0.85±0.34 | 0.75±0.45 | 0.85±0.43 | |
| 单药组 | 尿线细 | 1.95±1.16 | 0.90±0.63 | 0.75±0.53 | 0.70±0.49 |
| 联合组 | 1.95±0.76 | 1.10±0.65 | 0.75±0.53 | 0.80±0.32 | |
| 单药组 | 尿等待 | 2.90±1.32 | 1.70±1.03 | 1.10±0.63 | 0.80±0.48 |
| 联合组 | 2.55±1.41 | 1.75±1.05 | 1.15±0.53 | 0.85±0.34 | |
| 单药组 | 夜尿次数 | 1.35±1.12 | 0.65±0.72 | 0.45±0.54 | 0.35±0.46 |
| 联合组 | 1.65±1.09 | 0.75±0.67 | 0.40±0.48 | 0.25±0.38 | |
| 单药组 | 总分 | 19.12±1.08 | 16.84±0.81 | 9.81±1.01 | 8.87±1.14 |
| 联合组 | 18.97±0.94 | 17.12±0.97 | 10.07±0.77 | 8.41±1.21 | |
| a:P<0.05与单药组比较 | |||||
|
|
A:尿急治疗积分对比;B:尿频治疗积分对比;C:疼痛积分对比;D:QoL生活质量积分对比;治疗前各积分均为0 a:P<0.05,与单药组比较 图 2 尿频、尿急、疼痛以及生活质量治疗前及治疗后各期2组患者回访症状积分 |
前列腺炎是临床最为常见的一组病症,按照NIH分类,Ⅰ、Ⅱ和Ⅲa 型前列腺炎的病因、发病机制以及治疗方案均比较明确,Ⅲb和Ⅳ型前列腺炎的病因、发病机制以及治疗方案则比较混乱,尤其是CPⅢb临床上不仅常见,而且治疗效果不好,究其原因是该型前列腺炎发病机制不详,认为除炎症因素外,可能和排尿功能障碍、精神心理因素、神经内分泌因素、免疫反应异常、盆底相关疾病因素以及下尿路功能障碍等因素有关,故又称之为慢性骨盆疼痛综合征[6]。CPⅢb患者的尿液、前列腺液检查无炎症表现,而Ⅳ型前列腺炎患者前列腺液检查有炎症依据,却没有临床症状,这一现象导致人们对前列腺炎发病机制、分类及诊断的质疑。
2008年Shocks等[7]针对前列腺炎以及下尿路症状相关的临床研究提出了“UPOINT”分类概念,认为既往定义的前列腺炎及其临床表现并不仅仅限于前列腺,而是涉及前列腺、直肠、盆底功能以及心理等因素的一组临床征象,盆底功能障碍和肠道激惹现象在上述征象的发生中有重要作用。我们利用排粪造影技术研究了“前列腺炎”患者的盆底功能改变,发现以“前列腺炎”或下尿路症状就诊的患者绝大多数伴有直肠、盆底运动功能改变和/或耻骨直肠肌痉挛。耻骨直肠肌参与肛提肌的形成,是盆膈重要组成部分,与尿生殖膈的会阴深横肌共同附着于会阴中心腱。盆膈对盆底张力的维持,肛门外括约肌、尿道外括约肌功能具有重要作用。传统理论认为正常的排便过程由耻骨直肠肌主动松弛,降低肛管内压,使肛管与直肠前壁的夹角(肛直角)增大形成一个钝角从而使大便顺利排出。而痉挛的耻骨直肠肌则失去主动松弛的作用,肛直角不能顺利增大,肛管内压增高,典型的排粪造影可以显示耻骨直肠肌压迹,形成“鹅征”,是引起功能性便秘的重要原因[8 ,9]。Goncalves和他的团队[10]在一项涉及女性膀胱活动过度(OAB)的研究中,通过测定肛管内压发现其研究对象中所有耻骨直肠肌痉挛的患者都在OAB组,而对照组未发现1例,认为OAB患者发生尿频、尿急与耻骨直肠肌痉挛有关。耻骨直肠肌作为盆底肌群的组成部分,其痉挛通过提高盆底张力引发类似于膀胱出口梗阻(BOO)效应,增加膀胱内压引发患者尿频、尿急症状[11]。我们对门诊以“前列腺炎”就诊的患者用排粪造影研究发现伴有耻骨直肠肌痉挛的CPⅢb者的下尿路症状均以尿频、尿急等症状为主。本研究发现,虽然单用α-受体阻滞剂可缓解症状,但联合应用Cox-2抑制剂缓解耻骨直肠肌痉挛可进一步改善尿频、尿急、尿不尽感等和尿道及其周围肌肉痉挛有关的症状,而对尿中断、尿等待、夜尿次数增多等症状无进一步改善,表明其效果和缓解耻骨直肠肌痉挛有关,说明耻骨直肠肌痉挛在CPⅢb的发病机制中发挥了重要作用。
众所周知,尿道平滑肌痉挛是前列腺炎、前列腺增生患者产生尿频、尿急的重要机制,α-受体阻滞剂缓解尿道平滑肌痉挛可解除尿频、尿急现象。我们观察到单用α-受体阻滞治疗Ⅲb型前列腺炎可一定程度改善尿频、尿急、尿不尽感等一系列临床症状。因此,α-受体阻滞剂治疗Ⅲb前列腺炎也成为中华医学会泌尿外科分会《前列腺炎诊断治疗指南》所推荐[12]。尿道平滑肌和耻骨直肠肌分属于不随意肌(平滑肌)和随意肌(横纹肌),隶属于不同的神经支配,发生痉挛的机制不同。目前对耻骨直肠肌痉挛缺乏研究,可能和肠道激惹、相关炎症因子以及它们引起的盆神经丛功能紊乱有关[13]。Cox-2抑制剂属于非甾体类抗炎制剂,具有抗炎、止痛作用。研究发现Cox-2抑制剂塞来昔布可明显缓解会阴切开后发生的盆底疼痛,尤其是可以缓解耻骨直肠肌痉挛性疼痛。Hsieh等[14]利用低能激光治疗肌肉筋膜痛,证实肌肉筋膜疼痛的改善与包括Cox-2在内的细胞炎症因子的减少以及缓解肌肉痉挛有关。本研究结果表明,联合应用Cox-2抑制剂塞来昔布不仅明显改善了CPⅢb患者的各项临床症状,尤其是与尿道平滑肌、耻骨直肠肌痉挛相关的尿频、尿急、尿不尽等症状,而且明显改善了疼痛和QoL评分(P<0.05),进一步说明了耻骨直肠肌痉挛在CPⅢb症状发生中具有重要作用。
精神焦虑因素往往也是引发CPⅢb尿频、尿急以及肌肉筋膜痛的重要原因,有研究提示持续性精神应激可以使得Cox-2在外周高水平表达,在失眠、焦虑状态下,皮质脊髓等高位神经元传导异常冲动,导致兴奋性冲动与抑制性冲动失衡而影响下神经元。而这种失平衡则能引发慢性肌肉筋膜疼痛综合征[15]。使用Cox-2抑制剂可以显著改善患者持续的焦虑状态,平衡皮质脊髓的兴奋传导与抑制传导的程度[16]。Cox-2抑制剂塞来昔布的作用可能和改善患者的精神应激引起的Cox-2高表达、影响疼痛的传导形式,改善患者主观的疼痛感受有关。参照Charach等[5]介绍的评分方法,对患者尿频、尿急、疼痛和QoL进行评价,更客观、明确地显示了Cox-2抑制剂对CPⅢb的治疗作用。
综上所述,前列腺炎是一种常见病、多发病,发病机制不详,治疗效果不佳,尤其是CPⅢb在发病机制和治疗上存在较多争议,有待深入研究。本研究发现联合使用Cox-2抑制剂缓解耻骨直肠肌痉挛可明显提高CPⅢb的治疗效果,并且显著缓解患者盆底疼痛不适,改善患者生活质量,提示耻骨直肠肌痉挛在CPⅢb的发病机制中起到重要作用,为进一步研究CPⅢb的发病机制、探索治疗方法提供了新的思路。
| [1] | Screponi E, Carosa E, Di-Stasi S M, et al. Prevalence of chronic prostatitis in men with premature ejaculation[J]. Urology, 2001, 58(2): 198-202. |
| [2] | Lan T, Wang Y, Chen Y, et al. Influence of environmental factors on prevalence, symptoms, and pathologic process of chronic prostatitis/chronic pelvic pain syndrome in northwest China[J]. Urology, 2011, 78(5): 1142 1149. |
| [3] | Wu C, Zhang Z, Lu Z, et al. Prevalence of and risk factors for asymptomatic in flammatory (NIH-IV) prostatitis in Chinese men[J]. PLoS One, 2013, 8(8): e71298. |
| [4] | Potts J, Payne R E. Prostatitis: Infection, neuromuscular disorder, or pain syndrome? Proper patient classification is key[J].Cleve Clin J Med, 2007, 74 Suppl 3: S63-S71. |
| [5] | Charach G, Greenstein A, Rabinovich P, et al. Alleviating constipation in the elderly improves lower urinary tract symptoms[J]. Gerontology, 2001, 47(2): 72-76. |
| [6] | R. Soler, K. E. Andersson, M. B. Chancellor, et al.Future direction in pharmacotherapy for non-neurogenic male lower urinary tract symptoms[J].Eur Urol, 2013, 64: 610-621. |
| [7] | Shoskes D A, Nickel J C, Rackley R R, et al. Clinical phenotyping in chronic prostatitis/chronic pelvic pain syndrome and interstitial cystitis: a management strategy for urologic chronic pelvic pain syndromes[J]. Prostate Cancer Prostatic Dis, 2009, 12(2): 177-183. |
| [8] | 王怀经, 张绍祥. 局部解剖学[M]. 2版. 北京: 人民卫生出版社, 2005: 223. |
| [9] | 熊坤林, 龚水根, 张伟国. 耻骨直肠肌综合征的影像学诊 断及临床意义[J]. 中华胃肠外科杂志, 2006, 9(6): 498-501. |
| [10] | Goncalves M L, Fernandes S F, de-Almeida R M, et al. Anorectal manometry evaluation in adult women with clinical and urodynamic diagnostics of overactive bladder[J]. Arq Bras Cir Dig, 2013, 26(4): 280-285. |
| [11] | 那彦群, 郭震华. 实用泌尿外科学[M]. 北京: 人民卫生出版社, 2009: 335-337. |
| [12] | Shim S R , Kim J H , Choi H, et al. General effect of low-dose tamsulosin (0.2 mg) as a first-line treatment for lower urinary tract symptoms associated with benign prostatic hyperplasia: a systematic review and meta-analysis[J].Curr Med Res Opin, 2015, 31(2): 353-365. |
| [13] | Shah A P, Mevcha A, Wilby D, et al. Continence and micturition: an anatomical basis[J]. Clin Anat, 2014, 27(8): 1275-1283. |
| [14] | Hsieh Y L, Yang S A, Yang C C, et al. Dry needling at myofascial trigger spots of rabbit skeletal muscles modulates the biochemicals associated with pain, inflammation, and hypoxia[J]. Evid Based Complement Alternat Med, 2012, 2012: 342165. |
| [15] | Vidor L P, Torres I L, Medeiros L F, et al. Association of anxiety with intracortical inhibition and descending pain modulation in chronic myofascial pain syndrome[J]. BMC Neurosci, 2014, 15: 42. |
| [16] | Gurvich A, Begemann M, Dahm L, et al. A role for prostaglandins in rapid cycling suggested by episode-specific gene expression shifts in peripheral blood mononuclear cells: a preliminary report[J]. Bipolar Disord, 2014, 16(8): 881-888. |



