200038 重庆,第三军医大学西南医院全军眼科中心,视觉损伤与再生修复重庆市重点实验室
2Center of Ophthalmology,Chongqing Key Laboratory of Visual Damage and Regeneration & Restoration,Southwest Hospital,Third Military Medical University,Chongqing,400038,China
视网膜电图(electroretinogram,ERG)因其可以客观、无创地评估视网膜内不同神经元的功能,被广泛应用于临床和基础研究中[1]。ERG的b波是其主要成分,近来研究表明其起源于代谢型谷氨酸受体(mGluR6)介导的G蛋白偶联通路,尤其是暗适应ERG的b波,主要来源于ON型视杆双极细胞[2]。Müller细胞作为一种横贯视网膜的胶质细胞,具备维持视网膜内谷氨酸代谢、水及钾离子平衡等功能,特异性的损伤或敲除某一部分功能可以导致b波幅值的改变[3]。谷氨酰胺合成酶(GS)可以将转运到Müller细胞内的谷氨酸转变为无毒性作用的谷氨酰胺,形成了重要的谷氨酸-谷氨酰胺循环,使用药物特异性的抑制GS的表达可以降低ERG的幅值[4]。本研究中,Müller细胞GS活性选择性被DL-AAA抑制,它是一种6个碳的类似于兴奋性谷氨酸化学物质,是星形胶质细胞的谷氨酸受体的竞争物,可以通过降低GS活性破坏Müller细胞的谷氨酸代谢[5]。通过建立该模型来评估Müller细胞对ERG的作用,利用小波分析提取b波的时频域特征,以期获得有效的、特异性的评估Müller细胞功能的功能参数,为临床及基础研究提供有效的评价依据。
1 材料与方法 1.1 动物出生后30 d的Rcs-rdy+-p+大鼠18只(由第三军医大学大坪医院野战外科研究所实验动物中心提供,不分雌雄)。外眼和检眼镜检查屈光间质清晰,眼底无病变。予以12 h 明-暗交替光照,不限食水,室温18~23 ℃条件下饲养。
1.2 视网膜下腔注射视网膜下腔注射不同浓度的DL-AAA溶液(7、70、140 μg/μL)。使用玻璃微电极通过视网膜颞侧巩膜处注射到视网膜下腔。对每只动物,右眼注射4 μL DL-AAA,同样剂量的PBS注射到左眼作为对照组。大鼠均在麻醉状态下行各种手术操作,并使用直接检眼镜检测大鼠的眼底。注射后7 d行ERG检测。
1.3 ERG记录方法采用RETI-scan系统视觉电生理检测仪(德国Roland 公司)记录闪光ERG。刺激器为Ganzfeld 全野刺激器。 记录电极为gold-foil 环状角膜电极(德国Roland 公司),参考电极和接地电极分别为不锈钢自制针状电极,各电极自身阻抗均小于5 kΩ。同时记录双眼数据。实验前大鼠暗适应12 h ,行肌肉注射麻醉(速眠新注射液,长春农牧大学兽医研究所,0.004 mL/kg),常规散瞳(复方托吡卡胺,日本参天制药),于暗红光下安放电极,记录电极分别置于双眼角膜,以人工泪液保持角膜滋润,参考电极分别刺入双侧颊部皮下,接地电极置于尾部。再次暗适应10 min 后,行ERG记录。采用6种不同刺激光强(-20、-10、-5、0、5 dB)进行刺激,刺激频率为0.06 Hz,带宽为0.2~300 Hz,依据刺激强度每次刺激间隔为1~2 min。b/a是指同一ERG种b波的幅值与a波的幅值比[6]。T1/2d是指b波的半数最大值之间的时程[7]。
1.4 免疫组化大鼠使用三溴乙醇麻醉后,使用4%的PFA/PBS灌注,冰冻切片后可行免疫荧光染色。视网膜从眼眶中分离出来,然后将其轻轻地从巩膜和色素上皮层分开。使用0.01 mol/L的磷酸盐缓冲剂冲洗。分离的眼睛进一步用4%的PFA/PBS固定,然后30%蔗糖溶液浸泡16 h,最后使用OCT低温储存。冰冻切片被保存在-80 ℃。切片放于空气中干燥,使用PBS冲洗5 min,然后孵化,使用兔抗GS受体,在0.25%的Triton X-100和0.25%小牛血清4 ℃过夜。切片清洗3次,使用二抗室温孵化1 h。所有切片冲洗后封装好,使用DAPI染核。
1.5 统计学方法所有ERG数据的处理使用Matlab7.4及Excel软件进行分析。首先导出数据用Matlab7.4进行预处理,提取b波;自编程序行小波变化(Morlet小波)。使用SPSS 10.0行统计学分析,采用配对样本t检验。
2 结果 2.1 DL-AAA降低ERG的幅值视网膜下注射不同浓度DL-AAA后记录其ERG,ERG的分析参数主要是a、b波的幅值,b/a比值和T1/2d。结果表明随着药物浓度的升高,ERG的a、b波幅值均明显降低(图 1A):与PBS组相比,低浓度DL-AAA(7 μg/μL)的ERG波形无明显改变,中高浓度DL-AAA(70 μg/μL和140 μg/μL)的a、b波幅值均明显降低(P<0.05,P<0.01,图 1B~E)。中浓度时,b/a比值没有出现明显变化,提示b波的幅值降低 是由a波幅值降低引起的,而在高浓度时,b/a幅值明显降低(P<0.01),且T1/2d亦出现明显延迟(P<0.05),提示在该浓度下,b波自身出现降低。表明视网膜下腔注射DL-AAA可以引起ERG不同成分的改变,当浓度较高时,ERG的各主要成分均出现明显改变。

|
| A:PBS及不同浓度DL-AAA注射到视网膜下腔后典型ERG波形(红色为DL-AAA注射眼,蓝色为PBS注射眼);B~E:对应的ERG参数分析,依次为a波幅值、b波幅值、 b/a值、T1/2d值;a:P<0.05,b:P<0.01,与DL-AAA眼比较 图 1 不同浓度DL-AAA对ERG的影响 |
为了进一步确定视网膜下腔注射DL-AAA对Müller细胞GS的作用,使用免疫荧光确定GS的表达水平,如图 2所示。相对于PBS眼,DL-AAA组的GS表达荧光水平明显降低。

|
| A、C:PBS注射眼;B、D:DL-AAA注射眼;C、D:为图A、B白色矩形框内的放大图像;GCL:视网膜节细胞层,INL:内核层,ONL:外核层 图 2 免疫荧光观察DL-AAA降低GS的表达水平 |
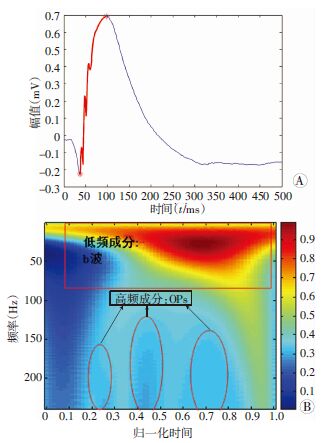
ERG的b波由软件自动截取,如图 3A所示,在a波出现的时间范围内自动寻找其最低点,在b波出现的时间范围内寻找最大值,然后截取两者之间的部分,先行归一化处理后行小波分析,分析如图 3B所示伪彩图。图 3B中圆圈部分主要是视网膜振荡电位(oscillatory potentials,OPs)的贡献,而上方红色部分则主要是b波的贡献。
|
| A:典型的ERG波形,通过选取波谷与波峰提取的b波成 分;B:小波分析后的典型波形,不同伪彩区域为不同的成分 图 3 提取ERGb波及其小波变化 |
接下来对分离出的b波进行小波变换,如图 4所示,包络阈值设定为0.8,即满足80%相似度的归为一类画出包络线,蓝色代表DL-AAA注射组,红色表示PBS注射组,3组的PBS眼的包络阈值均较稳定,其环域面积未出现明显改变,而DL-AAA眼随着其浓度的增加,环域面积出现改变。为了进一步提取该信息,分析其最小环比,图中黑色表示DL-AAA注射眼,绿色表示PBS注射眼。随着DL-AAA浓度增加,最小环比面积增加,环中心时间后移且频域范围变宽。

|
| A:低浓度;B:中浓度;C:高浓度;蓝色为DL-AAA注射眼的包络线,红色为PBS注射眼的包络线,黑色为DL-AAA注射眼的环域面积,绿色为PBS注射眼的环域面积 图 4 小波分析提取不同浓度DL-AAA作用下ERGb波的信息 |
DL-AAA是谷氨酸的类似物,当通过视网膜下腔给药时,“谷氨酸”的浓度升高。正常情况下,暗环境中,视网膜光感受器持续释放谷氨酸。当光刺激开始时,光感受器停止释放谷氨酸,产生ERG,其不同成分起源不同,a波主要来源于光感受器,b波则是ON型双极细胞。细胞外多余的谷氨酸必须被快速的移除,否则会产生兴奋性毒性。 尽管有研究指出,外层视网膜的谷氨酸清除主要依赖位于光感受器和双极细胞上的谷氨酸转运体5(EAAT5)[8],但在谷氨酸转运体1(GLAST)敲除鼠中可以观察到b波幅值的降低,GLAST仅表达在Müller细胞上[9];同时通过玻璃体腔给药抑制GS后,也可引起同样的效用,GS亦是特异性的表达在Müller细胞上[4],既往研究表明Müller细胞在调节谷氨酸代谢时会影响视网膜对光反应。本实验采用的DL-AAA抑制GS,给药方式是视网膜下腔,有研究指出视网膜下腔注射DL-AAA会引起光感受器的变化[10],文中a波幅值降低提示光感受器受损。当DL-AAA浓度较高后,不仅光感受器受损,双极细胞亦受影响。虽然本研究没有探讨DL-AAA影响视网膜神经元对光反应的具体机制,但a、b波幅值的降低是由于位于Müller细胞上的GS被抑制后而引起的。
小波分析方法是信号处理中的“显微镜”,通过母小波函数“放大”局部信号,可以提取更加细微的变化。目前小波分析方法在ERG的应用上主要集中在OPs和a波上[11, 12, 13]:随着刺激光强度的增加,OPs的峰频增加,峰时提前,而a波则在刺激光强度增加的时候出现高频成分。本研究通过视网膜下腔注射不同浓度的DL-AAA,采用小波分析其ERG的b波变化,发现随着药物浓度的增加,最小环比面积增加,提示电信号离散度增加即稳定性降低,环中心延迟提示慢相成分出现。结果提示Müller细胞上GS对维持视网膜内谷氨酸代谢的平衡性起到了重要的作用,最小环比是谷氨酸代谢功能出现异常的敏感指标。该研究为临床及基础研究提供了一种客观评估视网膜内谷氨酸循环对神经元功能影响的依据。
| [1] | 李海生, 潘家普. 视觉电生理的原理与实践[M]. 上海: 上海科学普及出版社, 2002: 111-112. |
| [2] | Koike C, Obara T, Uriu Y, et al. TRPM1 is a component of the retinal ON bipolar cell transduction channel in the mGluR6 cascade[J]. Proc Natl Acad Sci U S A, 2010, 107(1): 332-337. |
| [3] | Bringmann A, Pannicke T, Grosche J, et al. Muller cells in the healthy and diseased retina[J]. Prog Retin Eye Res, 2006, 25(4): 397-424. |
| [4] | Bui B V, Hu R G, Acosta M L, et al. Glutamate metabolic pathways and retinal function[J]. J Neurochem, 2009, 111(2): 589-599. |
| [5] | Welinder E, Textorius O, Nilsson S E. Effects of intravitreally injected DL-alpha-aminoadipic acid on the c-wave of the D. C. -recorded electroretinogram in albino rabbits[J]. Invest Ophthalmol Vis Sci, 1982, 23(2): 240-245. |
| [6] | Nguyen C T, Vingrys A J, Wong V H, et al. Identifying cell class specific losses from serially generated electroretinogram components[J]. Biomed Res Int, 2013, 2013: 796362. |
| [7] | Dong C J, Hare W A. GABAc feedback pathway modulates the amplitude and kinetics of ERG b-wave in a mammalian retina in vivo[J]. Vision Res, 2002, 42(9): 1081-1087. |
| [8] | Hasegawa J, Obara T, Tanaka K, et al. High-density presynaptic transporters are required for glutamate removal from the first visual synapse[J]. Neuron, 2006, 50(1): 63-74. |
| [9] | Harada T, Harada C, Watanabe M, et al. Functions of the two glutamate transporters GLAST and GLT-1 in the retina[J]. Proc Natl Acad Sci U S A, 1998, 95(8): 4663-4666. |
| [10] | Shen W, Zhang J, Chung S H, et al. Submacular DL-alpha-aminoadipic acid eradicates primate photoreceptors but does not affect luteal pigment or the retinal vasculature[J]. Invest Ophthalmol Vis Sci, 2011, 52(1): 119-127. |
| [11] | Forte J D, Bui B V, Vingrys A J. Wavelet analysis reveals dynamics of rat oscillatory potentials[J]. J Neurosci Methods, 2008, 169(1): 191-200. |
| [12] | Barraco R, Persano-Adorno D, Brai M. An approach based on wavelet analysis for feature extraction in the a-wave of the electroretinogram[J]. Comput Methods Programs Biomed, 2011, 104(3): 316-324. |
| [13] | Barraco R, Persano-Adorno D, Brai M. ERG signal analysis using wavelet transform[J]. Theory Biosci, 2011, 130(3): 155-163. |



