随着全髋关节置换(total hip arthroplasty,THA)手术量的迅速增长,其翻修手术例数亦有明显增加,而翻修术中常见的髋臼骨缺损一直是对关节外科医师的巨大挑战。中、重度的骨缺损对翻修术式的选择及假体的固定均有明显影响[1, 2]。既往如钛网结合颗粒骨打压植骨、大块骨结构性植骨、加强环(ring或cage)等方法处理髋臼缺损,均并非完美,甚至存在一些争议[2, 3, 4]。近年来羟基磷灰石(hydroxyapatite,HA)等喷涂愈合面的Jumbo杯在髋臼骨缺损的翻修中应用日益广泛,文献[5, 6, 7, 8]已有较好的临床随访结果。但也有文献[9]报道,普通背侧处理的臼杯10年生存率并不理想,并分析髋臼侧的骨长入欠佳是其可能原因。最近10年,钽金属骨填充材料逐渐开始临床应用,钽金属杯也在严重骨质疏松和缺损的初次置换中被采用[10],钽金属Jumbo杯也许是解决普通背侧处理生物Jumbo杯骨长入能力不足的策略。本研究回顾性分析钽金属Jumbo杯在髋臼骨缺损的全髋关节翻修中的近期疗效,评价该方式是否更利于此类病例的处理。
1 资料与方法 1.1 一般资料收集2009年9月至2012年9月在我中心接受髋关节翻修手术的18例患者的临床资料,包括男性8例,女性10例,年龄37~76(56.8±15.3)岁。THA术后感染二期翻修3例,髋臼金属炎性假瘤3例,假体无菌性松动12例。合并高血压病9例,冠心病7例,2型糖尿病7例,慢性支气管炎3例,骨质疏松症13例。纳入标准:①髋臼存在Paprosky分型Ⅱ型及以上骨缺损;②使用钽金属Jumbo杯(Zimmer,美国)重建髋臼骨缺损者。排除标准:①任何原因导致的失访;②随访期间意外外伤出现假体周围骨折。
1.2 骨缺损评估全部病例在髋臼负重区、前后柱及内壁存在不同程度的容积性或结构性骨缺损。Paprosky分型:Ⅱb型6例,Ⅱc型7例,Ⅲa型2例,Ⅲb型3例。
1.3 假体选择臼杯外径均达Jumbo杯界定标准(欧美国家外径:女性≥62 mm,男性≥66 mm或大于初始臼杯外径10 mm[5];亚洲国家外径:女性≥60 mm,男性≥64 mm[11]),钽金属层与松质骨界面摩擦系数0.98,孔隙率80%,孔隙大小400 μm,为多孔三维结构,弹性模量3 GPa,与人体软骨下骨弹性模量近似(1.5 GPa)。臼杯含三孔型和多孔型。本组13例患者使用三孔臼杯,5例使用多孔钽臼杯(术中根据髋臼骨量及螺钉安放位置决定)。界面选择高交联超高分子聚乙烯衬垫匹配32 mm陶瓷头(Zimmer,美国)。
1.4 手术方法 1.4.1 手术入路及显露手术均由同一名高年资专科医师完成。患者取健侧卧位,全身麻醉。手术入路选择常规后外侧入路,若原切口接近此入路则按原切口作为入路,显露方法按陈光兴等[12]方法。
1.4.2 髋臼处理彻底清除髋臼周围瘢痕、骨赘,充分显露髋臼,依次取出内衬、臼杯,内陷臼杯取出时注意避免损伤盆腔内壁血管,清除磨损碎屑、炎性假瘤、骨水泥,刮除囊变区肉芽组织,保持外展45°、前倾25°用髋臼锉磨锉髋臼,磨锉时需小心、轻柔,减少进一步的骨丢失,依次增大至适宜型号,骨缺损区域选择颗粒打压植骨,保持2 mm压配置入髋臼杯,锤击臼杯时同样忌用暴力,以免髋臼骨折,2~4枚螺钉加强固定。本组病例髋臼宿主骨面均大于30%,Ⅱ型6例于臼底部采用同种异体松质骨颗粒容积性植骨,7例未植骨;Ⅲ型5例于臼底及臼杯上缘、后上缘与宿主骨间采用异体颗粒骨打压植骨。
1.5 围手术期处理及康复训练预防感染:术前半小时使用抗生素1次,术后48 h内停药。镇痛:术前当晚及术晨各口服非甾体类抗炎药1次,术后48 h内使用注射用非甾体类抗炎药,随后改为口服非甾体类抗炎药至术后2周。预防深静脉血栓:术后6~10 h口服利伐沙班1片,其后每日1次至术后5周。继续基础疾病治疗,术后患肢穿防旋鞋,加强护理预防褥疮,早期行踝关节背伸跖屈主被动活动,股四头肌、股二头肌、臀大肌联合等长收缩运动,下肢加压静脉泵促进静脉回流预防深静脉血栓。鼓励患者尽早下床,术中骨质条件可,压配满意,骨覆盖70%以上者术后直接负重,术中发现骨质疏松明显,骨覆盖 不足70%者早期部分负重,根据界面骨长入情况于6周 至3个月逐渐恢复负重。
1.6 术后随访及评价指标手术前后行Harris评分评价患髋功能,VAS评分评价疼痛程度。术后6周,3、6个月,1年及以后每年随访1次,摄标准骨盆正位X线片及患髋侧位片,观察髋关节假体位置、旋转中心、髋臼外展角及有无移位等,按DeLee-Charnley分区法[13]评估假体周围透光线,按Anderson骨长入影像学评价标准[14]评价骨长入情况。
1.7 统计学处理使用SPSS 15.0统计软件,数据以x±s表示,手术前后评分比较采用配对t检验。
2 结果 2.1 随访18例患者均未失访,随访时间24~54个月,平均35.7个月。术后患髋疼痛症状均有明显缓解,按个体计划进行功能锻炼,8例患者在2周内弃拐,10例患者于6周至3个月弃拐。术后发生后脱位1例(术后4周),为类风湿性关节炎左THA术后炎性假瘤致髋臼假体无菌性松动行翻修患者,经手法复位,髋人字支具保护6周后未再复发(图 1)。无感染、神经损伤、深静脉血栓等其他并发症。
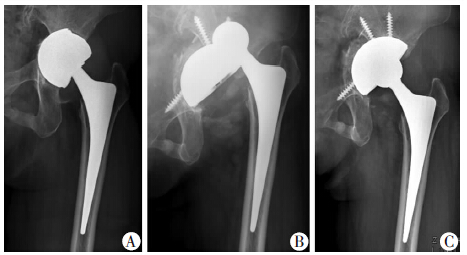 |
| A:翻修术前正位X线片;B:翻修术后4周脱位,X线片示 臼杯无松动;C:术后6个月正位X线片,植骨区骨融合良好图 1 左THA术后32个月炎性假瘤致髋臼假体无菌性松动Paprosky Ⅱc型女性患者翻修术前及术后4周、6个月X线片表现 |
患者术后疼痛程度较术前明显降低,功能改善明显。末次随访时Harris评分Paprosky Ⅱ型为(84.8±11.8) 分,明显高于术前(48.3±12.5)分,(t=-13.8,P<0.01);Ⅲ型为(77.8±9.3)分,明显高于术前(38.5±10.6)分(t=-16.4,P<0.01)。末次VAS评分Paprosky Ⅱ型为(1.1±0.7)分,低于术前(3.8±1.5)分(t=14.7,P<0.01);Ⅲ型为(1.9±1.2)分,明显低于术前(5.1±1.6)分(t=19.2,P<0.01)。
2.3 影像学评估末次随访时X线片见所有患者髋臼杯无移位,臼杯与骨面接触紧密,骨缺损区被完全填充,植骨整合替代情况满意,假体周围有辐射状骨小梁密度增加影像,均未见假体周围透亮线及骨溶解,按照Anderson影像学标准,18例臼杯均获得良好骨长入,假体稳定,生存率100%。臼杯外展角平均47.6°(42°~55°),超过50°者3例,均未发生脱位,1例43°者于术后4周发生后脱位1次。术前旋转中心较对侧平均高12.2 (3~30)mm,术后较对侧平均高2.6(0~7)mm,原臼杯内陷致旋转中心内移者(7例)同时有臼杯位置及旋转中心向外恢复移位,臼杯内缘均恢复至髂坐线以外,旋转中心平均外移3.1(0.5~8)mm(图 2)。
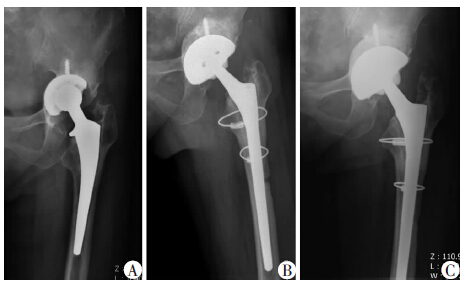 |
| A:翻修术前正位X线片;B:术后3个月正位X线片示植骨区骨融合良好,旋转中心向外下移位,接近正常;C:术后18个月正位X线片示植骨区骨融合进一步改善,假体位置良好图 2 左THA术后68个月骨溶解致髋臼假体无菌性松动,Paprosky Ⅲ b型女性患者翻修术前及术后3、18个月X线片表现 |
患者男性,62岁,右THA术后9年骨溶解致髋臼假体无菌性松动,Paprosky Ⅲb型,术前Harris评分35分,VAS评分5分,术后1年Harris评分82分,VAS评分1分(图 3)。
 |
| A:翻修术前正位X线片;B、C:术后6周、1年正位X线片;D:术后下蹲功能像图 3 右THA术后9年骨溶解致髋臼假体无菌性松动Paprosky Ⅲ b型男性患者翻修术前及术后6周、1年X线片表现和术后下蹲功能像 |
在髋关节翻修术中处理合并髋臼明显骨缺损时,合理处理一直是个挑战。既往出现了一些方法和设计,但均或多或少存在一些不尽如人意之处,如钛网结合颗粒骨打压植骨、大块骨结构性植骨、加强环(ring或cage)、高旋转中心放置臼杯等方法,操作过程复杂,手术时间长,异体骨需求量大,增加感染风险,骨水泥固定远期存活率低,高旋转中心降低生物力学效能。Jumbo杯具有操作技术简化,能提供足够的假体与宿主骨接触面,减少对移植骨的需求及可能恢复正常旋转中心等优点[5, 15, 16],其临床应用日益广泛,已有许多短期临床随访文献报道了良好的临床结果[6, 11],同时也有少量中-远期随访结果报道。Wedemeyer等[17]报道了一组病例的Jumbo杯在平均随访7年时生存率达94%。Lachiewicz等[8]报道使用Jumbo杯的129例患者,设立髋臼再翻修或影像学证实臼杯松动、任何原因所致臼杯取出、涉及髋关节的再次手术3个终点,10年生存率分别为97.3%、93.8%、88.5%,15年生存率分别为82.8%、79.8%、56.5%。本组病例术后均获得良好临床效果,术后Harris评分较术前明显提升,在相对较短的临床随访中生存率高。
获得臼杯较高的远期生存率需要稳定的初始固定和良好的骨长入两个前提。部分严重髋臼骨缺损病例通过结构性植骨、多枚螺钉固定等方法可增加普通生物型髋臼杯的初始稳定性,但由于宿主骨以硬化骨为主,血供差,骨床质量差。
骨质疏松明显,缺损区植骨需较长时间整合,骨长入能力不足可致远期固定失效。既往许多普通型Jumbo杯背侧材料摩擦系数较低,诱导骨长入能力有限,在此类病例中存在一定劣势,臼杯的初始稳定相对不足,背侧愈合并非完美,影响远期的假体生存率。钽金属材料骨小梁结构表面的臼杯孔隙率能够达到75%~80%,可为骨小梁长入提供类似松质骨的蜂窝结构;其弹性模量和硬度与松质骨类似,应力传导更均匀,有利于成骨;摩擦系数是普通生物型臼杯的2~4倍,界面稳定性和松动峰值应力明显高于普通臼杯,具备更强的初始机械稳定性;另外钽金属的生物惰性较常用骨科金属内植物更高,不易定植和黏附细菌,在感染的二期翻修中应用更安全。Malkani等[18]的研究中使用钽金属臼杯的全部患者只有50%左右的宿主骨面积用于初始固定,术后2年内均未发生假体松动。本组患者全部选择钽金属Jumbo杯,术后X线片证实假体周围骨长入良好,异体骨整合顺利,随访期内无一例松动,佐证了这一界面在早期骨长入方面的优势。
术中面临不同程度骨缺损所致髋臼杯骨覆盖不足时有不同的处理选择。传统观念认为臼杯获得初始稳定至少需要50%的骨覆盖[19],也是大多数骨科医师所认同的。但随着较之常规假体具有更高孔隙率和更高摩擦系数材料的出现,这一观点开始受到挑战[20, 21]。Sternheim等[22]将采用多孔隙臼杯进行髋臼侧翻修的患者分为骨覆盖>50%和<50%两组,在平均6年的随访后,骨覆盖>50%组无一例假体松动,而骨覆盖<50%组则有7.5%的髋臼杯无菌性松动发生率。翻修患者在髋臼存在骨缺损同时,骨质量亦较差,臼杯的初始稳定会受到一定影响,尤其是前后柱缺损者,若初始稳定失效时因臼杯骨接触面不足,骨长入不佳,则必然出现松动结果。增加磨锉、增大臼杯直径旨在获得相对足够的初始稳定,同时增加假体与宿主骨接触面,增加骨长入概率,为长期的生物学固定创造条件,故在条件允许情况下应尽量通过磨锉、植骨、调整臼杯位置等方式增加臼杯骨覆盖,降低松动风险,若在使用大直径臼杯时仍遗留明显骨缺损,结构性植骨或钽金属垫块填充均是可行的方法。本组病例均通过加大磨挫,增加臼杯与宿主骨接触面积,覆盖均超过50%,辅以必要的螺钉内固定获得满意的初始稳定,术 后相应调整功能锻炼方案,为假体骨长入创造条件,最终达到生物固定,随访期内无一例出现臼杯松动、移位。
髋臼骨缺损患者常见旋转中心上移,采用高旋转中心放置臼杯,通过增加股骨柄颈长而弥补下肢长度及Offset的手术方式也是一种选择[23]。但高旋转中心在一定程度上仍会影响外展肌肉(主要为臀中肌)力臂,降低其生物力学效能,造成外展无力、跛行,增加患髋压力,影响假体寿命,同时可能造成假体撞击,增加脱位风险[24, 25]。Jumbo杯提供更大的周径使其安置位置更接近解剖位置,即使上方没有大块移植物,仍能避免过高的旋转中心,同时使旋转中心适当外移,增加外展力臂,改善关节生物学效能。本组患者即通过使用Jumbo杯结合植骨使高旋转中心恢复或接近正常,大部分患者在患肢长度恢复的同时,外展肌力得到明显改善,步态基本恢复正常,最明显1例患者旋转中心下移达23 mm,术后患肢长度恢复满意,外展肌力及跛行步态改善明显;有5例患者遗留轻度跛行,考虑与长期的功能障碍,既往手术致臀中肌损伤、失用,术后患肢肌力锻炼不足等因素有关,但较之术前跛行步态亦有明显改善,且随术后时间推移及功能锻炼的跟进,可有进一步的改善。同时所有患者臼杯位置无变化,证实了恢复旋转中心和外展力臂符合髋关节的生物力学需求,降低臼杯压应力,进而降低了臼杯早期松动移位的风险。
在关于Jumbo杯的研究中,术后并发症最常见的为后脱位,文献报道发生率为2.4%~21%,导致其发生的相关因素较多,包括手术入路、术中解剖、多次手术史、骨缺损量、臼杯安放位置、股骨头直径等。研究已证明<32 mm直径的股骨头假体与脱位有明显相关性[8]。Garbuz等[26]的一项前瞻性随机对照研究表明,平均5年随访使用36 mm和40 mm直径股骨头假体的脱位发生率为1.1%,而32 mm直径股骨头假体的脱位发生率为8.7%。另一较常见原因为部分患者术中为获得良好的骨覆盖,可能会增加臼杯外展角,减小 前倾角,均会增加后脱位风险。本组病例均采用32 mm 直径股骨头假体,发生1例脱位,为类风湿性关节炎左THA术后炎性假瘤致髋臼假体无菌性松动行翻修患者,初次手术选用金对金大直径头全髋关节假体,发生炎性假瘤概率较高,导致臼杯周围骨溶解并松动,术中彻底清除炎性假瘤及骨溶解病灶,同种异体颗粒骨植骨、固定,术后无骨溶解及炎性假瘤复发。术后臼杯外展角43°,分析脱位原因为髋臼后壁缺损明显,术中为获得良好骨性覆盖缩小臼杯前倾角;患者患有严重的类风湿性关节炎,双下肢多关节累及,肌力下降明显,活动协调性差,关节动静力稳定性差。而3例臼杯外展角>50°的患者术中将聚乙烯衬垫高边调整至后上方,术后严格避免屈髋内旋动作,均未发生脱位。故为了降低脱位发生率,髋臼位置(外展角和前倾角)正确安放,衬垫高边的适当调整,尽可能使用大直径股骨头假体,以及患者的教育和合理的功能锻炼都是需要强调的。
综上所述,将Jumbo杯的操作简便,提供足够的假体与宿主骨接触面,减少对移植骨的需求,尽可能恢复旋转中心等优点与钽金属界面优良的骨长入能力结合起来,为应对髋臼存在PaproskyⅡ型以上骨缺损的全髋关节翻修提供了很好的选择。本研究仍存在缺陷:①没有设置使用普通非骨水泥臼杯、钛笼或定制假体的对照组;②平均随访时间仅35.7个月,研究结论需要更长时间的随访加以证实;③采用X线片对假体周围骨长入情况进行评估而未行CT检查,对骨长入及骨溶解的判断可能存在误差;④对臼杯前倾角不能准确测量,不能准确评估其与脱位概率的关系。后期可多中心合作,纳入更大量的病例,设置选择其他材料的对照组并长期随访,将CT检查常规引入以更好地评估假体骨长入情况和测量前倾角。
| [1] | Haydon C M,Mehin R,Burnett S,et al. Revision total hip arthroplasty with use of a cemented femoral component. Results at a mean of ten years[J]. J Bone Joint Surg Am,2004,86-A(6):1179-1185. |
| [2] | Jain S,Grogan R J,Giannoudis P V. Options for managing severe acetabular bone loss in revision hip arthroplasty. A systematic review[J]. Hip Int,2014,24(2):109-122. |
| [3] | Wedemeyer C,Otte S,von-Knoch M,et al. Structural femoral head allografts in revision surgery of loosened acetabular cups[J]. Unfallchirurg, 2007, 110(2):104-110. |
| [4] | Patil N,Hwang K,Goodman S B. Cancellous impaction bone grafting of acetabular defects in complex primary and revisiontotal hip arthroplasty[J]. Orthopedics,2012,35(3):e306-e312. |
| [5] | Whaley A L,Berry D J,Harmsen W S. Extra-large uncemented hemispherical acetabular components for revision total hip arthroplasty[J]. J Bone Joint Surg Am,2001,83-A(9):1352-1357. |
| [6] | Hendricks K J,Harris W H. High placement of noncemented acetabular components in revision total hip arthroplasty. A concise follow-up,at a minimum of fifteen years,of a previousreport[J]. J Bone Joint Surg Am,2006,88(10):2231-2236. |
| [7] | Gustke K A,Levering M F,Miranda M A. Use of jumbo cups for revision of acetabulae with large bony defects[J]. J Arthroplasty,2014,29(1):199-203. |
| [8] | Lachiewicz P F,Soileau E S. Fixation,survival and dislocation of jumbo acetabular components in revision hip arthroplasty[J]. J Bone Joint Surg Am,2013,95(6):543-548. |
| [9] | Meneghini R M,Meyer C,Buckley C A,et al. Mechanical stability of novel highly porous metal acetabular components in revision total hip arthroplasty[J]. J Arthroplasty,2010,25(3):337-341. |
| [10] | Pulido L,Rachala S R,Cabanela M E. Cementless acetabular revision:past,present,and future. Revision total hip arthroplasty:the acetabular side using cementless implants[J]. Int Orthop,2011, 35(2):289-298. |
| [11] | Fan C Y,Chen W M,Lee O K,et al. Acetabular revision arthroplasty using jumbo cups:an experience in Asia[J]. Arch Orthop Trauma Surg,2008,128(8):809-813. |
| [12] | 陈光兴,古凌川,杨柳,等. 改良后外侧小切口全髋关节置换手术技术[J]. 中华关节外科杂志:电子版,2008,2(3):254-262. |
| [13] | DeLee J G,Charnley J. Radiological demarcation of cemented sockets in total hip replacement[J]. Clin Orthop Relat Res,1976(121):20-32. |
| [14] | Moore M S,McAuley J P,Young A M,et al. Radiographic signs of osseointegration in porous-coated acetabular components[J]. Clin Orthop Relat Res,2006,444:176-183. |
| [15] | Deirmengian G K,Zmistowski B,O’Neil J T,et al. Management of acetabular bone loss in revision total hip arthroplasty[J]. J Bone Joint Surg Am,2011,93(19):1842-1852. |
| [16] | Rees H W,Fung D A,Cerynik D L,et al. Revision total hip arthroplasty without bone graft of high-grade acetabular defects[J].J Arthroplasty, 2012, 27(1):41-47. |
| [17] | Wedemeyer C,Neuerburg C,Heep H,et al. Jumbo cups for revision of acetabular defects after total hip arthroplasty:a retrospective review of a case series[J]. Arch Orthop Trauma Surg,2008,128(6):545-550. |
| [18] | Malkani A L,Price M R,Crawford C H 3rd,et al. Acetabular component revision using a porous tantalum biomaterial:a case series[J]. J Arthroplasty,2009,24(7):1068-1073. |
| [19] | Haddad F S,Rayan F. The role of impaction grafting:the when and how[J]. Orthopedics,2009,32(9):675-679. |
| [20] | Lakstein D,Backstein D,Safir O,et al. Trabecular metal cups for acetabular defects with 50% or less host bone contact[J]. Clin Orthop Relat Res,2009,467(9):2318-2324. |
| [21] | Baad-Hansen T,Kold S,Nielsen P T,et al. Comparison of trabecular metal cups and titanium fiber-mesh cups in primary hip arthroplasty:a randomized RSA and bone mineral densitometry study of 50 hips[J]. Acta Orthop,2011,82(2):155-160. |
| [22] | Sternheim A,Backstein D,Kuzyk P R,et al. Porous metal revision shells for management of contained acetabular bone defects at a mean follow-up of six years:a comparison between up to 50% bleeding host bone contact and more than50% contact[J].J Bone Joint Surg Br,2012,94(2):158-162. |
| [23] | Gustke K A. Jumbo cup or high hip center:is bigger better?[J]. J Arthroplasty,2004,19(4 Suppl 1):120-123. |
| [24] | Morag G,Zalzal P,Liberman B,et al. Outcome of revision hip arthroplasty in patients with a previous total hip replacement for developmental dysplasia of the hip[J]. J Bone Joint Surg Br,2005,87(8):1068-1072. |
| [25] | Bozic K J,Freiberg A A,Harris W H. The high hip center[J]. Clin Orthop Relat Res,2004(420):101-105. |
| [26] | Garbuz D S,Masri B A,Duncan C P,et al. The Frank Stinchfield Award:dislocation in revision THA:do large heads (36 and 40 mm) result in reduced dislocation rates in a randomized clinical trial?[J]. Clin Orthop Relat Res,2012,470(2):351-356. |



