视网膜色素变性(retinitis pigmentosa,RP)是一种因基因变异导致的遗传性致盲性眼病。感光细胞的变 性和凋亡是视力持续性下降并最终失明的原因。 有部分患者还可出现黄斑水肿,据报道患病率在3%~25%[1],但其病理机制并未完全研究清楚。黄斑水肿可加重RP患者的中心视力下降。目前常用的玻璃体腔注射抗新生血管因子(anti-VEGF)或玻璃体腔注射曲安奈德(triamcinolone acetonide,TA),由于其有眼内感染、高眼压、白内障等风险,对于RP患者这样的低视力群体风险更大。因此,本研究探讨巩膜后注射TA在RP黄斑水肿患者治疗中的安全性和临床疗效。 1 资料与方法 1.1 研究对象
2013年2月至2014年3月,我院眼科门诊确诊为RP黄斑水肿患者10例。患者均通过视力、眼压、眼底彩色照相、眼底自发荧光(fundus autofluorescence,FAF)、眼底荧光造影(fundus fluorescein angiography,FFA)、光学相干断层扫描(optical coherence tomography,OCT)、闪光视网膜电图(flash electroretinogram,FERG)及多焦视网膜电图(multifocal electroretinogram,mfERG)等检查,认为其符合RP确诊标准。其中男性5例,女性5例;年龄14~59(34.9±13.6)岁;病程1~40(15.1±14.7)年;视力10~65(43.4±18.7)个字母数。6例自觉有夜盲病史,均无该病家族史。所有患者均完成术后1个月随访。
排除标准为:研究眼有其他眼科疾病,并会阻碍研究治疗改善视力;研究眼有眼内手术史;伴有严重全身疾病;治疗前1个月内参加过任何研究药物的临床研究;不能遵守随访流程。
巩膜后注药技术经第三军医大学西南医院伦理委员会批准,并在中国临床试验注册中心注册(注册号:ChiCTR-OPC-15005910),所有患者均在了解黄斑水肿及RP现有治疗措施和术中、术后的益处和风险后签署知情同意书。 1.2 方法 1.2.1 手术方法
用一种新型巩膜后注射装置[国家实用新型专利(巩膜后注射装置,ZL 2013 2 0740202.0)],包含注射针头和衔接器。其为弯曲的钝针头,弯曲度与眼球相近,使用时,注射针头只需连接普通的注射器,经颞侧结膜上的微创小切口,距角膜缘6 mm处紧贴巩膜进针,直至切口距针体尾部3 cm处时停止进针,在黄斑部后方紧贴巩膜后注射TA 20 mg,注药后观察药物无外流,缓慢拔出针头,纱布覆盖。 1.2.2 随访方法及观察指标
本组患者均完成术前和术后1周、1个月的随访,每次随访时由指定的技师负责视力、眼压、OCT的采集。视力(Snellen视力表及糖尿病性视网膜病变早期治疗视力检查表ETDRs检查患者裸眼及最佳矫正视力)、眼压(非接触式)。OCT采用日本Topcon 3D OCT仪进行检查,8条子午线方向扫描,扫描长度6 mm。测黄斑中心凹处视网膜内表面至视网膜色素上皮和脉络膜毛细血管光带之间的距离(厚度),其中黄斑1~9区平均厚度为黄斑区9个区域厚度值的均值,以中心凹中心为圆心显示为9个区域,依次编号为1~9,1为黄斑中心凹 (1区)(直径1 000 μm),2~5依次为内环(直径1 000~ 3 000 μm)的颞侧、上方、鼻侧、下方的4等分区域,6~9依次为外环(直径3 000~6 000 μm)的颞侧、上方、鼻侧、下方的4等分区域[2],分区见图 1。
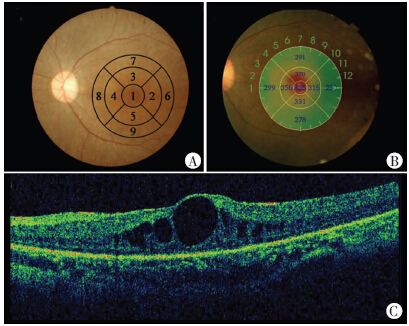 |
| A:黄斑区分区,以中心凹中心为圆心显示为9个区域,依次编号为1~9,1为黄斑中心凹(1区)(直径1 000 μm),2~5依次为内环(直径1 000~3 000 μm)的颞侧、上方、鼻侧、下方的4等分区域,6~9依次为外环(直径3 000~6 000 μm)的颞侧、上方、鼻侧、下方的4等分区域;B:黄斑区光学相干断层扫描(OCT)自动生成9个区对应的值;C:与图B对应的黄斑区OCT 图 1 黄斑区分区示意图 |
采用 SPSS 18.0统计软件。计量资料以±表示。各疗效指标[黄斑中心凹(1区)厚度、黄斑1~9区平均厚度及视力]的统计采用重复测量方差分析。 2 结果 2.1 患者基本资料及诊断
本研究共纳入RP黄斑水肿患者10例。患者眼底可见视乳头界清、色淡红,C/D=0.2~0.3,黄斑中心凹光反射弥散,中周部可见骨样细胞色素沉积,周边视网膜粗糙(图 2A);FAF示后极部高荧光环(图 2B);FFA早期(0 ∶22.45)示后极部可见大面积透见荧光,视网膜动脉普遍变细(图 2C),晚期(6 ∶59.63)可见荧光渗漏(图 2D);OCT示IS/OS连接带反射不清,黄斑水肿(图 2E);FERG显示5项反应均呈熄灭型;mfERG均呈熄灭型。
 |
| A:眼底彩照示视乳头界清、色淡红,C/D=0.2~0.3,黄斑中心凹光反射弥散,中周部可见骨样细胞色素沉积;B:眼底自发荧光(FAF)示后极部高荧光环;C:眼底荧光造影(FFA)早期(0 ∶22.45)示后极部可见大面积透见荧光,视网膜动脉普遍变细;D:FFA 晚期(6 ∶59.63)可见荧光渗漏;E:巩膜后注射曲安奈德前后黄斑水肿的比较,术前黄斑水肿明显,术后1周水肿减轻,术后1个月基本正常 图 2 视网膜色素变性黄斑水肿患者的眼科影像学表现 |
OCT检查结果显示患者术后黄斑中心凹(1区)厚度及黄斑1~9区平均厚度均明显下降(图 2E),以术后1个月最为明显。对黄斑中心凹(1区)厚度的统计学分析提示,主体内效应的差异有统计学意义(P=0.042),即治疗前后的黄斑中心凹(1区)厚度存在显著差异。与术前相比,术后1个月黄斑中心凹(1区)厚度明显下降[(279.6±130.5)μm vs(358.4±152.2)μm,P=0.023];术后1周[(298.7±146.2)μm] 较术前虽呈现下降趋势,但差异尚无统计学意义(P=0.073)。对黄斑1~9区平均厚度的统 计学分析提示,主体内效应的差异有统计学意义(P=0.005),即治疗前后的黄斑1~9区平均厚度存在显著差异。与术前相比,黄斑1~9区 平均厚度术后1周[(284.3±76.8)μm vs (301.9±83.3)μm,P=0.047]、 术后1个月[(271.9± 68.7)μm vs (301.9±83.3)μm,P=0.011]均有明显下降。提示黄斑1~9区平均厚度可作为观察疗效更为敏感的指标。 2.3 术后视力的变化
术后1周、1个月视力虽较术前分别提高2个 [(45.4±19.0) vs (43.4±18.7)个]和6个[(49.8± 20.1) vs (43.4±18.7)个]字母数,但主体内效应的差异尚无统计学意义(P=0.085)。 2.4 术后并发症
所有患者均完成术后1个月的随访。10例患者术后均未发生结膜出血、高眼压、感染等术后并发症。 3 讨论
视网膜变性疾病出现黄斑水肿有各种病理学方面的推测:RP患者出现黄斑水肿被认为与血-视网膜屏障(blood-retinal barrier,BRB)破坏[3]和切向玻璃体牵拉[4]有关。目前研究把RP黄斑水肿的病理机制再一次聚焦到炎症反应这一可能因素上,认为此类患者内层BRB和外层BRB的渗透性均增高[3],同时炎症细胞渗入到RP患者玻璃体腔内。皮质类固醇通过抑制炎症细胞增殖、迁移,减少炎症因子的合成和释放[5]。TA是人工合成的长效糖皮质激素,糖皮质激素可以通过花生四烯酸途径减少前列腺素的释放,稳定血管内皮屏障,同时具有抑制炎症,稳定BRB状态,降低血管渗透性,并且可以下调VEGF的表达,成为治疗黄斑水肿的药物[6, 7]。注药方式分为:①玻璃体腔注射TA:近年来将玻璃体腔注射TA治疗糖尿病、视网膜静脉阻塞、葡萄膜炎等各种原因所致的黄斑水肿,可以在较短时间内使黄斑水肿减轻或消退[8],但并发症较多。由于眼内小梁网组织存在激素受体,TA是一种人工合成激素,与小梁网激素受体结合后可引起房水流出阻力增高,出现高眼压甚至导致青光眼损害。国外报道玻璃体腔注射TA后约20%~40%患者会出现眼压升高,约30%出现白内障[9]。②后腾氏囊注射TA:国外也有将TA后腾氏囊注射治疗黄斑水肿的观察报道[10],TA后腾氏囊注射可以使药物在球后长期维持稳定的有效治疗量。对一些黄斑水肿较轻、时间较短的患者可考虑TA后腾氏囊注射治疗,注射剂量为20~40 mg,并可反复注射,间隔时间为18 d(TA的半衰期)。但后腾氏囊注射有刺破眼球的风险[11],并且由于注射部位距离黄斑较远,效果有限。③玻璃体腔注射雷珠单抗,可降低血管渗透性,减轻黄斑水肿[12]。近年来,有关抗VEGF类药物取得了一定的研究成果,但同时在给药剂量、重复药次数、适应证、远期效果等方面尚存在一些争议[13]。但该药物价格很高,玻璃体腔注射也有眼内感染、白内障、出血的风险[14],同时该药物价格昂贵,带来较重的家庭和社会经济负担。
因此,我们开展巩膜后注射TA来治疗黄斑水肿。通过一种特殊设计的器械和方法,经过颞上方结膜的微创小切口将药物直接注射到黄斑后面的巩膜外,由于不进入眼球内的玻璃体腔,大大降低了刺破眼球、高眼压和眼内感染的风险;经过颞上方结膜的微创小切口进针可以避免伤及眼外肌;同时由于药物直接注射到黄斑后面,巩膜外的筋膜囊起到限制药物在局部的作用,对于黄斑水肿有直接的疗效。本研究采用的“巩膜后”是有别于“球后”的不同器械和方法,球后注射采用的是锋利的直针头,患者向鼻上方注视,在眶下缘中外1/3与内2/3交界处将针头直刺入皮肤,约 1~2 cm,随后沿眶壁走行向内上方倾斜30度,再进针到3~3.5 cm回抽针管如无回血可缓缓注入药液,该方法注射的药物在球后的筋膜囊,离黄斑区较远,疗效较差,同时有刺破眼球及损伤下直肌的风险。虽然先前的实验表明,巩膜的通透极限的相对分子质量是70×103[15],但最近的研究却表明相对分子质量为150×103的白蛋白分子也能够通过巩膜[16],而TA的相对分子质量为434.5,极易通过。该方法简便易学、既能降低治疗的风险及成本,又可以获得较好的治疗效果。本研究发现黄斑中心凹(1区)厚度以及黄斑1~9区平均厚度均在术后1个月下降更为明显,提示巩膜后注射TA疗效的高峰在术后1个月。黄斑1~9区平均厚度在术后1周及1个月均有明显差异,提示黄斑1~9区平均厚度可作为观察疗效更为敏感的指标,同时有些患者的水肿并非均在中心凹,需重视黄斑区的平均厚度。由于黄斑水肿会破坏RP患者感光细胞内节/外节(IS/OS)连接带,故影响黄斑中心凹功能,直接导致视力下降[17]。本研究发现患者术后视力较术前虽有提高,但差异无统计学意义,提示黄斑水肿减轻,但IS/OS连接带的修复尚需一定时间。
本研究结果显示,巩膜后注射TA可用于治疗RP患者的黄斑水肿,1个月随访疗效较稳定,能有效改善患者黄斑水肿的症状,而且手术较安全。本研究提示术后需重视随访,不足之处在于病例数少,随访时间短,需进一步扩大病例数,并对远期效果进行更加深入的研究。
| [1] | Walia S, Fishman G A, Hajali M. Prevalence of cystic macular lesions in patients with Usher II syndrome [J]. Eye (Lond), 2009, 23(5): 1206-1209. |
| [2] | 李世迎, 王一, 阴正勤, 等. 高度近视眼黄斑视网膜神经上皮层厚度的OCT测量[J]. 第三军医大学学报, 2004, 26(5): 419-422. |
| [3] | Larsen M, Engler C B, Haim M,et al. Bloodretina barrier permeability is independent of trace substance lipid solubility in retinitis pigmentosa and in the healthy eye [J]. Int Ophthalmol, 1997, 21(4): 229-234. |
| [4] | Takezawa M, Tetsuka S, Kakehashi A. Tangential vitreous traction: a possible mechanism of development of cystoid macular edema in retinitis pigmentosa [J]. Clin Ophthalmol, 2011, 5: 245-248. |
| [5] | Jonas J B, Hayler J K, Sofker A,et al. Intravitreal injection of crystalline cortisone as adjunctive treatment of proliferative diabetic retinopathy [J]. Am J Ophthalmol, 2001, 131(4): 468-471. |
| [6] | Ip M S, Gottlieb J L, Kahana A,et al. Intravitreal triamcinolone for the treatment of macular edema associated with central retinal vein occlusion [J]. Arch Ophthalmol, 2004, 122(8): 1131-1136. |
| [7] | Saraiva V S, Sallum J M, Farah M E. Treatment of cystoid macular edema related to retinitis pigmentosa with intravitreal triamcinolone acetonide [J]. Ophthalmic Surg Lasers Imaging, 2003, 34(5): 398-400. |
| [8] | Martidis A, Duker J S, Greenberg P B,et al. Intravitreal triamcinolone for refractory diabetic macular edema [J]. Ophthalmology, 2002, 109(5): 920-927. |
| [9] | Jonas J B. Intravitreal triamcinolone acetonide: a change in a paradigm [J]. Ophthalmic Res, 2006, 38(4): 218-245. |
| [10] | Koga T, Mawatari Y, Inumaru J,et al. TransTenon’s retrobulbar triamcinolone acetonide infusion for refractory diabetic macular edema after vitrectomy [J]. Graefes Arch Clin Exp Ophthalmol, 2005, 243(12): 1247-1252. |
| [11] | Lin J M, Chiu Y T, Hung P T,et al. Early treatment of severe cystoid macular edema in central retinal vein occlusion with posterior subtenon triamcinolone acetonide [J]. Retina, 2007, 27(2): 180-189. |
| [12] | Pieramici D J, Rabena M, Castellarin A A,et al. Ranibizumab for the treatment of macular edema associated with perfused central retinal vein occlusions [J]. Ophthalmology, 2008, 115(10): e47-e54. |
| [13] | Shahsuvaryan M L. Therapeutic potential of intravitreal pharmacotherapy in retinal vein occlusion [J]. Int J Ophthalmol, 2012, 5(6): 759-770. |
| [14] | Ding X, Li J, Hu X,et al. Prospective study of intravitreal triamcinolone acetonide versus bevacizumab for macular edema secondary to central retinal vein occlusion [J]. Retina, 2011, 31(5): 838-845. |
| [15] | Filippatos T D, Athyros V G, Elisaf M S. The pharmacokinetic considerations and adverse effects of DPP4 inhibitors [corrected] [J]. Expert Opin Drug Metab Toxicol, 2014, 10(6): 787-812. |
| [16] | Ambati J, Gragoudas E S, Miller J W,et al. Transscleral delivery of bioactive protein to the choroid and retina [J]. Invest Ophthalmol Vis Sci, 2000, 41(5): 1186-1191. |
| [17] | Kim Y J, Joe S G, Lee D H,et al. Correlations between spectraldomain OCT measurements and visual acuity in cystoid macular edema associated with retinitis pigmentosa [J]. Invest Ophthalmol Vis Sci, 2013, 54(2): 1303-1309. |



