双能量CT心肌灌注扫描可同时实现冠状动脉血管造影(CTA)和心肌碘灌注成像,是目前能结合SPECT核素心肌显像和冠状动脉DSA的优势于一体的“一站式”成像技术[1, 2, 3]。较传统单源CT,双源CT能有效减少定位不准和运动伪影,但上腔静脉及心腔内对比剂残余、浓度不均及金属支架等因素,导致组织不均匀吸收低能量光子而产生X线束硬化伪影(beam-hardening,BH)[4, 5]。BH在心肌碘灌注图上表现为与缺血心肌类似的灌注缺损。目前的研究表明二者较难区分,但伪影可通过单能量成像来消除[6, 7]。
双能量CT成像技术主要有两大优势功能:物质成分分析和线束硬化伪影矫正[6]。高、低双球管发出的混合能量X射线可按任意混合比模拟生成40~190 keV的单色能量图像,纯化的X射线能有效减少能量的不均匀吸收,纠正线束硬化伪影[7, 8]。国内外对CT心肌灌注成像的单能量图像质量方面研究不多,更多集中于研究纠正金属线束硬化伪影[8, 9, 10]。由于不同组织有选择性吸收单能量射线的特点[11, 12],本研究通过观察线束硬化伪影的好发部位及不同单能量对其进行纠正的效果,寻找图像线束硬化伪影发生率低并能以最佳图像质量显示心肌的单能量。
1 资料与方法 1.1 临床资料连续对84例(男性57例,女性27)拟诊或确诊冠心病的患者进行双源双能量CT心肌灌注扫描。纳入标准:患者屏气功能良好,心律平稳,心率<80/min,一次屏气后心率波动<5/min,肝、肾功能良好,无碘对比剂过敏及妊娠。患者均以心前区不适为主要临床表现(排除呼吸道、消化道疾病的影响),年龄44~61岁,体质量指数20.42~23.83 kg/m2。84例患者均行动态心电图和超声心动图检查,动态心电图未见明显S-T段压低或抬高的心肌缺血指征,左心室射血分数56%~78%,其中12例1年内曾行冠脉DSA,6例曾行SPECT核素心肌显像。
1.2 检查方法患者检查前静坐30 min自然降低心率,期间告之注意事项并签署知情同意书。做好呼吸训练,检查前数分钟给予扩张冠脉的硝酸甘油1片舌下含服。钙化积分、小剂量Bolus-tracking后根据达峰时间计算扫描延迟时间,进行双能量CT心肌灌注扫描。
扫描参数:使用Siemens公司Somatom Definition Flash Dual-source CT,双能量CT心肌灌注扫描模式:低、高能球管管电压(100 kVp/Sn 140 kVp),Sn:锡板,回顾性心电门控,管电流依心率自动调节,参考范围:0~300 mAs,准直器宽度32×2×0.6 mm,旋转速度0.33 s/r,螺距:0.2~0.3(心率自适应),单幅图像矩阵512×512。
对比剂方案:非离子型对比剂碘普罗胺(370 mg/mL),总量:50~70 mL,注射流率:4~5 mL/s(据血管弹性及通畅度选择),MEDRAD双筒高压注射器(型号:Stellant D),经右侧肘静脉行三期持续注射:一期为纯对比剂35~50 mL,完成冠脉血管造影;二期为混合液40~80 mL(对比剂:生理盐水=3 ∶7)[1, 13],持续灌注心肌;三期为纯生理盐水40~50 mL,冲淡残余对比剂。
1.3 图像后处理低、高能量混合权重因子0.5,自动生成的混合M图像等效于混合能量120 kV[12, 14];重建最佳舒张期(冠状动脉CTA成像)和最佳收缩期(心肌灌注显像)的薄层图像,层厚0.75 mm,层间距0.5 mm,卷积核:血管CTA用B26f,心肌灌注用D30f[1, 2]。数据传送至Siemens MMWP工作站,应用Circulation、Inspace处理最佳舒张期图像,最大密度投影(MIP)和容积再现(VR)重组冠状动脉。
在心肌碘分布图上按照美国心脏协会(AHA)标准将心肌在左室短轴位划分为17段,以层厚3 mm,ROI为20~30 mm2的感兴趣区测量伪影段和左室中间段外侧壁非伪影段的心肌碘含量;分别在Monoenergy模式的65、75、85、95、105 keV及120 kV下测量同一ROI的CT值(HU)及其标准偏差,并测量左心室中心CT值作为对比;测量六组能量级的胸骨前皮下脂肪的CT值偏差作为图像背景噪声(SD),计算非伪影心肌的信噪比(signal noise ratio,SNR)和对 比噪声比(contrast noise ratio,CNR),SNR=CT心肌/SD,CNR=(CT心肌-CT左心室)/SD,取绝对值。
1.4 图像质量评价由两位高级影像诊断医师分别对六种能量的图像进行随机评分,窗宽600 HU,窗位200 HU。根据伪影严重程度、心肌均匀性、对比度和诊断价值等对图像质量进行评分。采用0~5分法:无法诊断为0分;有伪影、心肌密度不均噪声大、严重影响诊断为1分;有伪影、心肌密度不均中度影响诊断为2分;有伪影、心肌密度不均轻度影响诊断为3分;有伪影心肌密度均匀不影响诊断为4分;无伪影、心肌密度均匀满意诊断为5分。
1.5 统计学分析采用IBM SPSS 20.0统计软件,校正性别、年龄、体质量指数、心率、左室射血分数等基础情况的影响,计量资料以x±s表示,多组计量资料的差异性检验选用单因素方差分析,两两比较用LSD-t法;不符合计量资料分析要求者,选用非参数检验,等级资料选择秩和检验。对两位高级诊断医师的主观评价做Kappa分析。检验水准α=0.05。
2 结果 2.1 一般情况84例患者的资料服从正态分布,年龄(56.73±10.42)岁,心率(70.5±8.09)/min,体质量指数(22.81±2.57)kg/m2,综合冠状动脉CTA和DSA、SPECT心肌核素显像的结果:61例患者的冠状动脉存在不同程度迂曲,50例患者1~2支主干存在轻到中度狭窄,42例患者散在1~3处钙化,其管腔轻到中度狭窄,6例患者存在弥漫性钙化及中度狭窄,3例患者心尖部及前壁散在不规则小缺血灶。
2.2 伪影部位及数量统计84例患者的平均对比剂用量为(63.81±8.47)mL,对比剂用量分组统计:<55 mL共27例,伪影率18.4%,55~65 mL共24例,伪影率37.89%,>65 mL共33例,伪影率43.71%(P<0.05);BH的分布情况及数量(表 1):65 keV>75 keV>105 keV>120 kV>95 keV>85 keV(P<0.05);在伪影最明显的65 keV下观察BH:基底段36.5%(100/274),上腔静脉旁段24.82%(68/274),间隔壁25.91%(71/274),后壁12.77%(35/274),各部位BH发生率差异有统计学意义(P<0.05)。
| 部位 | 65 keV | 75 keV | 85 keV | 95 keV | 105 keV | 混合能量 120 kV |
| 基底段 | 100 | 93 | 78 | 81 | 88 | 86 |
| 上腔静脉旁段 | 68 | 63 | 57 | 57 | 64 | 60 |
| 间隔壁 | 71 | 64 | 54 | 55 | 60 | 59 |
| 后壁 | 35 | 26 | 18 | 18 | 23 | 20 |
| 合计 | 274 | 246 | 207 | 211 | 235 | 225 |
伪影区心肌碘含量(-2.37±0.84)mg/g,类似缺血心肌的碘灌注图像(图 1A),非伪影区心肌碘含量 (3.5±0.92)mg/g(表 2),二者有明显差异(t=-19.36,P<0.01),伪影的碘灌注缺损在SPECT核素心肌显像上灌注均匀(图 1B);同一能量下伪影与非伪影心肌CT值差异有统计学意义(P<0.05);观察单能量与混合能量图像(表 2、图 2)可见,65~105 keV,伪影心肌CT值逐渐增加,非伪影心肌CT值逐渐降低,85 keV与120 kV的心肌CT值最接近(表 2),各组CT值差异有统计学意义(P<0.01);85 keV的SD最低(t=32.27,P<0.01),各组SD差异有统计学意义(P<0.01);75 keV与85 keV的SNR较高,二者无明显差别(t=1.5,P=0.14),75 keV 的CNR最高(t=25.47,P<0.01),CNR曲线走形均在75 keV达到峰值(图 1C),85 keV与65 keV 的CNR之间无明显差别(t=0.27,P=0.79),其余各组SNR、CNR差异有统计学意义(P<0.01);较优的85 keV与120 kV比较,85 keV的线束硬化伪影数较少,SD85
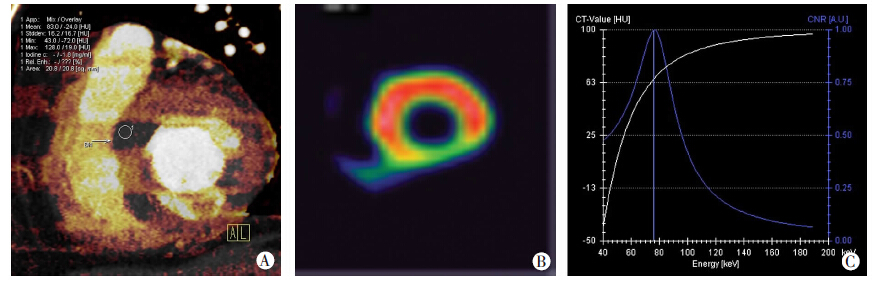 |
| A:心肌碘图左心室短轴位上的横带状的线束硬化伪影(↑)在上腔静脉及右心房两边的心肌对称分布;B:心肌核素显像提示图A的低灌注区无心肌缺血;C:线束硬化伪影的CNR曲线(蓝色)及CT值曲线(白色) CNR在75 keV达到峰值,伪影的CT值从40~190 keV逐渐增加图 1 CT心肌碘分布、SPECT核素心肌显像对照图及伪影的CNR曲线 |
| 指标 | 65 keV | 75 keV | 85 keV | 95 keV | 105 keV | 混合能量120 kV |
| CT无伪影(HU) | 149.10±35.06 | 114.06±23.74 | 93.52±18.52 | 79.98±21.01 | 70.41±22.03 | 96.06±16.32 |
| CT伪影(HU) | 52.36±22.04 | 78.52±20.33 | 85.41±19.73 | 90.02±20.37 | 101.90±21.65 | 82.32±13.11 |
| SD | 21.60±5.16 | 14.07±3.48 | 12.98±3.16 | 16.14±4.31 | 18.99±5.01 | 15.75±3.49 |
| SNR | 5.72±1.56 | 6.89±1.79 | 6.50±1.70 | 4.47±1.35 | 3.27±0.99 | 5.82±1.63 |
| CNR | 15.53±4.56 | 18.79±6.76 | 15.40±5.67 | 10.15±4.48 | 4.94±3.03 | 18.28±6.61 |
 |
| A:65 keV;B:75 keV;C:85 keV;D:95 keV;E:105 keV;F:混合能量120 kV ↑:线束硬化伪影图 2 单能量图和混合能量图像 |
两名医师随机对六种能量的图像进行评分,85 keV 得分最高,均认为65~105 keV密度分辨率逐渐下降,85 keV组织均匀性好,图像细腻,与周围组织的对比度强,能较好地满足诊断要求,主观评价的结果高度一致(Kappa=0.79,P<0.01)。
3 讨论近年来,在心血管影像领域,静息状态下的双能量CT心肌灌注成像逐渐成为国内外学者研究的热点,其临床价值在于“一站式成像”可同时了解冠状动脉和心肌血供情况,为缺血心肌找到责任血管。它对冠心病的诊断准确性与SPECT核素心肌显像、冠脉DSA、磁共振心脏成像相比,吻合率可达到80%以上[1, 2, 3]。但同时完成上述两项检查需要持续注入浓度不等的对比剂维持灌注,且心肌为运动器官,导致图像易出现X线束硬化伪影(BH)[4, 5]。BH和缺血、梗死心肌的灌注缺损表现类似,二者难以区分,可能增加诊断的假阳性率。目前国内外对双能量CT心肌灌注的单能量成像研究还在初期,多项研究[6, 7, 8, 9, 10]表明最佳单能量成像可消除伪影并实现目标组织的优化成像,在该技术逐渐成熟的情况下,我们希望找到CT心肌灌注的最佳单能量成像。
本研究中84例患者均扫描成功,结合其他辅助检查,排除了心肌严重缺血。左心室短轴位的碘分布图上,观察到BH常表现为横带状、边界清晰、上下边缘平行的“刀切样”的低灌注区,在上腔静脉或左心室左右对称分布,穿透整个心肌层,类似缺血心肌的灌注缺损灶,但心肌缺血灶的形态多不规则,边界不清,分布无规律性,国外文献报道的BH特点为带状、透壁性,心肌高密度区的低强化灶[3, 4]。因射线被衰减的严重程度不同,伪影区心肌的碘含量从负到正,变化范围较广,但都比周围正常心肌低。正常情况下,碘随血液的流动均匀分布在被增强的组织中,碘吸收不同能量的X射线后,根据其在物质中不同的衰减系数转换为相对碘浓度和CT值,并进行数字化伪彩编码,转换为碘分布图。和SPECT核素心肌显像的图一样,色彩明亮、均匀的区域代表组织血供丰富,色彩暗沉、不均的区域代表组织缺血,故碘分布图能间接反映组织的血流灌注情况。线束硬化伪影与心肌缺血的碘含量较低,但二者的形成机制不同,伪影的“低碘”是因为X射线被不均匀衰减,即使碘含量丰富的心肌也无法吸收足够的射线转换为其实际碘含量,而缺血心肌的“低碘”是因为心肌血供的缺乏导致实际碘含量不足[5, 15]。若因某些因素导致组织不能均匀吸收X射线影响碘含量换算,产生图像失真(如线束硬化伪影),则即使是碘分布均匀的组织,也表现出灌注缺损[3, 4, 9, 10]。
碘图上难以区别的BH与缺血心肌,除了形态区别外,主要通过单能量成像来纠正伪影[16]。首先,本研究显示左心室基底段的BH发生率特别高,其中又以上腔静脉旁段(S2/3)最明显,与Rodriguez-Granillo等[14]提示的基底段后壁常出现BH一致。基底段的组织种类较多,有脂肪、心肌和其他结缔组织,形态结构欠均匀,均导致X射线被不均匀吸收,故易出现BH。其次,伪影较多的为左心室间隔壁,主要与上腔静脉及左心室内高浓度对比剂残留有关,而浓度不均更易导致BH。Secchi等[4]研究提到此现象:室间隔位于左右心室之间,心室腔内的对比剂导致X射线在横行穿过左、右心室侧壁和心腔时被大量吸收衰减。我们观察左心室中间段和心尖段,左心室后壁也常发生BH,与文献[11, 14]的结果一致。我们分组统计了对比剂用量与BH发生率的关系,结果提示在对比剂的用量方面,应以尽量保持上腔静脉及右心室无残留为原则,减少BH的发生。
国外研究表明,纠正BH的最佳单能量在70~120 keV 之间[7, 8, 9, 10]。系统自动生成的CNR曲线均在75 keV达到峰值,同时为保证能级跨度均匀,我们以10 keV为间隔选取了实验中的5组单能量。随着单能量级的增加,正常心肌的CT值逐渐降低,伪影区心肌密度逐渐增高,与国外研究[8, 9, 10]一致。在85 keV 的正常心肌CT值为(93.52±18.52)HU,研究也提示的正常成人静息态下最佳收缩期的心肌密度为92~98 HU,85 keV与120 kV的心肌密度最接近,后壁基底段的心肌密度容易受到线束硬化伪影的影响,比正常密度低[14, 17],故85 keV是5组单能量中最能真实反映心肌密度的能级。Wu等[8]研究发现,单能量图像与120 kV图像显示的线束硬化伪影密度和数量有差别,前者可减少BH导致的灌注缺损假阳性病灶。不同原子序数的物质与X射线发生光电效应和康普顿效应后,吸收的能量不同,双能量CT的单能量成像技术基于组织的这种特征也可生成能谱曲线,寻找到对比度最佳的特征单能量[6, 11, 18]。
我们观察到65~105 keV,BH逐渐淡化,在85 keV 时BH几乎消失,伪影区密度与周围正常心肌一致,在上升到105 keV的过程中伪影又逐渐明显。Hemmingsson等[12]报道单能量较混合能量图像能有效减少BH 60%~90%,显示软组织较好、图像噪声水平较低的单能量出现在70~80 keV附近。因我们选择的能级不同,85 keV与80 keV的噪声差别有待进一步研究。比较图像的CNR可见,心肌成像的最佳条件为75 keV和85 keV,但75 keV的噪声较高,伪影较85 keV 明显,故图像质量不及后者。研究显示,随着单能量的逐渐增加,BH会逐渐淡化,CNR会逐渐降低,CNR峰值出现在70~80 keV之间[4, 19],与我们的实验结果吻合。Meinel等[10]发现接近120 keV的单能量图像组织对比度会下降,我们在从65 keV移动到105 keV的过程中也发现,心肌与周围组织的密度对比度下降,但图像颗粒感不明显。主观评价者对图像质量的评价认为,85 keV图像的假阳性率最低,图像失真度小,能满足诊断。
综上所述,双源双能量CT心肌灌注成像的线束硬化伪影主要发生在左心室基底段、上腔静脉旁及间隔壁,综合伪影数量和图像质量来看,85 keV能在有效纠正BH的同时提高图像质量,突现了双能量CT心肌单能量成像的优势。因鉴别点不明显,对拟诊心肌缺血的部位还需结合单能量和混合能量图像共同观察。本实验不足在于能级跨度不够深入,75~95 keV之间是否还有图像质量更好的能级还有待研究,而对比剂的准确量化、伪影与缺血的鉴别特点应是单能量成像在去除伪影的优势方面研究的新方向。
| [1] | Schwarz F, Ruzsics B, Schoepf U J, et al. Dual-energy CT of the heart--principles and protocols[J]. Eur J Radiol, 2008, 68(3): 423-433. |
| [2] | 齐燕, 齐双, 欧陕兴. 双源CT在心脏成像中的应用研究[J]. 心脏杂志, 2010, 22(2): 302-304. |
| [3] | Peng J, Zhang L J, Schoepf U, et al. Acute myocardial infarct detection with dual energy CT: correlation with single photon emission computed tomography myocardial scintigraphy in a canine model[J]. Acta Radiol, 2013, 54(3): 259-266. |
| [4] | Secchi F, De-Cecco C N, Spearman J V, et al. Monoenergetic extrapolation of cardiac dual energy CT for artifact reduction[J]. Acta Radiol, 2015, 56(4): 413-418. |
| [5] | Yamada M, Jinzaki M, Kuribayashi S, et al. Beam-hardening correction for virtual monochromatic imaging of myocardial perfusion via fast-switching dual-kVp 64-slice computed tomography: a pilot study using a human heart specimen[J]. Circ J, 2012, 76(7): 1799-1801. |
| [6] | 王未, 周长圣, 方晓堃, 等. 第二代双源双能量CT心肌灌注成像的初步应用[J]. 放射学实践, 2014, 29(9): 993-997. |
| [7] | Mangold S, Gatidis S, Luz O, et al. Single-source dual-energy computed tomography: use of monoenergetic extrapolation for a reduction of metal artifacts[J]. Invest Radiol, 2014, 49(12): 788-793. |
| [8] | Wu X, Langan D A, Xu D, et al. Monocromatic CT image representation via fast switching dual kVp[J]. Proc SPIE, 2009, 7258: 725845. |
| [9] | Guggenberger R, Winklhofer S, Osterhoff G, et al. Metallic artifact reduction with monoenergetic dual-energy CT: systematic ex vivo evaluation of posterior spinal fusion implants from various vendors and different spine levels[J]. Eur Radiol, 2012, 22(11): 2357-2364. |
| [10] | Meinel F G, Bischoff B, Zhang Q, et al. Metal artifact reduction by dual-energy computed tomography using energetic extrapolation: a systematically optimized protocol[J]. Invest Radiol, 2012, 47(7): 406-414. |
| [11] | Okayama S, Seno A, Soeda T, et al. Optimization of energy level for coronary angiography with dual-energy and dual-source computed tomography[J]. Int J Cardiovasc Imaging, 2012, 28(4): 901-909. |
| [12] | Hemmingsson A, Jung B, Ytterbergh C. Dual energy computed tomography: simulated monoenergetic and material-selective imaging[J]. J Comput Assist Tomogr, 1986, 10(3): 490-499. |
| [13] | Vliegenthart R, Pelgrim G J, Ebersberger U, et al. Dual-energy CT of the heart[J]. AJR Am J Roentgenol, 2012, 199(5 Suppl): S54-S63. |
| [14] | Rodriguez-Granillo G A, Rosales M A, Degrossi E, et al. Signal density of left ventricular myocardial segments and impact of beam hardening artifact: implication for myocardial perfusion assessment by multidetector CT coronary angiography[J]. Int J Cardiovasc Imaging, 2010, 26(3): 345-354. |
| [15] | Koonce J D, Vliegenthart R, Schoepf U J, et al. Accuracy of dual-energy computed tomography for the measurement of iodine concentration using cardiac CT protocols: validation in a phantom model[J]. Eur Radiol, 2014, 24(2): 512-518. |
| [16] | 任庆国, 滑炎卿, 李剑颖. CT能谱成像的基本原理及临床应用[J]. 国际医学放射学杂志, 2011, 34(6): 559-563. |
| [17] | Stanton C L, Haramati L B, Berko N S, et al. Normal myocardial perfusion on 64-detector resting cardiac CT[J]. J Cardiovasc Comput Tomogr, 2011, 5(1): 52-60. |
| [18] | Wang X, Meier D, Taguchi K, et al. Material separation in x-ray CT with energy resolved photon-counting detectors[J]. Med Phys, 2011, 38(3): 1534-1546. |
| [19] | Lewis M, Reid K, Toms A P. Reducing the effects of metal artefact using high keV monoenergetic reconstruction of dual energy CT (DECT) in hip replacements[J]. Skeletal Radiol, 2013, 42(2): 275-282. |



