脉络膜新生血管(choroidal noevascularization,CNV)参与多种眼底疾病的发生,如年龄相关性黄斑变性、特发性脉络膜视网膜炎等,是目前致盲的最重要因素之一,且发病率近年有所增长。尽管CNV形成的研究不断进展,但其发病机制极其复杂,至今尚不完全明确。近年研究发现神经轴突导向因子slit2参与新生血管形成[1, 2]。slit2是一种分泌型糖化蛋白,主要分布在肺、肾、神经、实体肿瘤等,参与血管新生、细胞迁移,调节肿瘤的增殖、凋亡,调控白细胞趋化等[3]。但slit2是否也参与CNV形成的研究尚少见报道。本课题组前期研究证明沉默视网膜色素上皮细胞(RPE)中的slit2基因,可使缺氧诱导的血管内皮生长因子(VEGF)降低,而后者是促进CNV形成的重要因子,因此认为slit2可能参与CNV的形成[4]。本实验利用腺病毒转染技术,使RPE细胞中slit2基因过表达,观察过表达slit2的RPE细胞对猴脉络膜视网膜血管内皮细胞(RF/6A)的迁移及管腔形成的影响,为CNV的治疗提供新的靶点。
1 材料与方法 1.1 实验细胞人视网膜色素上皮细胞ARPE-19细胞系由本课题组提供,RF/6A购自中国上海中科院细胞库。
1.2 实验试剂Ad-slit2、Ad-null(长沙赢润生物技术有限公司),RPMI1640培养基、胎牛血清(FBS)、胰酶(美国Gibco公司),磷酸盐缓冲溶液(PBS)、青霉素-链霉素混合液、SDS-PAGE制胶试剂盒、SDS上样缓冲液(中国碧云天公司),RT-PCR试剂盒、Prime ScriptTM RT reagent kit、SYBR Premix Ex TapTM Ⅱ(日本TaKaRa公司),ELISA试剂盒、山羊抗兔抗体(武汉博士德公司),兔抗人slit2抗体(美国Abcam公司),兔抗人VEGF抗体(美国Immunoway公司),Matrigel胶(美国BD公司),Transwell小室(美国Corning公司)等。
1.3 细胞培养RPE细胞及RF/6A细胞均用含10% FBS、1%青霉素-链霉素混合液的RPMI1640培养基,置于37 ℃,5% CO2条件下的孵箱内培养。按细胞传代方法,将RPE细胞消化成悬浮状体,种于6孔板或24孔板中,分成3组:空白对照组、Ad-null转染组、Ad-slit2转染组。待其贴壁成对数成长时,按1 ∶1 000的比例分别将Ad-slit2、Ad-null分别加入孔内的培养基中,将板置于孵箱内,孵育24 h及48 h后收集细胞做检测。
1.4 RT-PCR检测按RT-PCR试剂盒说明,提取各组细胞总mRNA,并逆转录为cDNA。slit2上游引物5′-GGGCATTTGAT-ACTCCATTC-3′,下游引物 5′-TCTTCTTTCTCAGCCAC-TCTCC-3′,104 bp;VEGF上游引物5′-GAGTACATCTTCAAGCCATCCTG-3′,下游引物5′-TGCTCTATCTTTC-TTTGGTCTGC-3′,204 bp;β-actin上游引物5′-GTGAT-CTCCTTCTGCATCCTGT-3′,下游引物 5′-CCACGAAAcTACCTTCAACTCC-3′,132 bp。引物由上海生工生物工程公司合成。SYBR Premix Ex TapTM Ⅱ实时PCR总反应体系是25 μL:Premix Ex TapTM Ⅱ 12.5 μL、上游引物(10 μmol/L)及下游引物(10 μmol/L)均1 μL、模板2 μL 、无酶DNase 8.5 μL。反应条件:95 ℃预变性30 s,95 ℃变性5 s,60 ℃退火30 s,均扩增40个循环。循环结束后进行产物溶解曲线测定。根据2-△△Ct法计算slit2、VEGF的相对含量。
1.5 Western blot检测收集各组细胞,加入蛋白酶抑制剂和裂解液的混合液(按1 ∶100比例混合),吹打混匀,静置5 min后再次吹打,反复6次后,在4 ℃离心机里离心15 min,吸出上清,即为总蛋白。按BCA蛋白定量试剂盒说明,测量各组总蛋白的浓度。按SDS-PAGE制胶试剂盒的说明配制分离胶和浓缩胶,加样后电泳、转膜、5%脱脂奶粉封闭2 h,孵抗slit2或抗VEGF抗体,4 ℃过夜,洗膜后孵二抗,37 ℃静置2 h,洗膜后曝光显影。
1.6 ELISA检测收集各组细胞的上清培养基,离心后去沉淀取上清,用样本稀释液按1 ∶1稀释上清备用。按照人VEGF ELISA试剂盒说明操作,检测标准品及各组光密度值。根据标准曲线,计算各组VEGF的含量。
1.7 迁移实验(Transwell小室法)将1×105/mL的RPE细胞种于24孔板中,加入600 μL培养基,待其呈对数生长期时,加入Ad-slit2、Ad-null,转染24、48 h后,将种有密度为1×104/mL RF/6A细胞的Transwell小室(孔径为8.0 μm)放入孔中,建立共培养模式,在37 ℃、5% CO2条件下孵育48 h后,取出小室,用棉签将小室上层细胞擦掉,用 5%多聚甲醛 固定15 min,再用1%结晶紫染色15 min,在显微镜下观察并随机取5个视野照相,计算每一视野下RF/6A细胞的迁移数目。
1.8 管腔形成实验(Matrigel胶体外三维成型法)将1×104/mL RPE细胞种于Transwell小室(孔径为0.4 μm)中,加入100 μL培养基,细胞贴壁后加入Ad-slit2及Ad-null,转染24、48 h后备用。按1 ∶1将Matrigel胶和RPMI1640培养基混合均匀,加入24孔板中,每孔加200 μL,置于37 ℃的孵箱1 h,基质胶凝固。将1×105/mL的RF/6A细胞种于各孔的基质胶上,加600 μL培养基。将Transwell小室放入孔中,建立共培养体系,放入37 ℃、5% CO2的孵箱孵育24 h后,取出小室。在显微镜下观察各孔中RF/6A细胞的管腔形成情况,随机选5个视野照相,计算形成管腔个数,并用Image-pro软件计算其管腔形成的总长度。
1.9 统计学分析实验重复至少3次。采用SPSS 17.0统计软件,计量数据用 ±s表示,进行单因素方差分析及t检验。
2 结果 2.1 Ad-slit2转染对RPE细胞slit2 mRNA及蛋白表达的影响RT-PCR结果显示Ad-slit2转染RPE细胞24、48 h后,RPE细胞中slit2 mRNA均较空白对照组表达明显提高,差异具有统计学意义(F=654.11,P < 0.05),而其阴性对照组,即Ad-null转染24、48 h组,较空白对照组无明显变化(P>0.05,图 1A)。Western blot显示Ad-slit2转染24 h及48 h组,RPE细胞中slit2蛋白表达水平比空白对照组明显提高;而阴性对照组均较空白对照组无明显变化(P>0.05,图 1B)。
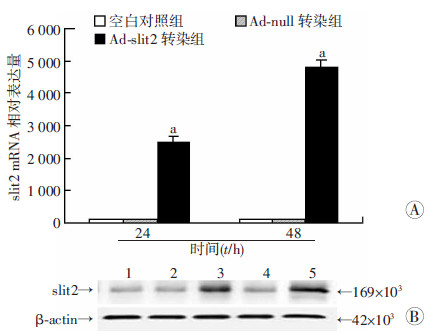 |
| A:各组slit2 mRNA的相对表达量a:P < 0.05,与空白对照组比较;B:各组slit2蛋白表达1:空白对照组;2:Ad-null转染24 h组;3:Ad-slit2转染24 h组;4:Ad-null转染48 h组;5:Ad-slit2转染48 h组 图 1 Ad-slit2转染对RPE细胞slit2 mRNA及蛋白表达的影响 |
RT-PCR结果显示,Ad-slit2转染24 h及48 h组RPE细胞中VEGF mRNA表达量均显著高于空白对照组,差异具有统计学意义(F=66.816,P < 0.05);而阴性对照组,即Ad-null转染24、48 h组,均较空白对照组无明显变化(P>0.05,图 2A)。Western blot结果显示Ad-slit2转染24、48 h后,RPE细胞中VEGF蛋白表达水平均较空白对照组明显提高(图 2B)。
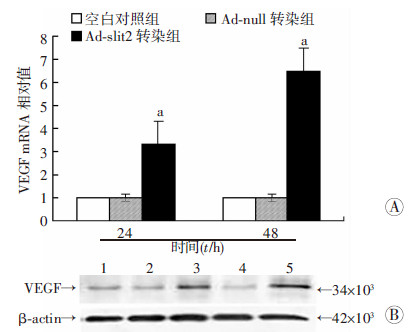 |
| A:各组VEGF mRNA的相对表达量a:P < 0.05,与空白对照组比较;B:各组VEGF蛋白表达1:空白对照组;2:Ad-null转染24 h组;3:Ad-slit2转染24 h组;4:Ad-null转染48 h组;5:Ad-slit2转染48 h组 图 2 Ad-slit2转染对RPE细胞VEGF mRNA及蛋白表达的影响 |
ELISA结果显示Ad-slit2转染于RPE细胞24、48 h后,其培养基上清液中分泌型 VEGF均较空白对照组分泌量增多,差异具有统计学意义(F=30.69,P < 0.05);而Ad-null转染24、48 h组,均较空白对照组无明显变化(P>0.05,图 3)。
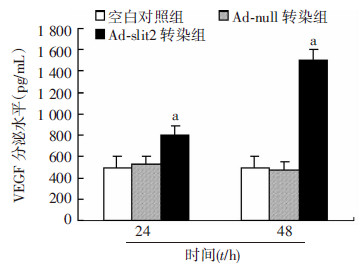 |
| a:P < 0.05,与空白对照组比较 图 3 Ad-slit2转染对RPE细胞培养基上清液内VEGF分泌水平的影响 |
Ad-slit2转染24、48 h后,RPE细胞对RF/6A细胞的迁移数目[(67.7±4.2)、(79.7±3.5)个]均较空白对照组[(40.6±4.5)个]增多,差异具有统计学意义(F=81.16,P < 0.05);而阴性对照组,即Ad-null转染24、48 h组[(36.7±3.5)、(36.0±3.6)个],与空白对照组比较无明显变化(图 4)。
 |
| A:空白对照组;B:Ad-null转染24 h组;C:Ad-slit2转染24 h组;D:Ad-null转染48 h组;E:Ad-slit2转染48 h组 图 4 光学显微镜下观察Ad-slit2转染于RPE细胞对RF/6A细胞迁移数的影响(结晶紫× 200) |
与空白对照组比较,Ad-slit2转染24 h及48 h组,在每一视野下RF/6A细胞形成管腔总长度及管腔数均明显增加,差异具有统计学意义(F=59.66,P < 0.05;F=9.676,P < 0.05);而阴性对照组,即Ad-null转染24、48 h组,均较空白对照组无明显变化(P>0.05,表 1、图 5)。
| 组别 | 管腔长度(mm) | 管腔形成个数 |
| 空白对照组 | 3.95±0.31 | 8.7±3.2 |
| Ad-null转染24 h组 | 4.53±0.26 | 8.9±3.6 |
| Ad-slit2转染24 h组 | 6.04±0.34 a | 15.0±4.2 a |
| Ad-null转染48 h组 | 4.09±0.18 | 8.3±2.4 |
| Ad-slit2转染48 h组 | 7.27±0.45 a | 23.0±4.5 a |
| a:P < 0.05,与空白对照组比较 | ||
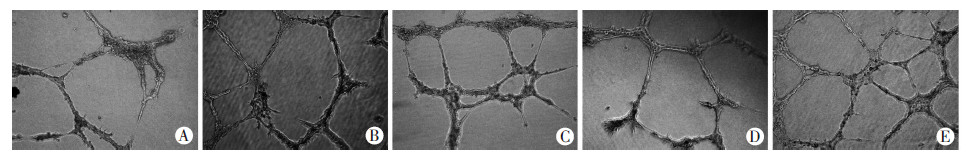 |
| A:空白对照组;B:Ad-null转染24 h组;C:Ad-slit2转染24 h组;D:Ad-null转染48 h组;E:Ad-slit2转染48 h组 图 5 倒置显微镜下观察Ad-slit2转染于RPE细胞对RF/6A细胞管腔形成的影响(× 200) |
slit基因最早于1984年由Nusslein-Volhard等在果蝇的中枢神经系统发现,其家族在脊椎动物中存在 3个亚型,即slit1、slit2、slit3,并有4种受体,即Robo1~ 4[5]。其中slit2与新生血管的发生关系密切,成为时下研究热点。然而slit2对新生血管形成所起的作用存在分歧。Wang等[6]研究发现slit2表达于恶性黑色素瘤细胞,且促进肿瘤诱发的血管形成;Wang等[7]在口腔鳞状细胞癌的研究中也证明了slit2/Robo1在癌变过程中参与激活血管形成,经slit2/Robo1特异性阻断剂R5处理后,肿瘤的血管形成受到抑制。但也有一些研究得到的却是相反的结论,如Han等[8]研究表明slit2参与角膜新生血管的形成,且slit2与robo1及robo4的相互作用抑制角膜新生血管形成;Jones等[9]研究发现通过slit2激活robo4在体外可抑制血管内皮生长因子(VEGF)所诱导的血管形成,在体内可通过阻断Scr家族激酶活化抑制VEGF所刺激的血管渗漏。综上表明,slit2处在不同环境下,对新生血管形成所起作用亦有所不同。
脉络膜新生血管形成的病理基础是脉络膜毛细血管突破bruch膜侵入RPE层,局部血管生成因子和抑制因子动态平衡打破。而目前有关slit2基因在脉络膜新生血管形成中所起作用的研究较少,我们前期研究证明RPE细胞中slit2及Robo1均有表达,且沉默slit2后,Robo1及VEGF的表达也随之减少,初步证实了slit2/robo1可能参与CNV的形成。本实验以猴脉络膜视网膜血管内皮细胞(RF/6A)为研究对象,RF/6A细胞是公认的研究CNV形成的细胞[10, 11]。发现腺病毒介导slit2转染至RPE细胞24、48 h后,RPE细胞中slit2基因均呈过表达状态,将过表达slit2的RPE细胞与RF/6A共培养后,发现其可促进RF/6A的迁移及管腔形成。研究中还发现RPE细胞过表达slit2基因的同时,其VEGF表达量也随之增多,分泌型VEGF蛋白亦随之增加,与我们课题组前期研究结果一致,表明VEGF参与了RPE中slit2基因对RF/6A的作用。Jin等[12]也证明VEGF可促进RF/6A的增殖及管腔形成,其作用机制是通过PI3K/Akt及 MEK/ERK信号通路起作用。因此本实验进一步证实了RPE细胞中的slit2基因参与脉络膜新生血管的形成,从而导致相关疾病的发生。
综上所述,本实验证明过表达slit2的RPE细胞可促进RF/6A细胞的迁移及管腔形成,进而参与了CNV的形成,为其相关疾病提供新的治疗靶点,如湿性老年黄斑变性、病理性脉络膜变性等。但腺病毒介导目前仍局限在实验研究,尚未进入临床试验;除此本实验为体外实验,尚需要进一步完成体内实验的研究加以证明。
| [1] | 孙丽梅, 田连胜, 马红艳, 等. SLIT2在乳腺浸润性导管癌中的表达及意义[J]. 中国组织化学与细胞化学杂志, 2012, 21(4): 377-380. |
| [2] | 余祖滨, 白莉, 高磊, 等. 肺癌组织神经生长导向因子Slit2蛋白表达及其临床意义的研究[J]. 中华肿瘤防治杂志, 2008, 15(12): 901-904. |
| [3] | 李霖, 卿国忠. Slit-Robo信号通路作用的研究进展[J]. 国际病理科学与临床杂志, 2013, 33(1): 72-77. |
| [4] | 黄莉芸, 周希瑗. 腺病毒介导的slit2 shRNA对缺氧诱导的人视网膜色素上皮细胞中血管内皮生长因子表达的影响[J]. 中国生物制品学杂志, 2014, 27(3): 361-365, 371. |
| [5] | Nusslein-Volhard C, Wieschaus E, Kluding H. Mutations affecting the pattern of the larval cuticle in Drosophila melanogaster[J]. Roux’s Arch Dev Biol, 1984, 193(5): 267-282. |
| [6] | Wang B, Xiao Y, Ding B B, et al. Induction of tumor angiogenesis by Slit-Robo signaling and inhibition of cancer growth by blocking Robo activity[J]. Cancer Cell, 2003, 4(1): 19-29. |
| [7] | Wang L J, Zhao Y, Han B, et al. Targeting Slit-Roundabout signaling inhibits tumor angiogenesis in chemical-induced squamous cell carcinogenesis[J]. Cancer Sci, 2008, 99(3): 510-517. |
| [8] | Han X, Zhang M C. Potential anti-angiogenic role of Slit2 in corneal neovascularization[J]. Exp Eye Res, 2010, 90(6): 742-749. |
| [9] | Jones C A, London N R, Chen H, et al. Robo4 stabilizes the vascular network by inhibiting pathologic angiogenesis and endothelial hyperpermeability[J]. Nat Med, 2008, 14(4): 448-453. |
| [10] | 罗旭昇, 吴星伟, 顾青, 等. 复方血栓通对猴脉络膜-视网膜内皮细胞增生、移行和管腔形成的作用[J]. 中华眼视光学与视觉科学杂志, 2011, 13(4): 263-268. |
| [11] | Dong X, Wang Y S, Dou G R, et al. Influence of DⅡ4 via HIF-1α-VEGF signaling on the angiogenesis of choroidal neovascularization under hypoxia conditions[J]. PLoS One, 2011, 6(4): e18481. |
| [12] | Jin J, Yuan F, Shen M Q, et al. Vascular endothelial growth factor regulates primate choroid-retinal endothelial cell proliferation and tube formation through PI3K/Akt and MEK/ERK dependent signaling[J]. Mol Cell Biochem, 2013, 381(1/2): 267-272. |



