使用生物材料软组织代用品进行植入手术修复是软组织缺损及畸形治疗的重要手段。目前临床治疗中常用的有硅橡胶(silicone rubber,SR)、膨体聚四氟乙烯(ePTFE)、高密度聚乙烯(Medpor)等。其中硅橡胶在临床上最为常用,具有化学性质稳定,易塑形,易清洁、消毒,良好的经济性价比等优点[1]。但因硅橡胶表面呈强烈的疏水性,导致组织细胞的相容性较差,易形成包膜,导致假体挛缩移位[2],还容易引起感染、破溃[3]。只有对硅橡胶进行表面改性、修饰,使其表面达到仿生化效果,促进细胞黏附,调控细胞有序排列等,才能在临床应用中获得更好的效果。
在课题组前期研究中,采用羟基磷灰石进行表面仿生涂层[4]、β-磷酸三钙和硅橡胶进行共混交联复合[7, 8]等方法对硅橡胶进行改性处理,发现成纤维细胞在硅橡胶表面的黏附和增殖能力变强。同时也发现,几种改性材料的表面形貌均较硅橡胶发生了变化,提示我们硅橡胶的表面形貌影响材料的细胞相容性。为了进一步研究表面形貌对材料表面性能以及细胞生物学行为的影响,本研究在硅橡胶表面制作了微沟槽图形结构,研究了其表面理化性能和细胞增殖情况,以期为进一步研制具有临床应用前景的软组织填充材料提供依据。
1 材料与方法 1.1 具有微沟槽图形结构的硅橡胶制备取出具有微沟槽图形的12 cm×12 cm方形母版(中国电子科技集团公司第二十六研究所提供),将硅橡胶(成都晨光化工研究院)A、B组分按1 ∶1混匀后浇灌到母板上,室温下硫化3~4 h成膜,取下具有微沟槽图形结构的硅橡胶(patterned SR,P-SR)待下一步实验。
将制作的普通SR和P-SR置于多功能离子注入机(核工业西南物理研究院),以高纯度石墨为碳离子源[7, 8](注入剂量1×1016 ion/cm2)进行注入改性。
实验分组: SR组,P-SR组,碳离子注入改性硅橡胶(carbon ion implanted SR,C-SR)组,碳离子注入后的微沟槽图形硅橡胶(patterned carbon ion implanted SR,PC-SR)组。
1.2 扫描电镜(scanning electron microscope,SEM)观察材料表面大体形貌将各组材料分别裁剪成1 cm×1 cm大小,用去离子水清洗,37 ℃烤箱烤干。置于扫描电镜(型号S-3400N,日本)样本台上,在真空状态下向样本表面喷金镀膜,完毕后,扫描电镜下观察其形貌。
1.3 原子力显微镜(atomic force microscope,AFM)观察材料表面微观形貌将各组材料分别裁剪成1 cm×1 cm大小,置于装有无水乙醇的超声净化器清洗,37 ℃烤箱里烤干。清洁干燥后将材料平放于原子力显微镜(SAP400,日本)载物台上,探头随机对准一处,探测其表面形貌。
1.4 水接触角测量材料清洁步骤同原子力显微镜方法。将受试材料平放于水接触角测量仪(型号DropMeter A-100p,中国)载物台上,以去离子水为介质,选取3处不同部位,测量其水接触角,最后计算每组样本平均值。
1.5 细胞黏附实验利用人皮肤组织,采用组织块法进行人真皮成纤维细胞的原代培养,取3~4代细胞进行实验。将各材料裁剪成1 cm×1 cm大小,75%酒精消毒,紫外线照射30 min。将各组材料置于24孔板内,使用含10%小牛血清的DMEM培养液,接种5×104人真皮成纤维细胞/孔,37 ℃、5%CO2的培养箱继续培养6 h后,移除培养基,PBS清洗2~3次。黏附细胞采用胰酶消化收集,台盼蓝染色后,血球计数仪计数。细胞黏附率=黏附细胞数/接种细胞数×100%。
1.6 CCK-8法检测各组材料细胞增殖能力将各材料分别裁剪成6 cm×1 cm大小,75%酒精消毒,紫外线照射30min。 用无菌打孔机剪出近似96孔板大小的小圆片,置于孔板里,每组材料设置5组复孔,使用含有10%小牛血清的DMEM培养液,每孔接种4×103人真皮成纤维细胞/孔,37 ℃、5%CO2 的培养箱继续培养48 h。
废弃旧培养液,每孔加入50 μL DMEM+5 μL CCK-8液,加到96孔板里,同时加设1组空白组,为无细胞组。放入孵箱里继续培养1 h;使用酶标仪在波长450 nm处测量各孔光密度值[D(450)]。
1.7 免疫荧光观察材料表面细胞的生长材料准备和细胞接种方法同细胞黏附实验。接种4×104人真皮成纤维细胞/孔,37 ℃、5%CO2的培养箱继续培养48 h后,废弃培养液,加PBS清洗2~3次;3.7%甲醛溶液固定细胞15 min;0.1%Triton X-100/PBS穿孔细胞15 min;5%山羊血清室温封闭15 min;Actin-Tracker Green 避光室温孵育1 h;PBS避光清洗;Hoechst33342避光孵育5 min,50%甘油滴于载玻片上封片,置于激光共聚焦显微镜下观察材料表面细胞的生长情况。
1.8 Western blot检测细胞黏附相关蛋白的表达将人真皮成纤维细胞接种于铺有材料的6孔板里,置于37 ℃、5%CO2孵箱培养48 h。RIPA细胞裂解液提取总蛋白,蛋白上样量为20 μg,蛋白转印至PVDF膜(Millipore公司,美国)后,5%脱脂奶粉封闭 2 h,一抗使用兔抗人踝蛋白Talin(1 ∶500,Abcam公司,英国),兔抗人斑联蛋白Zyxin(1 ∶500,Cell Signaling公司,美国),内参GADPH(1 ∶1 000,康晨公司,中国),4 ℃过夜孵育。二抗室温孵育2 h,Talin及GADPH抗体使用辣根过氧化物酶(HRP)标记山羊抗兔(1 ∶1 000),Zyxin使用辣根过氧化物酶(HRP)标记山羊抗兔(1 ∶400)。配制ECL显色试剂(碧云天公司,中国) ,于凝胶成像仪曝光显影。
1.9 统计学分析实验数据以x±s表示,采用SPSS 17.0统计软件进行单因素方差分析和Tukey显著性检验。采用Quantity One软件进行结果分析,统计蛋白灰度比值。
2 结果 2.1 材料表面形貌SEM观察各材料表面形貌,P-SR较SR比较,未观察到有明 显变化;PC-SR和C-SR比较,观察到材料表 面出现了部分纹理,PC-SR较C-SR纹理多,其排列无明显规律(图 1)。
 |
| A: SR; B: P-SR; C: C-SR; D: PC-SR 图 1 SEM观察各组材料的表面形貌 |
AFM观察发现:4组材料的表面形貌有显著差异,SR表面平滑,P-SR呈现微沟槽图形,约6 μm宽;碳离子注入后改变了SR的表面结构,呈现不规则的凸凹结构(C-SR),PC-SR在微沟槽图形基础上呈现凸凹结构(图 2)。
 |
| A:SR;B:P-SR;C:C-SR;D:PC-SR 图 2 AFM观察各组材料表面微观形貌 |
各组材料水接触角从低到高依次为C-SR、SR、PC-SR、P-SR(表 1)。
| 组别 | 水接触角(°) | 细胞黏附率(%) | 细胞增殖[D(450)] |
| SR组 | 110.13±1.35 | 20.44±3.32 | 0.153±0.024 |
| P-SR组 | 120.93±2.99 | 19.66±3.63 | 0.154±0.017 |
| C-SR组 | 101.53±2.65 | 50.50±4.35a | 0.342±0.028a |
| PC-SR组 | 114.10±2.21 | 48.50±4.10a | 0.270±0.014a |
| a: P<0.05,与SR、P-SR比较 | |||
C-SR组、PC-SR组分别与SR组、P-SR组比较,细胞黏附率明显提高(P<0.05),其中C-SR组细胞黏附率最高,PC-SR组细胞黏附率略低于C-SR组,PC-SR 组和C-SR组相比,差异无统计学意义(P>0.05,表 1)。
2.4 细胞增殖能力C-SR组、PC-SR组分别与SR组和P-SR组比较,细胞增殖能力明显提高(P<0.05)。其中C-SR组细胞增殖能力最强,PC-SR组细胞黏附率略低于C-SR组,C-SR组和PC-SR组比较,差异无统计学意义(P>0.05,表 1)。
2.5 细胞生长情况人真皮成纤维细胞在SR的生长情况较差,细胞稀疏,排列无序;P-SR组细胞生长情况较SR类似,但细胞梭形较SR明显,排列有序。C-SR组细胞生长情况优于SR,且细胞形态铺展,面积增大;PC-SR组,细胞生长优于SR和P-SR,略差于C-SR,细胞铺展情况优于SR和P-SR,但较C-SR差,细胞的排列较C-SR组相比有序(图 3)。
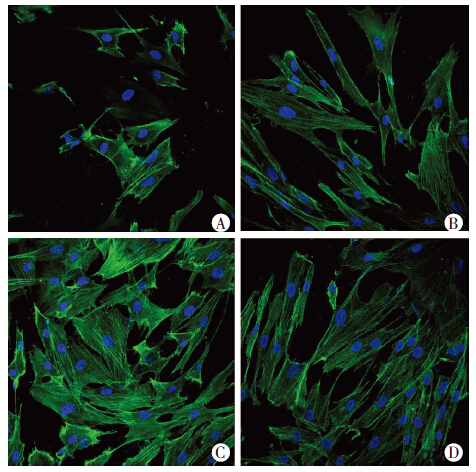 |
| A:SR;B:P-SR;C:C-SR;D:PC-SR 图 3 免疫荧光观察各组材料表面细胞生长情况 (×800) |
C-SR和PC-SR组Talin、Zyxin表达较SR升高,各组之间比较差异无统计学意义(P>0.05,图 4)。
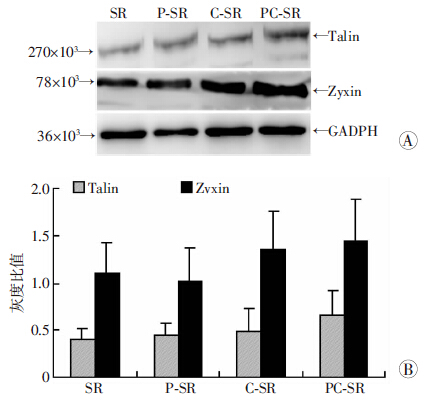 |
| A: Western blot检测结果;B:定量分析 图 4 Western blot检测各组材料表面细胞中Talin、Zyxin蛋白的表达 |
本研究采用母版制作的具有微图形的硅橡胶材料,由于母版的沟槽尺寸约为6 μm,SEM无法观察到P-SR和PC-SR组有明显的沟槽状结构,进一步采用AFM观察,可观察到P-SR和PC-SR表面的沟槽样结构(图 2)。排列一致的微沟槽图形会使细胞的排列有序,胞体突起沿着沟槽方向有序排列[9],本研究中也观察到此现象(图 3)。在课题组前期研究中,发现采用C离子注入会使材料表面形成凸凹结构(C-SR)。这是由于自离子源被激发后,携带高能能量的碳离子作用于硅橡胶,轰击其表面所形成,从而有利于细胞黏附[7]。而在具有微图形的SR表面进行C离子注入,可观察到微沟槽图形的基础上呈现了凸凹结构,但这种改性会对材料的表面性能和细胞生长排列造成何种影响呢?
本实验发现对材料进行微沟槽处理后,会增加材料的水接触角,降低其亲水性(表 1)。细胞在材料表面的生长行为与材料表面的亲/疏水性有关[10]。因此,本研究通过细胞黏附和增殖实验,以及免疫荧光观察细胞在各组材料表面的形态和生长情况,观察到人真皮成纤维细胞在SR表面的生长情况较差,细胞稀疏;C-SR组细胞增殖能力最强,细胞形态铺展。P-SR组和PC-SR组细胞排列较为有序,形态呈梭形。其中,细胞增殖实验结果提示微图形化后细胞的黏附和增殖能力轻度下降,但细胞的排列有序。目前较多的理论认为亲水性表面有利于细胞外基质蛋白的粘附,进而促进细胞的黏附和增殖[11, 12],但也有学者认为若材料表面亲水性过强,会不利于蛋白质吸附,进而影响细胞 黏附和增殖[13, 14, 15]。这可能是由于高度亲水性材料可引起更多细菌以及其他杂质分子的吸附而引起异物反应。有研究指出,由于材料表面水化层与材料局部区域接触,两者孔隙间存在空气,细胞与材料的接触面实质是材料表面、空气层以及水化层组成的复合界面[16]。光滑的SR表面,液滴则与界面完全接触,当材料表面存在微图形时,液滴与材料面接触不完全,液滴会黏滞于具有微图形的材料表面,增加水接触角,从而不利于蛋白的吸附和细胞增的殖。因此,只有亲/疏水性达到适宜的平衡值才会促进蛋白质的吸附和细胞的增殖。
临床应用研究表明,图形化的硅橡胶假体和平滑的硅橡胶假体相比,可减少包膜挛缩的发生率[17]。这可能是由于图形化的硅橡胶和平滑硅橡胶引起的细胞内反应不同造成。例如:Seyhan等[18]研究提示成纤维细胞培养于图形化的硅橡胶材料和光滑硅橡胶表面,光滑组TGF-β的表达明显高于图形组,说明图形组成纤维细胞向肌成纤维细胞的分化受到了抑制,因而减少了包膜(实质是材料周围的瘢痕化组织形成)挛缩的发生。也有学者指出,在图形化材料表面生长的细胞,由于微图形导致的细胞接触抑制,可抵消细胞相互接触的收缩力,减少包膜挛缩发生[19]。结合本研究的结果,发现微沟槽图形结构可影响材料的水接触角,进而影响细胞的黏附、增殖和排列等。这可能是由于材料表面微图形结构发挥了“接触导向”作用[20],影响到粘着斑的形成和定位[21, 22, 18],再通过细胞内信号传导,调控微丝的结构、中间丝以及微管的组装,使得细胞定位和形态发生改变。本研究发现与细胞黏附相关的蛋白Talin和Zyxin的表达发生了变化,这种改变可通过不同的信号内传导途径,引起细胞一系列反应,表现为细胞的骨架排列,细胞黏附、增殖等发生变化,细胞功能的改变,最终会减少包膜挛缩的发生率。此外,还有学者指出,微图形结构可抑制细菌孢子在硅橡胶表面的黏附,减低感染导致的包膜挛缩发生率[23, 24]。
通过本研究结果,结合相关研究,提示我们微图形结构可影响细胞的功能,减少包膜挛缩的发生率。这也提示我们,可在生物植入材料表面制作不同的微图形结构,从而对细胞的增殖和排列等进行控制,以调控细胞功能,设计出符合临床应用要求的植入材料。此外,微图形的形状和大小如何对细胞的生物学行为造成影响以及相关机制,还需要我们进一步研究。
| [1] | Hatamleh M M, Watts D C. Mechanical properties and bonding of maxillofacial silicone elastomers[J]. Dent Mater, 2010, 26(2): 185-191. |
| [2] | Franca D C, de-Castro A L, Soubhia A M,et al. Biocompatibility evaluation of 3 facial silicone elastomers[J]. J Craniofac Surg, 2011, 22(3): 837-840. |
| [3] | Bellamy K, Limbert G, Waters M G,et al. An elastomeric material for facial prostheses: synthesis, experimental and numerical testing aspects[J]. Biomaterials, 2003, 24(27): 5061-5066. |
| [4] | 王一丞, 张一鸣, 石小花, 等. 仿生化硅橡胶基羟基磷灰石涂层材料的研制与性能检测[J]. 第三军医大学学报, 2012, 34(4): 324-327. |
| [5] | Zhang Y M, Wang S L, Lei Z Y,et al. Mechanical and biological evaluations of beta-tricalcium phosphate/silicone rubber composite as a novel soft-tissue implant[J]. Aesthetic Plast Surg, 2009, 33(5): 760-769. |
| [6] | Zhang Y M, Wang S L, Wang Y C,et al. Evaluation of the surface physical properties of β-tricalcium phosphate/silicone rubber, a prospective softtissue implant material[J]. Mater Lett, 2012, 66(1): 203-205. |
| [7] | Wang S L,Shi X H,Yang Z,et al. Osteopontin (OPN) is an important protein to mediate improvements in the biocompatibility of C ion-implanted silicone rubber[J]. PLoS One, 2014, 9(6):e98320. |
| [8] | 杨芷, 沈丽如, 石小花, 等. 碳离子硅橡胶改性材料的表面性能检测及其细胞相容性评价[J]. 第三军医大学学报, 2013, 35(2): 123-126. |
| [9] | Gingras J, Rioux R M, Cuvelier D,et al. Controlling the orientation and synaptic differentiation of myotubes with micropatterned substrates[J]. Biophys J, 2009, 97(10): 2771-2779. |
| [10] | Lu D R, Park K. Effect of surface hydrophobicity on the conformational changes of adsorbed fibrinogen[J]. J Coloid Interface Sci, 1991, 144(1): 271-281. |
| [11] | Ismail F S, Rohanizadeh R, Atwa S,et al. The influence of surface chemistry and topography on the contact guidance of MG63 osteoblast cells[J]. J Mater Sci Mater Med, 2007, 18(5): 705-714. |
| [12] | Rausch-fan X, Qu Z, Wieland M,et al. Differentiation and cytokine synthesis of human alveolar osteoblasts compared to osteoblast-like cells (MG63) in response to titanium surfaces[J]. Dent Mater, 2008, 24(1): 102-110. |
| [13] | Feng X, Feng L, Jin M,et al. Reversible super-hydrophobicity to super-hydrophilicity transition of aligned ZnO nanorod films[J]. J Am Chem Soc, 2004, 126(1): 62-63. |
| [14] | 高长有,马列. 医用高分子材料[M].北京:化学工业出版社, 2006. |
| [15] | Rabe M, Verdes D, Seeger S. Understanding protein adsorption phenomena at solid surfaces[J]. Adv Colloid Interface Sci, 2011, 162(1/2): 87-106. |
| [16] | Cassie A B D,Baxter S. Wettability of porous surfaces[J]. Trans Faraday Soc, 1944, 40: 546-551. |
| [17] | Barnsley G P, Sigurdson L J, Barnsley S E. Textured surface breast implants in the prevention of capsular contracture among breast augmentation patients: a meta-analysis of randomized controlled trials[J]. Plast Reconstr Surg, 2006, 117(7): 2182-2190. |
| [18] | Seyhan H, Kopp J, Beier J P,et al. Smooth and textured silicone surfaces of modified gel mammary prostheses cause a different impact on fibroproliferative properties of dermal fibroblasts[J]. J Plast Reconstr Aesthet Surg, 2011, 64(3): e60-e66. |
| [19] | Harvey A G, Hill E W, Bayat A. Designing implant surface topography for improved biocompatibility [J]. Expert Rev Med Devices, 2013, 10(2): 257-267. |
| [20] | Zhou F, Yuan L, Huang H,et al. Phenomenon of “contact guidance” on the surface with nano-micro-groove-like pattern and cell physiological effects [J]. Chinese Sci Bull, 2009, 54(18): 3200-3205. |
| [21] | Seo C H, Furukawa K, Montagne K,et al. The effect of substrate microtopography on focal adhesion maturation and actin organizationvia the RhoA/ROCK pathway[J]. Biomaterials, 2011, 32(36): 9568-9575. |
| [22] | Yan C, Sun J, Ding J. Critical areas of cell adhesion on micropatterned surfaces[J]. Biomaterials, 2011, 32(16): 3931-3938. |
| [23] | Seo J H, Shin D S, Mukundan P,et al. Attachment of hydrogel microstructures and proteins to glass via thiol-terminated silanes[J]. Colloids Surf B Biointerfaces, 2012, 98: 1-6. |
| [24] | Cooper S P, Finlay J A, Cone G,et al. Engineered antifouling microtopographies: kinetic analysis of the attachment of zoospores of the green alga Ulva to silicone elastomers[J]. Biofouling, 2011, 27(8): 881-891. |



