2 264200 山东威海,威海市立医院神经内科
2 Department of Neurology, Weihai Municipal Hospital, Weihai, Shandong Province,264200, China
脑出血(Intracerebral hemorrhage,ICH)是急性脑血管病最常见的类型之一,约占脑血管病的10%~15%[1]。ICH有着较高的致残率和致死率[2, 3]。脑出血病理生理机制十分复杂,破入脑组织的血液凝固形成的血肿引起的占位效应可直接导致神经损伤,而血肿的成分及其降解产物则主要是引起继发性脑损害的主要原因[1, 4]。因此,及时、有效地清除血肿成为脑出血的重要治疗手段。但是,脑出血外科手术清除血肿的大型临床试验研究未达到预期的目标[5],而脑组织本身具有重要的血肿吸收能力,因此,促进血肿的自身吸收有望成为脑出血治疗的新手段。
CD36是主要的清道夫受体,广泛存在于小胶质细胞、单核细胞、血小板、血管内皮细胞等[6]。CD36通过吞噬氧化低密度脂蛋白(ox-LDL)、β淀粉样蛋白(Aβ)等在动脉粥样硬化及老年性痴呆的发病机制中发挥着重要的作用[7]。同时,CD36已被证实在脑出血中介导了血肿的吸收[8],并且受炎症反应的调控[9, 10]。此外,我们近期通过小样本临床实验研究发现CD36缺陷的脑出血患者血肿吸收明显减慢并且神经功能缺损重于CD36正常的患者[10]。本研究旨在通过扩大脑出血样本量,进一步探讨CD36缺陷对脑出血患者血肿吸收及神经功能恢复的影响。 1 资料与方法 1.1 研究对象
选择2012年7月至2014年6月在第三军医大学新桥医院神经内科住院的脑出血患者367例。参照欧洲卒中指南[11]及第四届中国脑血管病会议(1996)标准,纳入如下患者:①发病12 h内;②经过头颅CT检测证实为脑出血,且为第1次发病的患者。同时参照我们之前建立的标准,排除如下患者:①年龄小于18岁或大于80岁;②接受了外科手术治疗;③昏迷或入组48 h内死亡;④由脑肿瘤、创伤、药物滥用、凝血异常、抗凝治疗或血管畸形导致的脑出血;⑤入组半年前存在明显的炎性疾病(如:急慢性感染性疾病,系统性红斑狼疮、风湿、类风湿性疾病)等自身免疫性疾病;⑥医院获得性感染;⑦急性心肌梗死;⑧急慢性肝功能损害;⑨不遵从试验协议或不能接受测试研究的患者。共有18例患者被排除研究,包括失访患者8例和死亡患者10例。最后收集符合研究的病例349例:男性197例,女性152例;年龄22~79(58.38±14.35)岁。所有患者或监护人均同意本临床研究内容并签署知情同意书。本研究获得第三军大学新桥医院临床伦理委员会的批准。 1.2 脑出血患者临床资料收集 1.2.1 一般临床资料
所有入组研究的患者在入院时,发病24 h内,入院第3、7天进行CT检查。美国国立卫生院卒中量表(NIHSS)评分分别于患者入院时、发病后第7、14、30天进行,由1名经过专业培训且对患者临床资料不清楚的有经验的医师完成。mRS评分在患者发病3个月后随访时进行。患者的其他临床资料如:性别、年龄、发病至入院间隔时间、生命体征(体温、血压)、血管危险因素(有无高血压、糖尿病、血脂异常、吸烟史、饮酒史)、前期治疗(有无使用降压药物、降脂药物、降糖药物) 、实验室检查指标(血糖、血脂、血小板计数、白血球计数等)均在入院时获得。所有研究者均接受相同且专业的课题研究培训。 1.2.2 脑出血患者血肿体积计算
参照既往文献报道[12],采用公式: π/6×长 (cm)×宽 (cm)×高 (cm)计算血肿体积。并根据如下公式计算血肿吸收速度:(7 d时血肿体积-入院时血肿体积) /入院时血肿体积 ×100%。由1名具有专业背景知识的神经内科高级职称医师集中完成血肿体积的计算。 1.2.3 脑出血患者血样的收集与保存
入组的脑出血患者于入院时抽取肘静脉血10 mL进行分装、编号,将血标本冻存于-80 ℃冰箱。同时,获得血清标本利用酶联免疫吸附试验(ELISA)试剂盒检测血清炎症因子(IL-6、TNF-α、CRP等)。 1.3 方法 1.3.1 聚合酶链反应(PCR)
利用的全血基因组DNA试剂盒(原平皓生物技术有限公司,北京)提取患者基因组DNA,具体操作详见试剂盒说明书。将提取的外周血进行PCR检测,以鉴定CD36基因缺陷,PCR合成条件为: 20 μL 反应体系扩增分3步进行:94 ℃ 4 min;94 ℃ 30 s,60 ℃ 30 s,72 ℃ 30 s,共35个循环;72 ℃ 10 min。引物及探针设计按照亚洲人常见的缺陷类型及部位进行(表 1)。将10 μL PCR产物在2%
琼脂糖凝胶中进行电泳。电泳图中缺失的条带表示为CD36有缺陷。
突变位点 | 引物序列 | 片段长 度(bp) |
| C268T | 上游:5′-TATTCTGGCTGACTCAAGGC-3′ 下游:5′-ATGGTCAAGGTAAGAGTGTCTCA-3′ | 296 |
| 329-330del | 上游:5′-TAAGACCCCTTCTCGTTAGTTT-3′ 下游:5′-CCAAATGACCATGCCTCC-3′ | 487 |
| 619-624ins | 上游:5′-CATTTGAGTAACCAGTGATTGAGA-3′ 下游:5′-CAGAACAGGAGTTTCCAGAGC-3′ | 338 |
| 949ins | 上游:5′-CTTGGCTATTGAGTTTTAGTATGTG-3′ 下游:5′-TGCCACCATTCTTTCTTCTG-3′ | 576 |
| 1228-1239del | 上游:5′-GAGTCATTACAGGAACAAAATCAAA-3′ 下游:5′-TGGGTAATGGAAATACATATAGCTT-3′ | 290 |
此前,有报道显示炎症因子在脑出血后第3天达到高峰,并逐步恢复正常[10]。为比较2组患者炎症因子在恢复期的变化情况,我们利用ELISA技术检测患者发病后第3、14天血清炎症因子的变化。 1.4 统计学分析
采用SPSS 13.0统计软件。数据表示为x±s或百分比。2组间比较采用单因素方差分析;百分比之间的比较采用χ2检验。 2 结果 2.1 脑出血患者CD36缺陷筛查
CD36的5种突变位点均有CD36条带缺失,经统 计发现35例存在CD36缺陷,占脑出血总人数的10.03%。其中,C268T型6例,329-330del型10例,1228-1239del型11例,949ins型4例,619-624ins型5例(图 1)。
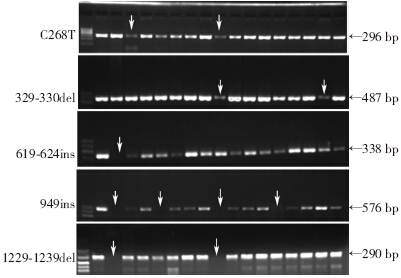 |
| ↑:脑出血患者筛查出不同位点的CD36缺陷图 1 基底节区脑出血患者CD36缺陷位点的典型PCR电泳图 |
由于脑出血部位不同,即使出血量相同的患者间NIHSS评分会有较大的差异。因此,我们从35例CD36缺陷患者中挑选出24例基底节区脑出血患者作为进一步的研究对象,同时从CD36正常的脑出血患者中随机挑选出24例出血部位、出血量、年龄、性别及其他因素相近的患者作为正常对照组(表 2),并且该 48例患者24 h内的头颅CT检查均未发现有血肿扩大(图 2)。 2组患者临床基本资料、影像学特征、生化指标差异无显著性(P>0.05)。
| 组别 | 年龄(x±s,岁) | 男性 [例(%)] |
发病到就诊时间 [中位数(四分位间距),h] |
危险因素[例(%)] | ||||
| 高血压 | 糖尿病 | 吸烟 | 脂糖代谢异常 | 酗酒 | ||||
| CD36正常组 | 60.8 ±7.0 | 16(66.7) | 7.6 (3.5~12.0) | 17(70.8) | 13(54.2) | 16(66.7) | 15(62.5) | 6(25.0) |
| CD36缺陷组 | 60.3±6.0 | 17(70.8) | 7.3 (3.0~11.0) | 16(66.7) | 14(58.3) | 15(62.5) | 13(54.2) | 7(29.2) |
| 组别 | 发病前使用药物 [例(%)] | 生命体征(x±s) | ||||||
| 降脂药 | 抗血小板 聚集药 | 降糖药 | 收缩压 (mmHg) | 舒张压 (mmHg) | 24 h最大收缩压 (mmHg) | 24 h最大舒张压 (mmHg) | 体温 (C°) | |
| CD36正常组 | 14(58.3) | 9(37.5) | 8(33.3) | 167±13 | 99±6 | 182±10 | 107±7 | 36.7±0.3 |
| CD36缺陷组 | 12(50.0) | 10(41.7) | 7(29.2) | 163±12 | 100±6 | 178±10 | 108±6 | 36.7±0.4 |
| 组别 | NIHSS评分 (分,±s) |
神经影像血肿体积 (cm3,x±s) |
实验室指标(x±s) | |||||
| 血糖(mg/dL) | 血小板计数 (×1 000/mm3) | 白细胞计数 (×1 000/mm3) | ||||||
| CD36正常组 | 16.8±3.7 | 22.9±3.8 | 138±10 | 190±18 | 8.2±1.3 | |||
| CD36缺陷组 | 17.4±4.2 | 23.2±3.9 | 136±11 | 192±14 | 8.1±1.4 | |||
 |
| 图 2 基底节区脑出血患者血肿吸收典型头颅CT表现 |
入院时2组患者血肿体积无明显差异[(23.2± 3.9) vs (22.9±3.8)mL,P>0.05]。但在脑出血后第7天,CD36缺陷患者血肿体积显著大于CD36正常患者[(17.3±1.2) vs (12.7±1.7)mL,P<0.05]。同时,CD36缺陷患者血肿吸收速度显著低于CD36正常患者[(22.4±2.4)% vs (44.8±5.1)%,P<0.05]。 2.4 CD36缺陷患者神经功能缺损评分明显增高
2组患者入院时NHISS评分比较显示:在入院时及发病第7天,2组患者NIHSS评分无显著差异(P>0.05),而在第14、30天时CD36缺陷患者NIHSS评分显著高于CD36正常患者(P<0.05,表 3)。同时,3个月随访时2组患者的mRS量表评分显示:CD36缺陷患者mRS评分明显增高(1.67±0.49 vs 0.67±0.52,P<0.05)。
| 组别 | 入院时 | 7 d | 14 d | 30 d |
| CD36缺陷组 | 17.6±1.4 | 15.7±2.4 | 14.2±2.7a | 8.4±2.1a |
| CD36正常组 | 16.9±1.1 | 15.1±1.8 | 12.1±2.3 | 6.5±1.9 |
| a:P<0.05,与CD36正常组比较 | ||||
脑出血后3 d,2组患者外周血TNF-α、IL-6及CRP水平差异无统计学意义(P>0.05,表 4);但在脑出血后14 d,CD36正常患者炎症因子水平较CD36缺陷患者显著降低(P<0.05,表 4)。
| 组别 | 3 d | 14 d | ||||
| TNF-α(pg/mL) | IL-6(pg/mL) | CRP(mg/L) | TNF-α(pg/mL) | IL-6(pg/mL) | CRP(mg/L) | |
| CD36正常组 | 18.16±3.31 | 14.57±3.21 | 20.21±2.48 | 7.29±1.54 | 4.74±2.13 | 9.26±1.93 |
| CD36缺陷组 | 19.87±3.72 | 15.01±3.49 | 19.57±3.18 | 13.26±3.38a | 8.17±3.01a | 13.24±2.95a |
| a:P<0.05,与CD36正常组比较 | ||||||
近年来,促进血肿的吸收成为治疗脑出血的新靶点[8, 10]。本研究从临床角度进一步研究CD36在脑出血患者血肿吸收中的作用,得出如下结论:①CD36缺陷在脑出血人群中占据着较大的比例,即10.03%;②CD36 缺陷的患者脑出血后血肿吸收速率较CD36正常患者慢;③CD36缺陷患者远期神经功能恢复较正常患者慢。
大量研究显示人群存在着CD36基因型缺陷。CD36缺陷分为两型:单核细胞和血小板均有CD36缺失为CD36Ⅰ型缺陷,而仅有血小板缺失为CD36Ⅱ型缺陷[7]。有意思的是,在欧、美人种中极少发现CD36缺陷,但在亚、非人种中CD36缺陷比例超过2%[13]。国内有报道显示,广东深圳和肇庆地区人群CD36抗原缺失型频率分别为3.06%和5%[14, 15]。然而,在中国对健康献血者的CD36进一步研究发现CD36的突变率低于亚洲人种的突变率[16, 17]。本研究中,我们从349例脑出血患者中筛选出35例CD36缺陷者(10.03%),结果与我们前期的小样本量研究相符,但CD36缺陷率较其他研究结果偏高,究其原因可能与我们选取的研究人群局限于脑出血患者有关。
此前,Zhao等[8]研究显示CD36在小鼠脑出血血肿吸收过程中具有重要作用。我们前期小样本量的研究亦发现CD36在促进脑出血血肿吸收中具有重要的作用,并且通过动物实验进一步证实CD36介导的血肿吸收受TLRs诱导的促炎因子的负调控[10]。本次临床研究经扩大脑出血样本量后进一步证实了CD36可促进脑出血后血肿吸收的作用,并且CD36缺陷的患者预后较CD36正常的患者 差,与之前的小样本量研究结果一致。CD36缺陷的患者血肿吸收慢,导致血肿成分对机体较长时间的慢性刺激,因此,导致患者炎症因子下降较CD36正常患者慢,即2组患者的炎症因子水平在第5天时无明显差异,但在第14天时前者显著高于后者。此外,由于慢性的炎症刺激导致了CD36缺陷的患者神经功能缺损评分在第14、30天时高于CD36正常患者,甚至在脑出血后的3月时也表现出显著差异。
本研究结果显示:脑出血人群中存在一定比例CD36缺陷,CD36在促进脑出血后血肿吸收中具有重要的作用。但是,本研究虽扩大了研究的样本量,仍为单中心的研究。下一步可进行多中心、大样本量研究来进一步证实CD36在血肿吸收中的作用。
| [1] | Keep-R F, Hua Y, Xi G. Intracerebral haemorrhage: mechanisms of injury and therapeutic targets[J]. Lancet Neurol, 2012, 11(8): 720-731. |
| [2] | 罗丹, 李芳芳, 王啸, 等. 自发性脑出血患者并发症的相关危险因素分析[J]. 第三军医大学学报, 2012, 34(14): 1438-1441. |
| [3] | 朱孔江, 徐广振, 杨辉. 小鼠脑出血模型血肿周围雌激素受体的表达[J]. 第三军医大学学报, 2013, 35(17): 1877-1879. |
| [4] | Zhou Y, Wang Y, Wang J,et al. Inflammation in intracerebral hemorrhage: from mechanisms to clinical translation[J]. Prog Neurobiol, 2014, 115: 25-44. |
| [5] | Mendelow A D, Gregson B A, Rowan E N,et al. Early surgery versus initial conservative treatment in patients with spontaneous supratentorial lobar intracerebral haematomas (STICH Ⅱ): a randomised trial[J]. Lancet, 2013, 382(9890): 397-408. |
| [6] | Silverstein-R L, Febbraio M. CD36, a scavenger receptor involved in immunity, metabolism, angiogenesis, and behavior[J]. Sci Signal, 2009, 2(72): re3. |
| [7] | Silverstein-R L. Inflammation, atherosclerosis, and arterial thrombosis: role of the scavenger receptor CD36[J]. Cleve Clin J Med, 2009, 76 Suppl 2: S27-S30. |
| [8] | Zhao X, Sun G, Zhang J,et al. Hematoma resolution as a target for intracerebral hemorrhage treatment: role for peroxisome proliferatoractivated receptor gamma in microglia/macrophages[J]. Ann Neurol, 2007, 61(4): 352-362. |
| [9] | Sansing L H, Harris T H, Welsh F A,et al. Tolllike receptor 4 contributes to poor outcome after intracerebral hemorrhage[J]. Ann Neurol, 2011, 70(4): 646-656. |
| [10] | Fang H, Chen J, Lin S,et al. CD36mediated hematoma absorption following intracerebral hemorrhage: negative regulation by TLR4 signaling[J]. J Immunol, 2014, 192(12): 5984-5992. |
| [11] | Steiner T, Kaste M, Forsting M,et al. Recommendations for the management of intracranial haemorrhage—part I: spontaneous intracerebral haemorrhage. The European Stroke Initiative Writing Committee and the Writing Committee for the EUSI Executive Committee[J]. Cerebrovasc Dis, 2006, 22(4): 294-316. |
| [12] | Gao L, Zhao H, Liu Q,et al. Improvement of hematoma absorption and neurological function in patients with acute intracerebral hemorrhage treated with Xueshuantong[J]. J Neurol Sci, 2012, 323(1/2): 236-240. |
| [13] | Aitman T J. CD36, insulin resistance, and coronary heart disease[J]. Lancet, 2001, 357(9257): 651-652. |
| [14] | 李大成, 蓝欲晓, 鲍自谦, 等. 深圳地区无偿献血者群体CD36抗原缺失型的表型分析[J]. 中国输血杂志, 2012, 25(4): 304-307. |
| [15] | 刘凌, 叶刚强, 李流娇, 等. 肇庆地区普通人群血小板基因HPA16和15基因多态性及CD36抗原缺失分析[J]. 广东医学, 2013, 34(13): 2054-2056. |
| [16] | Li R, Qiao Z, Ling B,et al. Incidence and molecular basis of CD36 deficiency in Shanghai population[J]. Transfusion, 2015, 55(3): 666-673. |
| [17] | Xu X, Ye X, Xia W,et al. Studies on CD36 deficiency in South China: two cases demonstrating the clinical impact of antiCD36 antibodies[J]. Thromb Haemost, 2013, 110(6): 1199-1206. |



