经椎间孔腰椎椎间融合术(transforaminal lumbar interbody fusion,TLIF)最先由Harms等[1]报道,该术式与传统的后路腰椎椎间融合(posterior lumbar interbody fusion,PLIF)相比,减少了脊髓受牵拉损伤和硬膜外纤维化的发生率,现已逐渐成为处理腰椎退行性病变的常用手术方式。由于术中减压操作使手术节段稳定性受到破坏,TLIF手术需要辅以后路椎弓根螺钉固定维持术后初始的节段稳定性[2, 3, 4, 5, 6]。目前,TLIF手术的治疗效果已经获得了较多临床研究和体外生物力学研究的证实[7, 8, 9, 10, 11, 12, 13],而后路双侧椎弓根螺钉固定方式也被生物力学研究证实可以提供融合节段足够坚强的稳定性[2, 3, 7, 9]。
通常认为后路内固定在椎间植骨融合完成之后所产生的固定作用将逐渐消失。有学者主张在确切的植骨融合形成后去除后路内固定[14];但有研究却发现植骨融合后内固定装置上仍然承受着和未融合状态下几乎一致的载荷[15, 16],去除内固定可能会带来对融合节段不利改变。因此,研究椎间植骨融合前后固定节段的生物力学功能变化是有必要的,将有助于回答植骨融合后是否应该去除后路内固定的问题。本研究拟通过有限元分析的方法构建植骨融合和未融合状态下的TLIF手术模型,探讨植骨融合进程对固定节段各项生物力学指标的影响,为临床实践提供生物力学理论依据。
1 资料与方法 1.1 三维有限元模型的建立健康成年男性志愿者1例(29岁,身高172 cm,体质量70 kg),既往无腰椎疾病史,拍摄腰椎X线片排除腰椎病变。志愿者知情同意,研究通过第三军医大学新桥医院伦理委员会审查。采用Philips Brilliance 64排螺旋CT从胸12椎体上缘至骶2椎体进行连续扫描,扫描参数:层厚1.0 mm,球管电流200 mA,电压120 kV。选取L3~S1椎体断面图像共193张,以通用DICOM格式读入Mimics软件,建立L3~S1椎体的STL三角网格模型,然后导入逆向工程软件Geomagic中进行修补与优化,生成表面模型。利用SolidWorks将生成的表面模型转换成实体模型,包括皮质骨、松质骨、终板、椎间盘、前纵韧带、后纵韧带、黄韧带、棘间韧带、棘上韧带等结构。韧带结构均设置为TRUSS单元,只承受牵拉载荷而不受压缩载荷。椎间盘结构包括髓核、纤维环和纤维环纤维[17]。在SolidWorks软件中通过上下终板平面放样生成了椎间盘的外形,按照3 ∶2比例切割划分髓核和纤维环结构。纤维环纤维按照与终板平面呈30°~45°的方式绘制。将实体模型导入有限元分析软件Abaqus 6.10,应用壳单元的处理方法设定皮质骨和骨性终板厚度为1.0 mm。将各部位材料的弹性模量、泊松比等材料系数及特征值输入模型(表 1)[18, 19, 20, 21],设置各部件相互作用关系,将关节突关节面用接触单元进行处理,对模型进行有限元网格划分。完成人正常L3~S1节段有限元模型(INT)的建立(图 1)。
| 材料 | 弹性模量(MPa) | 泊松比 | 横截面积(mm2) |
| 皮质骨 | 12 000.0 | 0.29 | - |
| 终板 | 1 200.0 | 0.29 | - |
| 松质骨 | 100.0 | 0.29 | - |
| 纤维环基质 | 4.2 | 0.40 | - |
| 髓核 | 1.0 | 0.49 | - |
| 纤维环纤维 | 450.0 | 0.45 | - |
| 前纵韧带 | 7.8 | 0.30 | 63.7 |
| 后纵韧带 | 10.0 | 0.30 | 20.0 |
| 棘上韧带 | 10.0 | 0.30 | 40.0 |
| 棘间韧带 | 8.0 | 0.30 | 30.0 |
| 黄韧带 | 15.0 | 0.30 | 40.0 |
| 横突间韧带 | 10.0 | 0.30 | 1.8 |
| 关节囊韧带 | 7.5 | 0.30 | 30.0 |
| 钛合金 | 110 000.0 | 0.30 | - |
| 椎间融合器 | 3 600.0 | 0.30 | - |
在正常L3~S1模型的基础上模拟构建TLIF手术模型。根据标准TLIF手术过程进行模拟,切除L4~L5节段右侧关节突,切除髓核组织,保留纤维环纤维与外层纤维环,斜行45°置入椎间融合器[3]。椎间融合器为PEEK融合器,高度为12 mm,与椎体终板接触为面性接触,融合器内充填松质骨,放置深度为融合器后缘于椎体后缘前4 mm处[22, 23]。采用椎间植入物与上下终板接触关系设定为面面接触的方法模拟椎间融合前状态,摩擦系数为0.3[3, 24],采用椎间植入物与上下终板接触关系设定为绑定的方法模拟椎间融合后状态。模拟Sextant系统椎弓根螺钉固定,螺钉直径6.5 mm,长50 mm。利用软件重建融合前无椎弓根螺钉固定模型即未融合未固定模型(M1)、融合前双侧椎弓根螺钉固定模型即未融合固定模型(M2)、融合后双侧椎弓根螺钉固定即融合固定模型(M3)、融合后去除椎弓根螺钉模型(M4)(图 1)。
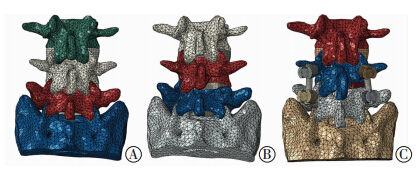 |
| A:人正常L3~S1三维有限元模型; B:TLIF手术损伤模型;C:双侧椎弓根螺钉内固定模型 图 1 腰骶椎三维有限元模型图 |
将S1椎体的下表面全固定,限制其所有的自由度。模型有效性验证采用与Renner等[25]的离体生物力学实验条件一致的加载方式,耦合L3椎体上表面所有节点于中性点并施加7.5 N·m扭矩。模型测试阶段则在L3椎体上表面施加面载荷,压力方向垂直向下,大小为500 N[24],均匀分布在整个L3椎体的上终板。在垂直加载的同时于L3椎体上表面中性点并施加 7.5 N·m 扭矩,模拟前屈、后伸、左右侧弯和左右轴向旋转工况下腰椎生物力学状态。将模型导入ABAQUS软件中进行计算求解。主要观察指标:①腰椎活动范围(range of motion,ROM),用L4~L5节段角位移表示;②后路内固定和椎间植入物应力,直接记录各种工况下的Von Mises应力峰值。
2 结果 2.1 模型有效性验证对完整状态模型进行有效性验证,在7.5 N·m扭矩条件下,腰椎前屈、后伸、左右侧屈及左右旋转6种工况下L4~L5节段角位移的计算结果与Renner等的生物力学测试结果一致,均处于一个标准差范围内(图 2)。因此,我们认为本模型在一定条件下有效,可以应用于临床和实验研究。
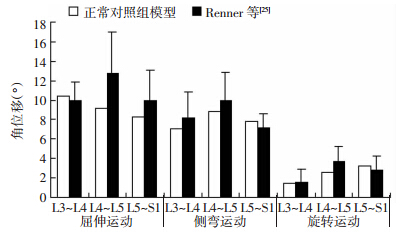 |
| 图 2 模型验证数据 |
各种模型在不同工况下L4~L5节段的角位移见图 3。未融合未固定模型(M1)的角位移均较INT状态明显增大,其中左旋转增加最明显,达到了INT模型的3.9倍。未融合固定模型(M2)较未融合未固定模型而言显著减少了固定节段的ROM数值。M2、M3和M4模型ROM较INT状态减少,其中融合固定模型(M3)中固定节段活动度减少最多,且尤以前屈、后伸时ROM减少显著。M3较M2状态角位移减少幅度较小。融合去固定模型(M4)与M3比较,除了前屈后伸状态角位移有部分增加之外,其余状态ROM改变不明显。
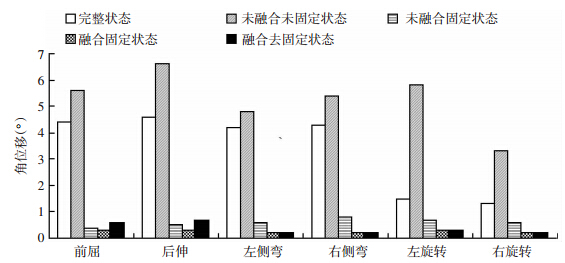 |
| 图 3 各模型在不同工况下L4~L5节段活动度(ROM) |
各种模型在不同工况下椎间植入物和后路椎弓根钉-棒系统的Von Mises应力峰值分别见图 4、5。对于椎间植入物而言,模型M1的应力峰值均高于其他模型,尤其在前屈状态和左旋转时差异明显;模型M3较模型M2在后伸状态中应力峰值下降明显,但是其他状态没有明显差异。模型M4较模型M3应力峰值有所增加,其中屈伸状态比较明显。模型M2内固定上Von Mises应力峰值明显高于模型M3,左侧弯螺钉应力峰值最大。
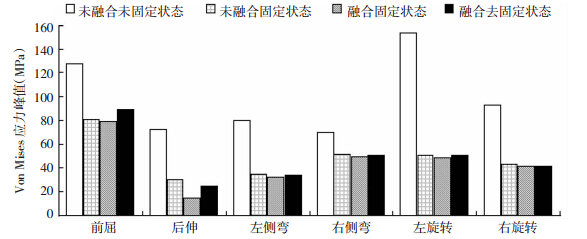 |
| 图 4 不同模型椎间植入物的Von Mises应力峰值 |
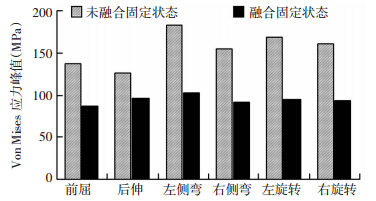 |
| 图 5 植骨融合前后后路内固定的Von Mises应力峰值 |
TLIF术中双侧椎弓根螺钉固定已成为该术式的主要固定方式。双侧椎弓根螺钉固定被用以提供足够的力学强度和融合节段的稳定性,提高椎间融合率,减少融合物的塌陷、移位和脱出。椎间融合术需要依靠植骨融合来完成良好的矫正及生理力线与稳定的重建,有学者认为内固定的矫正与固定只是暂时的,没有良好的植骨融合,螺钉迟早会断裂[26]。内固定的作用是促进植骨融合,一旦植骨融合,内植物的作用也随之消失,而随着患者术后活动量增加,脊柱前屈、后伸、侧屈及旋转载荷增加,可导致内固定的疲劳性断裂,因此主张在术后合适的时间去除内固定[14]。
TLIF手术中为了显露椎间盘,需要进行单侧或双侧的关节突关节切除术。关节突关节切除之后会显著影响节段的抗旋转稳定性。靳安民等[27]采用有限元方法研究小关节分级切除对腰椎稳定性的影响,结果发现小关节不同程度切除后,腰椎活动节段纤维环受影响最大的是轴向旋转,其次是后伸运动:单侧小关节全部切除时,其最大Von Mises应力分别上升了73.3%和47.07%,而双侧全切除时则分别上升了122.27%和97.36%。本研究中未融合未固定模型(M1)中所计算的结果与该实验结果相似,由于右侧关节突的切除,模型M1在各个工况下的节段活动度较完整模型均有显著的增加,特别是在左旋状态下ROM较完整状态增大了3.9倍,同时椎间植入物所承受Von Mises应力也显著高于其他模型。这一结果提示TLIF术后需要辅助以后路椎弓根螺钉内固定来提供节段的稳定性。
在双侧椎弓根螺钉固定模型(M2、M3)中,固定节段活动度较未融合未固定模型(M1)和完整模型(INT)均有明显的下降,特别是与M1模型的旋转状态相比较,固定模型有效地重建了关节突切除而丧失的节段稳定性。本研究结果也再次证实了双侧椎弓根螺钉固定可以提供有效的固定强度和稳定性。对于椎间植入物上应力峰值而言,固定模型较M1模型同样出现了显著下降,说明了椎间植入物承受的应力得到了后路椎弓根螺钉系统的有效分担。
本研究发现在椎间植骨融合后,固定节段的活动度会较未发生融合时有少量下降,而椎间植入物上的应力峰值也有所下降,但下降幅度较小。与此同时我们也发现后路内固定的应力峰值在融合之后出现了明显的下降,与文献报道的体内实验结果不一致[15, 16],该作者发现植骨融合发生前后椎弓根钉棒结构上载荷变化不明显。我们分析可能存在两方面的原因,一方面是手术方式的不同导致了结构生物力学特性的差异——本实验中应用的是TLIF手术模型,而在体实验应用的是椎体骨折模型和前路植骨模型,其双侧关节突关节完整而本实验TLIF手术模型的关节突结构却遭到了破坏。完整的关节突结构可以协同椎弓根钉棒结构形成有效的载荷分享,因此这种模式下内固定的载荷相比TLIF手术中钉棒固定的悬臂梁结构而言将获得有效的降低,这样就可能导致融合前后椎弓根钉棒结构上载荷改变不明显;另一方面是在体实验的复杂的肌肉韧带复合体的运动在有限元分析中无法进行有效的模拟,可能也是导致这一差异的原因,这也是离体生物力学研究存在的缺陷之一[6, 9]。
通过比较模型M3和模型M4的结果可以发现去掉内固定之后模型所发生的变化。从ROM数据可以看出,去掉后路固定之后节段的活动度没有明显的变化,仅在屈伸状态下有小幅度的上升,同时椎间植入物的应力峰值也仅在屈伸状态下出现了小幅度升高,并没有出现我们所预期的椎间植入物应力峰值大幅升高的结果。分析这一组数据我们可以得出,融合之后去除内固定对节段的活动度和椎间植入物的影响是有限的,钛合金椎弓根内固定系统的固定之下,没有出现我们所担心的应力遮挡效应,因此内植物去除之后所带来的获益是有限的。换个角度而言,在椎间植骨融合之后即使内固定出现断裂失效,其对TLIF手术总体的治疗效果的影响也是有限。随着脊柱外科微创观点和微创手术的普及,减少手术造成的患者创伤得到广大脊柱外科医生的重视,内固定取出术势必额外增加患者的手术创伤和治疗费用,同时考虑到钛合金内固定系统良好的生物相容性特点,我们建议在TLIF椎间植骨融合形成之后可以保留内固定而不用取出。
| [1] | Harms JG,Jeszenszky D.Die posteriore,lumbale,interkorporelle Fusion in unilateraler transforaminaler Technik[J].Oper Orthop Traumatol,1998,10(2):90-102. |
| [2] | Sim H B,Murovic J A,Cho B Y,et al.Biomechanical comparison of single-level posterior versus transforaminal lumbar interbody fusions with bilateral pedicle screw fixation:segmental stability and the effects on adjacent motion segments[J].J Neurosurg Spine,2010,12(6):700-708. |
| [3] | Ambati D V,Wright E K Jr,Lehman R A Jr,et al.Bilateral pedicle screw fixation provides superior biomechanical stability in transforaminal lumbar interbody fusion:a finite element study[J].Spine J,2014,[Epub ahead of print]. |
| [4] | Sethi A,Muzumdar A M,Ingalhalikar A,et al.Biomechanical analysis of a novel posterior construct in a transforaminal lumbar interbody fusion model an in vitro study[J].Spine J,2011,11(9):863-869. |
| [5] | Rouben D,Casnellie M,Ferguson M.Long-term durability of minimal invasive posterior transforaminal lumbar interbody fusion:a clinical and radiographic follow-up[J].J Spinal Disord Tech,2011,24(5):288-296. |
| [6] | Xiao Y X,Chen Q X,Li F C.Unilateral transforaminal lumbar interbody fusion:a review of the technique,indications and graft materials[J].J Int Med Res,2009,37(3):908-917. |
| [7] | Xu H,Ju W,Xu N,et al.Biomechanical comparison of transforaminal lumbar interbody fusion with 1 or 2 cages by finite-element analysis[J].Neurosurgery,2013,73(2 Suppl Operative):ons198-one205. |
| [8] | Chastain C A,Eck J C,Hodges S D,et al.Transforaminal lumbar interbody fusion:a retrospective study of long-term pain relief and fusion outcomes[J].Orthopedics,2007,30(5):389-392. |
| [9] | Xu H,Tang H,Guan X,et al.Biomechanical comparison of posterior lumbar interbody fusion and transforaminal lumbar interbody fusion by finite element analysis[J].Neurosurgery,2013,72(1 Suppl Operative):21-26. |
| [10] | Zhang Q,Yuan Z,Zhou M,et al.A comparison of posterior lumbar interbody fusion and transforaminal lumbar interbody fusion:a literature review and meta-analysis[J].BMC Musculoskelet Disord,2014,15:367. |
| [11] | Gologorsky Y,Skovrlj B,Steinberger J,et al.Increased incidence of pseudarthrosis after unilateral instrumented transforaminal lumbar interbody fusion in patients with lumbar spondylosis:Clinical article[J].J Neurosurg Spine,2014,21(4):601-607. |
| [12] | Yan D L,Pei F X,Li J,et al.Comparative study of PILF and TLIF treatment in adult degenerative spondylolisthesis[J].Eur Spine J,2008,17(10):1311-1316. |
| [13] | Xue H,Tu Y,Cai M.Comparison of unilateral versus bilateral instrumented transforaminal lumbar interbody fusion in degenerative lumbar diseases[J].Spine J,2012,12(3):209-215. |
| [14] | 王宇,靳安民,方国芳,等.腰椎椎弓根螺钉系统断裂的三维有限元分析[J].中国组织工程研究与临床康复,2008,12(48):9439-9442. |
| [15] | Rohlmann A,Graichen F,Weber U,et al.2000 Volvo Award winner in biomechanical studies:Monitoring in vivo implant loads with a telemeterized internal spinal fixation device[J].Spine (Phila Pa 1976),2000,25(23):2981-2986. |
| [16] | Rohlmann A,Graichen F,Bergmann G.Loads on an internal spinal fixation device during physical therapy[J].Phys Ther,2002,82(1):44-52. |
| [17] | Kim H J,Chun H J,Lee H M,et al.The biomechanical influence of the facet joint orientation and the facet tropism in the lumbar spine[J].Spine J,2013,13(10):1301-1308. |
| [18] | Denoziere G,Ku D N.Biomechanical comparison between fusion of two vertebrae and implantation of an artificial intervertebral disc[J].J Biomech,2006,39(4):766-775. |
| [19] | Grant J P,Oxland T R,Dvorak M F.Mapping the structural properties of the lumbosacral vertebral endplates[J].Spine (Phila Pa 1976),2001,26(8):889-896. |
| [20] | 郑琦,应小樟,石仕元,等.复杂性腰椎管狭窄症的有限元建模与分析[J].第三军医大学学报,2012,34(18):1897-1900. |
| [21] | Kim T Y,Kang K T,Yoon D H,et al.Effects of lumbar arthrodesis on adjacent segments:differences between surgical techniques[J].Spine (Phila Pa 1976),2012,37(17):1456-1462. |
| [22] | Tang S.Does TLIF aggravate adjacent segmental degeneration more adversely than ALIF?A finite element study[J].Turk Neurosurg,2012,22(3):324-328. |
| [23] | 陈志明,马华松,赵杰,等.腰椎单侧椎弓根螺钉固定的三维有限元分析[J].中国脊柱脊髓杂志,2010,20(8):684-688. |
| [24] | 敖俊,万磊,廖文波,等.腰椎间融合后路非对称与对称固定螺钉应力的有限元比较[J].中国组织工程研究,2013,17(9):1555-1562. |
| [25] | Renner S M,Natarajan R N,Patwardhan A G,et al.Novel model to analyze the effect of a large compressive follower pre-load on range of motions in a lumbar spine[J].J Biomech,2007,40(6):1326-1332. |
| [26] | 张光铂.浅谈脊柱内固定的应用与植骨融合[J].中国脊柱脊髓杂志,2002,12(5):325. |
| [27] | 靳安民,袁野,曹虹,等.单双侧小关节分级切除的有限元分析[J].中国临床解剖学杂志,2002,20(6):473-475. |



