原发性肝癌(hepatocellular carcinoma,HCC)为常见恶性肿瘤之一,其发病率及死亡率分别居第5位及第3位[1, 2]。经导管肝动脉化疗栓塞术(transcatheter hepatic arterial chemoembolization,TACE)目前为无法切除HCC的首选治疗方法[3, 4]。HCC常并存多支肝内和/或肝外肿瘤滋养动脉[5, 6],大网膜动脉(omental artery,OA)为较少见的肝外侧支肿瘤供血动脉之一。OA可起源于胃网膜左、右动脉或胰背动脉,交通吻合形成大网膜动脉弓而参与大网膜供血[5, 7]。OA中主要有4支参与HCC供血:大网膜右动脉(right omental artery,ROA)、大网膜中动脉(middle omental artery,MOA)、大网膜左动脉(left omental artery,LOA)和大网膜副动脉(accessory omental artery,AOA)[8]。目前与OA参与HCC供血相关的研究较少,但关于OA肿瘤供血支的发现、栓塞及术后疗效的研究对临床工作有重要指导作用。因此,本研究回顾性分析本院OA参与HCC血供的患者资料,以探讨OA参与HCC供血的影像特征及完全性栓塞治疗的有效性与安全性。 1 材料与方法 1.1 主要材料和试剂
我院2010年2月至2014年7月诊断为HCC并行TACE治疗2 934例,36例患者于41次治疗中发现OA参 与HCC供血,其中男性35例,女性1例;年龄18~ 75(50±11)岁。于第1~10次TACE治疗中发现OA参与HCC供血。患者均于术前签署TACE手术知情同意书。 1.2 设备与器材
1250MA DIGTEX PREMIER VC X线机 (日本岛津公司)、INFINIX 8000V X线机(日本东芝公司);5F RH 导管、4F YASHIRO超滑导管、2.7F progreat微导管(日本泰尔茂公司),Cobra C2导管(美国Cook公司)。 1.3 介入技术方法
采用Seldinger技术行股动脉穿刺,以5F RH导管及2.7Fprogreat微导管对肝内肿瘤滋养动脉实施超选择性TACE治疗;然后于右肾动脉、胃十二指肠动脉等行 DSA 检查,寻找是否存在肝外侧支肿瘤滋养动脉。参与肿瘤供血之OA动脉增粗、扭曲并向肿瘤部位走行,选择性插管至胃十二指肠动脉或胃网膜动脉造影较易发现OA肿瘤供血支起源位置及肿瘤染色,对于起源于脾动脉之LOA常于腹腔干动脉造影时发现,经血管造影证实后再行超选择性TACE治疗,最后再次造影证实OA肿瘤供血支完全闭塞。 1.4 术后随访及影像资料分析
术后2周内观察并记录患者栓塞后反应及并发症,术后1~3个月行CT/MRI增强检查,通过分析手术前、后MRI或CT、DSA等资料,记录肿瘤所在肝节段、病灶大小、是否侵犯肝包膜、OA参与肿瘤供血分支、术后肿瘤病灶碘油沉积及复发情况。采用肝癌改良实体肿瘤疗效评价标准(modified response evaluation criteria in solid tumors,mRECIST)[9]评价OA栓塞疗效:若病灶无强化则为完全缓解(complete response,CR);病灶强化半径至少减小30%为部分缓解(partial response,PR);既未达到缓解也未达到进展标准者为稳定(stable disease,SD);病灶强化半径至少增加30%为进展(progressive disease,PD)。若患者再次行TACE治疗,造影观察原OA是否完全闭塞,有无新生OA参与肿瘤供血。所有资料均由2位主治以上医师进行独立评估,若有异议则经过讨论达到一致。 2 结果 2.1 OA参与供血之HCC的影像特征
本组6名患者首次行TACE治疗时发现OA参与HCC供血者,余30名患者于第2~10次TACE治疗时发现,其中3名有2次TACE治疗时发现OA参与供血,1名有3次TACE治疗时均发现。OA供血之肿瘤病灶均侵犯并突破肝包膜外生生长,病灶位于肝右前叶、肝右后叶及肝左叶者分别为21、14例及6例,其中病灶位于肝S4、5段且于大网膜方向突破肝包膜者13例(图 1A),位于肝S5、6段且向下方外生生长者18例(图 1C)。肿瘤病灶直径大于5 cm者39例(95.1%),仅2例病灶直径小于5 cm,且发现于第 3次及第5次行TACE治疗时。
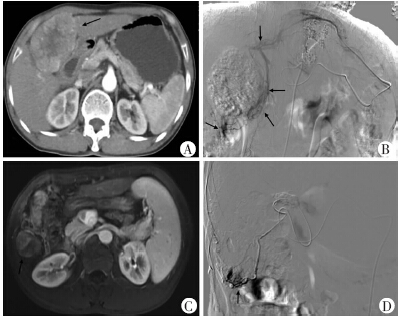 |
| A:CT增强示LOA参与肝左叶病灶供血,HCC病灶位于肝S4段,向大网膜方向突破肝包膜外(↑);B:LOA肿瘤供血支造影示肿瘤血管影,血管受推挤呈弧形走行(↑);C: MRI增强示ROA参与肝右叶病灶供血 HCC病灶位于肝S6段,向下方向突破肝包膜(↑);D:ROA肿瘤供血支造影示肿瘤血管及肿瘤染色影,肿瘤染色位于突破肝包膜区域(↑)图 1 OA参与HCC供血的影像学表现 |
本组53支OA参与HCC供血,32次TACE术中各仅发现1支OA参与供血,7次术中各发现2支OA参与供血,余2次术中分别发现3支及4支OA供血。OA起源较为固定,起源于胃网膜右动脉者48支,起源于胃网膜左动脉者5支。由于大网膜跨度大,OA各支可参与位于任意段肝脏肿瘤供血,本组中AOA(n=9)、 ROA(n=17)、MOA(n=17)及LOA(n=10)参与HCC供血(表 1),其中AOA参与供血病灶均位于肝右叶(图 2A、D);ROA、MOA及LOA参与肝左、右叶肿瘤病灶供血,与OA起源位置无明显关系。OA参与肿瘤供血血管造影可见:①腹腔干或胃十二指肠动脉造影时可见参与肿瘤供血OA明显增粗、扭曲(n=49,图 2A);②OA支向病灶方向走行僵硬(n=25,图 3A),或因肿瘤病灶大而受压呈弧形(n=13,图 1B);③OA支可于邻近病灶处发出多支小血管参与肿瘤供血(n=19,图 3B);④肿瘤染色位于病灶边缘处,多位于靠近或突破肝包膜区域(n=35,图 1D);⑤OA存在独立的肿瘤供血区(n=20),亦可与其余滋养动脉共同供血(n=33,图 3C)。
 |
| A:肝总动脉造影示AOA、ROA、MOA增粗、扭曲,向病灶方向走行(↑);B~D:分别超选择性插管至MOA、ROA、AOA肿瘤供血支造影示肿瘤血管及肿瘤染色影;E:完全性栓塞后行肝总动脉造影,原肿瘤血管及肿瘤染色影消失;F:4个月后再次TACE术时肝总动脉造影示肝右叶结节状及团块状肿瘤染色影(↑),未见肿瘤供血OA支图 2 参与HCC供血的OA行完全性化疗栓塞及再次手术血管造影 |
 |
| A:肝总动脉造影示MOA向病灶方向僵硬走行(↑);B: MOA肿瘤供血支造影示其发出2支肿瘤供血分支血管(↑);C:腹腔干动脉造影显示ROA增粗,且被肿瘤病灶向下推挤(↑);D:ROA肿瘤供血支造影示肿瘤血管及肿瘤染色影 图 3 参与HCC供血的OA血管造影表现 |
本组49支OA动脉于37次TACE治疗行超选择性插管至肿瘤供血分支深处,注入化疗药物-碘油乳化剂混悬液,并以150~350 μm聚乙烯醇颗粒行完全性 栓塞。2支OA因 与其他肿瘤供血动脉存在交通支而未再次插管栓塞,2支OA因痉挛狭窄而未能成功实施超选择性栓塞。患者于术后24 h出现腹痛(n=34)、恶 心呕吐(n=12)、发热(n=25)、右肩痛(n=2)、皮肤 瘙痒(n=1)、腹泻(n=3)等栓塞术后反应,未发现胃、小肠缺血、水肿甚至溃疡、穿孔、胰腺坏死等严重并发症。
本研究采用mRECIST方法,将28次行OA完全性化疗栓塞术后患者最近一次增强CT/MRI检查进行分析,其中CR9例,PR 13例,SD 2例,PD 4例,OA供血病灶栓塞有效率(response rate,RR) 为78.6%,肿瘤生长控制率(disease control rate,DCR)为85.7%。以OA是否独立供养肿瘤病灶分为2组(表 2),OA独立供血组中RR及DCR均明显高于共同供血组。肿瘤复发再次行TACE治疗15例,原OA肿瘤供血支全部完全闭塞,8例未见新生OA支(图 2),5例可见OA支向肿瘤病灶方向发出,但未见肿瘤血管及肿瘤染色影,仅2例可见新生OA参与肿瘤供血。
| OA参与肿瘤供血 | CR | PR | SD | PD | RR(%) | DCR(%) |
| OA独立供血 | 6 | 3 | 1 | 0 | 90.0 | 100.0 |
| OA与其他动脉 共同供血 | 3 | 10 | 1 | 4 | 72.2 | 77.8 |
| 总计 | 9 | 13 | 2 | 4 | 78.6 | 85.7 |
| RR:病灶栓塞有效率,RR =(CR+PR)/(CR+PR+SD+ PD);DCR:肿瘤生长控制率,DCR =(CR+PR+SD)/(CR+ PR+SD+PD) | ||||||
TACE术目前已成为HCC的主要治疗手段,能准确寻找并有效阻断肿瘤滋养动脉,特别是肝外侧支滋养动脉而取得满意疗效是其前提与技术保障[10]。虽然OA参与肿瘤供血较为少见,以往研究发现其发生率仅为0.68%~2.09%[11, 12, 13],本研究中发生率为1.4%(41/2 934),但关于OA参与肿瘤血供的影响因素及OA肿瘤供血支栓塞的临床价值的研究对指导介入手术临床工作尤为重要。 3.1 OA参与HCC供血的影响因素
OA参与HCC供血与肿瘤大小、外科手术及多次TACE治疗对病灶的刺激有关[7, 14],Won等[15]研究发现首次TACE治疗时OA参与HCC供血率为14.3%(3/21),本研究上述发生率为14.6%(6/41),且6例肿瘤病灶直径均大于5 cm。Gao等[13]认为肝动脉狭窄及闭塞可提高OA参与肿瘤供血的发生率,但本研究中肝动脉与OA共同参与肿瘤供血比例为65.9%(27/41),表明肝动脉狭窄及闭塞并不是OA参与供血的主要因素。本研究所有OA参与供血之肿瘤病灶均侵犯突破肝包膜外生生长,位于大网膜覆盖区域(S4、5、6)者占75.6%(31/41),也许能说明OA很少依靠肝脏韧带或肝裸区供血,而主要为大网膜与肿瘤粘连形成血供[5, 15],这与其他肝外侧支动脉参与肿瘤供血明显不同。本研究除AOA仅参与肝右叶肿瘤病灶供血外,ROA、MOA、LOA均可参与肝左、右叶供血,表明OA起源与肿瘤病灶位置所在无明显关系[16]。综上所述,我们认为多次治疗的大肝癌病灶位于肝S4~6段并突破肝包膜或侵犯大网膜时,应重视是否有OA参与肿瘤供血。 3.2 OA行超选择性插管及完全性栓塞的安全性
于腹腔干或胃十二指肠动脉造影时,正常OA多不显影或显影浅谈;当OA参与肿瘤供血时,该动脉增粗、迂曲,走行至肿瘤病灶区域,其远端分支区可见肿瘤染色。参与供血OA动脉常细长而扭曲,且多呈锐角起源于胃网膜动脉,故行超选择性插管较困难[11, 13],本研究插管成功率为92.5%(49/53),且尽量将微导管插入OA肿瘤供养分支深部直至造影证实未见肠胃壁染色影后才能实施完全性栓塞治疗。若插管技术不佳导致OA痉挛、形成夹层或闭塞,不仅会导致插管失败,还会增大新侧支形成的可能[15, 17]。而不进行超选择性插管,碘油化疗药及栓塞剂返流及误栓的几率则大大提高。本研究及以往研究均未发生小肠穿孔、坏死等严重并发症[7, 11, 18],以往研究发现2例患者术后CT提示碘油沉积于网膜,但也无与OA栓塞有关的严重并发症[15]。这是由于大网膜侧支血供丰富,误栓极少部分正常OA支不会引起网膜缺血、坏死,但若不进行超选择性栓塞,栓塞剂进入OA正常支或相交通的小肠动脉几率增加,从而增大小肠缺血、水肿甚至溃疡、穿孔的可能性。本研究仅3例出现腹泻症状,可能由于短暂性缺血导致小肠功能减弱。我们认为,只要能仔细防止栓塞剂返流误栓,超选择性栓塞OA肿瘤供血支安全性很高。 3.3 OA完全性栓塞的有效性
由于OA仅为众多HCC供血动脉之一,以生存率、生存时间[13]等评价OA栓塞的临床价值存在误差。OA成功栓塞仅能对其供血病灶产生影响,故本研究采用mRECIST方法,评估OA完全性栓塞的疗效。本研究发现OA供血病灶RR(74.2%)及DCR(80.6%)较前研究[15]均有所上升,单独供血肿瘤病灶的OA支完全性栓塞后,病灶无其他滋养动脉而迅速坏死,RR高达90%;多支动脉共同参与供血时,栓塞剂可通过交通动脉或肿瘤病灶阻塞其他动脉末梢,虽无法完全性栓塞,也能增强栓塞效果(RR=72.2%)。既往研究认为OA支无法行完全性栓塞[17],而本研究栓塞后再次造影证实OA均栓塞完全,其差异与栓塞材料有关,以往研究中所用栓塞剂为明胶海绵颗粒,直径较大,棱角欠光滑,而本研究栓塞剂为聚乙烯醇颗粒(150~350 μm),能充分达到毛细血管水平栓塞。再次行TACE治疗时造影15例,原OA肿瘤供血支全部闭塞,仅2例(13.3%)可见新生OA参与肿瘤供血。由此可见,完全性栓塞OA肿瘤供血支,能有效抑制其供血病灶的复发生长。
综上所述,OA作为较少见的肝外侧支肿瘤供血动脉之一,多参与位于肝S4~6段,并突破肝包膜或侵犯邻近大网膜的大肝癌供血,其血管造影特征明显,易于发现,但超选择性插管较困难。完全性栓塞OA肿瘤供血支安全性高,疗效可,尤其栓塞单独供血的OA效果更佳。
| [1] | El-Serag H B. Hepatocellular Carcinoma[J]. N Engl J Med, 2011, 365(12): 1118-1127. |
| [2] | Jemal A, Bray F, Center M M,et al. Global cancer statistics[J]. CA Cancer J Clin, 2011, 61(2): 69-90. |
| [3] | Murata S, Mine T, Sugihara F,et al. Interventional treatment for unresectable hepatocellular carcinoma[J]. World J Gastroenterol, 2014, 20(37): 13453-13465. |
| [4] | Nishikawa H, Kita R, Kimura T,et al. Transcatheter arterial chemoembolization for intermediate-stage hepatocellular carcinoma: clinical outcome and safety in elderly patients[J]. J Cancer, 2014, 5(7): 590-597. |
| [5] | 李强, 杨仁杰, 朱旭, 等. 肝外侧支动脉参与肝癌供血的介入治疗[J]. 中华肿瘤杂志, 2013, 35(8): 613-617. |
| [6] | Miyayama S, Matsui O, Taki K,et al. Extrahepatic blood supply to hepatocellular carcinoma: angiographic demonstration and transcatheter arterial chemoembolization[J]. Cardiovasc Intervent Radiol, 2006, 29(1): 39-48. |
| [7] | Miyayama S, Matsui O, Akakura Y,et al. Hepatocellular carcinoma with blood supply from omental branches: treatment with transcatheter arterial embolization[J]. J Vasc Interv Radiol, 2001, 12(11): 1285-1290. |
| [8] | 罗小平, 淦伟. 大肝癌大网膜动脉供血的DSA表现及其超选择性栓塞治疗的临床价值[J]. 实用放射学杂志, 2008, 24(11): 1565-1567. |
| [9] | Lencioni R, Llovet J M. Modified RECIST (mRECIST) assessment for hepatocellular carcinoma[J]. Semin Liver Dis, 2010, 30(1): 52-60. |
| [10] | Miyayama S, Yamashiro M, Okuda M,et al. Anastomosis between the hepatic artery and the extrahepatic collateral or between extrahepatic collaterals: observation on angiography[J]. J Med Imaging Radiat Oncol, 2009, 53(3): 271-282. |
| [11] | Paul S B, Gamanagatti S R, Mukund A,et al. Transarterial chemoembolization for hepatocellular carcinoma: Significance of extrahepatic collateral supply[J]. Indian J Cancer, 2011, 48(3): 339-344. |
| [12] | Chung J W, Kim H C, Yoon J H,et al. Transcatheter arterial chemoembolization of hepatocellular carcinoma: prevalence and causative factors of extrahepatic collateral arteries in 479 patients[J]. Korean J Radiol, 2006, 7(4): 257-266. |
| [13] | Gao S, Yang R J, Dong J H. Hepatocellular carcinoma with blood supply from parasitized omental artery: angiographic appearance and chemoembolization[J]. Chin J Cancer Res, 2012, 24(3): 207-212. |
| [14] | Miyayama S, Yamashiro M, Okuda M,et al. The march of extrahepatic collaterals: analysis of blood supply to hepatocellular carcinoma located in the bare area of the liver after chemoembolization[J]. Cardiovasc Intervent Radiol, 2010, 33(3): 513-522. |
| [15] | Won J Y, Lee D Y, Lee J T,et al. Supplemental transcatheter arterial chemoembolization through a collateral omental artery: treatment for hepatocellular carcinoma[J]. Cardiovasc Intervent Radiol, 2003, 26(2): 136-140. |
| [16] | Miyayama S, Yamashiro M, Shibata Y,et al. Variations in feeding arteries of hepatocellular carcinoma located in the left hepatic lobe[J]. Jpn J Radiol, 2012, 30(6): 471-479. |
| [17] | 田利, 王茂强, 李强, 等. 网膜支动脉参与肝癌供血的介入治疗研究[J]. 中国医药指南, 2009, 7(7): 13-14, 23. |
| [18] | 李强, 王茂强, 宋鹏, 等. 网膜动脉栓塞化疗在肝癌治疗中的价值[J]. 中华消化外科杂志, 2008, 7(6): 425-427. |



