脓毒症是一种由感染引起的全身炎症反应综合征,如不及时治疗和控制,可导致脓毒性休克及多器官功能不全综合征(multiple organ dysfunction syndrome,MODS),甚至死亡,是目前重症监护室中患者死亡的主要原因之一[1, 2]。脓毒症的发生率和死亡率较高,据统计全球每天约有1 400人死于脓毒症,其病死率超过50%[3, 4]。尽管近年对脓毒症的认识和治疗有很大进展,但其死亡率始终居高不下[5]。研究显示约40%脓毒症患者出现不同程度的心脏功能障碍,是脓毒症致多器官功能衰竭和患者死亡的重要原因之一。据调查显示伴心血管功能障碍的脓毒症患者,其病死率明显高于单纯脓毒症患者,高达70%~90%[6, 7, 8]。尽管国内外学者针对脓毒症心脏功能障碍的机制做了大量研究,也提出了许多治疗措施,但治疗效果仍不理想。因此寻找治疗脓毒性休克心脏功能障碍的药物措施,对降低脓毒症的发生率和死亡率具有重要意义。
垂体中叶素(intermedin,IMD)是降钙素基因相关肽(calcitonin gene-related peptide,CGRP)家族的新成员,由Roh 2003年于硬骨鱼体内发现。IMD由148个氨基酸组成,在体内可降解为IMD1-53,为其主要的活性片段[9]。研究提示,IMD可通过抗氧化应激、抑制细胞凋亡发挥对缺血再灌注心脏功能的保护作用[10]。但IMD对脓毒症心脏功能是否有保护作用,目前尚少见相关研究报道。本实验采用盲肠结扎穿孔术(cecal ligation and puncture,CLP)复制大鼠脓毒症模型,观察IMD对脓毒症大鼠心脏功能的影响。 1 材料与方法 1.1 脓毒症模型的建立
SD大鼠120只,雌雄不拘,12月龄,体质量220 g左右,由第三军医大学大坪医院野战外科研究所实验动物中心提供,用CLP复制腹膜炎脓毒症模型。实验大鼠常规消毒腹部,暴露盲肠,将盲肠内的粪便向盲肠末端充实,在距末端0.7 cm处用无菌丝线结扎,采用无菌的7号针头在已结扎盲肠远端中央处贯通穿刺后,将盲肠按原位送回腹腔,缝合皮肤,放回笼中饲养。模型制作12 h后,用15 mg/kg戊巴比妥钠腹腔麻醉大鼠,股动脉插管监测平均动脉血压(mean arterial blood pressure,MAP),当MAP下降30%或以上,模型成功。本实验模型成功率为70%。股静脉插管用于输液,插管完成后稳定10 min,从插管中注入500 U/kg的肝素钠全身抗凝。假手术组大鼠除不结扎盲肠和穿孔外,其余操作同模型组。 1.2 IMD对脓毒症大鼠存活时间和存活率的影响
SD大鼠80只,按随机数字表法将动物分为假手 术组、CLP组、CLP+CT组、CLP+CT+E-IMD组、CLP+CT+L-IMD组,每组16只。假手术组大鼠除不结扎盲肠和穿孔外,其余操作同模型组;常规治疗组在CLP 12 h 后给予液体LR ∶HES(2 ∶1)输注,同时给予抗生素头孢呋辛钠(100 mg/kg)和血管活性药物多巴胺(DA),使平均动脉压(MAP)>70 mmHg,中心静脉压维持在8 mmHg。 IMD早期治疗和晚期治疗分别为在CLP手术结束时和CLP 12 h后给予IMD(5×10-7g/kg)进行输注,输注3 h后结扎血管,缝合肌肉层和皮肤层,观察72 h内死亡大鼠的平均存活时间和存活率的变化。 1.3 IMD对脓毒症大鼠血气和心输出量(cardiac output,CO)、心脏指数(cardiac index,CI)、每搏指数(stroke index,SI)、氧供、氧耗的影响
SD大鼠40只,具体分组和各组处理同1.2。通过右颈总动脉将热稀释导管插入左心室连接心输血量测定仪测定CO和心率(HR),并通过公式计算心脏指数[CI=CO÷S[13],体表面积:S=K×W2/3(cm2),其中K=9.1;W:体质量(g)[14]]和每搏指数(SI=CI÷ HR[15])。同时在输液3 h点采集股动脉血和股静脉血,用血氧分析仪测定动脉血气:氧分压p(O2)、动脉血氧饱和度(SaO2)、碳酸氢根(HCO-3)、碱剩余(BE),以及静脉血气[静脉血氧饱和度(SvO2)和血红蛋白(Hb)],计算组织氧供(DO2=CI×13.4×Hb×SaO2)[13]和组织氧耗[VO2=CI×13.4×Hb×(SaO2-SvO2)][13]。 1.4 统计学处理
数据用x±s表示,包括CO、CI、SI、氧供、氧耗、血气均用重复测量单因素或双因素方差分析,存活时间和存活率通过中位数和四分位数间距进行分析,用Kruskal-Wallis检验进行比较。 2 结果 2.1 IMD对脓毒症大鼠72 h内死亡动物的平均存活时间及存活率的影响
CLP后超过一半的动物在6 h内死亡,无动物存活时间超过72 h,72 h内死亡大鼠的平均存活时间约4.83 h。 常规治疗后(CLP+CT),动物的存活率无显著提高,其72 h内死亡大鼠的平均存活时间为8.55 h。早期(CLP+CT+E-IMD)给予IMD比晚期给予IMD效果 更好,其中72 h内死亡大鼠的平均存活时间为23.15 h,72 h 存活率为31.2%(5/16);晚期(CLP+CT+L-IMD)给予IMD 在72 h内死亡大鼠的平均存活时间为16.67 h,72 h存活率为25.0%(4/16)。见图 1。
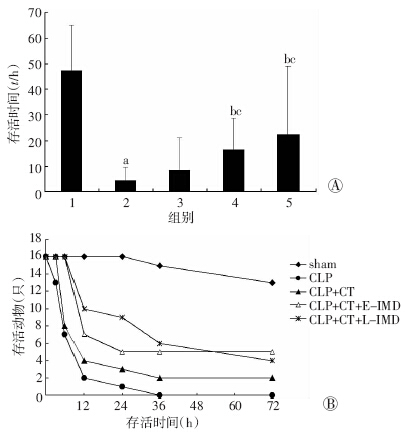 |
| 1:假手术组;2:CLP组;3:CLP+CT组;4:CLP+CT+E-IMD;5:CLP+CT+L-IMD A:死亡大鼠的平均存活时间比较;B:存活率比较 a:P<0.01,与假手术组比较;b:P<0.05,与CLP比较; c:P<0.05,与常规治疗组比较 图 1 各组脓毒症大鼠72 h内的存活时间和存活率变化 |
CLP后,大鼠的心功能指标包括CO、CI和SI均明显降低,常规治疗(CLP+CT)可以部分改善脓毒症大鼠的心功能;CLP+CT+E-IMD和CLP+CT+L-IMD组CO、CI、SI均可明显升高,CLP+CT+E-IMD组可以明显拮抗由脓毒症所致的心功能降低。见图 2。
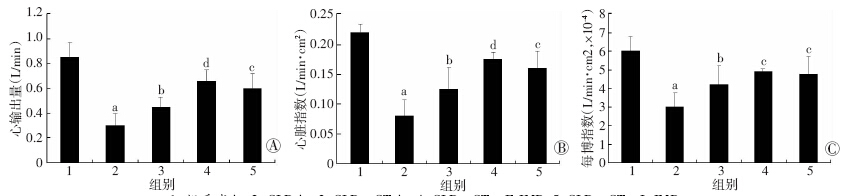 |
| 1:假手术组;2:CLP组;3:CLP+CT组;4:CLP+CT+E-IMD;5:CLP+CT+L-IMD A:各组心输出量的比较;B:各组心脏指数的变化;C:各组每博指数的比较 a:P<0.01,与假手术组比较;b:P<0.05,与CLP比较;c:P<0.01,与CLP比较;d:P<0.05,与常规治疗组比较 图 2 各组脓毒症大鼠心功能指标的比较 |
与假手术组比较,CLP大鼠的氧供和氧耗明显降低,降低率分别为68.2%和71.8%;CLP+CT组可以部分升高脓毒症大鼠的氧供和氧耗,但与CLP组相比无明显增加;IMD早期(CLP+CT+E-IMD)和晚期(CLP+ CT+L-IMD)治疗后,氧供和氧耗明显升高,早期给予IMD治疗效果更好,与CLP大鼠相比,早期给予IMD 后,氧供和氧耗分别升高了148.9%和172.2%。见图 3。
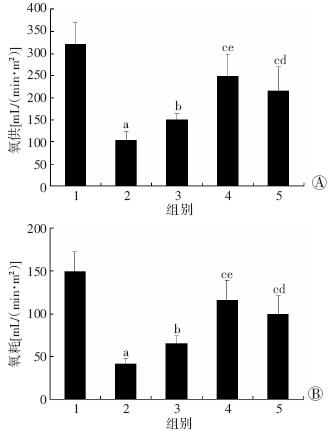 |
| 1:假手术组;2:CLP组;3:CLP+CT组;4:CLP+CT+E-IMD;5:CLP+CT+L-IMD A:各组氧供的变化;B:各组氧耗的变化a:P<0.01,与假手术组比较;b:P<0.05,与CLP比较;c:P<0.01,与CLP比较;d:P<0.05,与常规治疗组比较;e:P<0.01,与常规治疗组比较 图 3 各组脓毒症大鼠氧供和氧耗的比较 |
脓毒症后,大鼠的血气指标包括p(O2)、SaO2、BE和HCO-3均有变化,但不显著(表 1)。与脓毒症比较,IMD复苏后,p(O2)和SaO2有所升高,IMD对脓毒症大鼠的氧分压和氧饱和度有改善作用。
| 组别 | CLP模型前 | CLP末 | 治疗3 h |
| PaO2(mmHg) | 99.7±9.5 | ||
| 假手术组 | 98.3±8.6 | 97.5±8.1 | |
| CLP | 89.3±9.5a | 86.3±8.3 | |
| CLP+CT | 90.2±10.3a | 92.1±4.4 | |
| CLP+CT+E-IMD | 95.9±10.2 | 101.3±9.7bd | |
| CLP+CT+L-IMD | 92.9±9.8a | 98.8±6.5bd | |
| SaO2(%) | |||
| 假手术组 | 95.5±1.3 | 94.6±2.4 | 96.5±4.7 |
| CLP | 93.7±3.3 | 98.4±7.9 | |
| CLP+CT | 88.4±3.1a | 91.0±4.8 | |
| CLP+CT+E-IMD | 90.6±2.1a | 93.9±8.3b | |
| CLP+CT+L-IMD | 95.5±1.0 | 99.0±6.5bd | |
| BE(mmol/L) | |||
| 假手术组 | -1.0±2.8 | -1.9±1.6 | 0.9±3.6 |
| CLP | -1.7±2.2 | 0.3±3.3 | |
| CLP+CT | -1.9±2.1 | 0.4±4.4 | |
| CLP+CT+E-IMD | -0.9±2.5 | -0.6±5.4 | |
| CLP+CT+L-IMD | -0.8±2.4 | 2.7±3.1 | |
| HCO3-(mmol/L) | |||
| 假手术组 | 20.3±4.5 | 17.9±2.1 | 23.5±3.6 |
| CLP | 18.2±1.5 | 22.6±4.0 | |
| CLP+CT | 16.5±2.2 | 23.5±4.0 | |
| CLP+CT+E-IMD | 17.5±1.1 | 22.6±4.6 | |
| CLP+CT+L-IMD | 17.1±1.5 | 25.8±3.4 | |
| a:P<0.01,与假手术组比较;b:P<0.05,与CLP比较;c:P<0.05,与常规治疗组比较 | |||
脓毒症的发生率和死亡率均很高,心功能障碍是脓毒症患者的死亡原因之一,目前尚无有效的治疗措施。本研究旨在通过CLP模型来观察IMD对脓毒症大鼠心脏功能的保护作用。结果发现:脓毒症后大鼠的心脏功能、组织氧供和氧耗以及动物的存活时间、存活率明显降低;常规治疗(包括液体复苏、抗感染以及使用血管活性药物)后,尽管可以提高大鼠的动脉血压和中心静脉压,但大鼠的心脏功能、组织氧供、氧耗以及动物的存活时间和存活率增加不明显;IMD治疗后可以显著提高大鼠的存活时间和存活率,改善心脏功能,增加组织氧供和氧耗;早期给予IMD对大鼠的心脏功能、氧供、氧耗、血气的效果均比晚期给予IMD治疗效果好。
IMD作为降钙素基因相关肽家族的成员之一,以往研究证实,其对缺血再灌注心脏功能具有保护作用。Zhao等[10]研究发现IMD作用可改善缺血再灌注引起的脂质过氧化损伤,提高心肌细胞存活和抑制心肌细胞凋亡。又有研究证实IMD预处理能降低缺血再灌注损伤大鼠心肌组织的乳酸脱氢酶(LDH)和丙二醛(MDA)水平,升高cAMP,发挥对缺血再灌注心肌的保护作用[11]。进一步研究显示IMD对心肌缺血再灌注的保护作用主要通过减少炎症和氧化应激,增加抗凋亡蛋白表达,减少线粒体释放细胞色素C到胞浆,抑制线粒体途径介导的心肌细胞凋亡。本研究发现IMD
能提高脓毒症大鼠的存活,改善大鼠的心脏功能,增加组织氧的供应和利用,可能与IMD通过抗氧化应激和抑制细胞凋亡发挥对心肌的保护作用有关,至于其具体机制有待进一步研究。
本研究虽然发现IMD对脓毒症大鼠心脏功能有改善作用,但是仍存在不足。第一、因为大鼠个体的差异性,或者麻醉的问题,导致在CLP模型成功后,大鼠的状态有所差异;第二、本研究仅仅观察了IMD对脓毒症大鼠心脏功能的影响,未涉及相关机制研究。
| [1] | Dellinger R P, Levy M M, Rhodes A, et al. Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock, 2012[J]. Intensive Care Med, 2013, 39(2): 165-228. |
| [2] | 高戈, 冯喆, 常志刚, 等. 2012国际严重脓毒症及脓毒性休克诊疗指南[J]. 中华危重病急救医学, 2013, 25(8): 501-505. |
| [3] | Moore L J, McKinley B A, Turner K L, et al. The epidemiology of sepsis in general surgery patients[J]. J Trauma, 2011, 70(3): 672-680. |
| [4] | Klein-Klouwenberg P M, Ong D S, Bonten M J, et al. Classification of sepsis, severe sepsis and septic shock: the impact of minor variations in data capture and definition of SIRS criteria[J]. Intensive Care Med, 2012, 38(5): 811-819. |
| [5] | Barochia A, Solomon S, Cui X, et al. Eritoran tetrasodium (E5564) treatment for sepsis: review of preclinical and clinical studies[J]. Expert Opin Drug Metab Toxicol, 2011, 7(4): 479-494. |
| [6] | Rudiger A, Singer M. The heart in sepsis: from basic mechanisms to clinical management[J]. Curr Vasc Pharmacol, 2013, 11(2): 187-195. |
| [7] | Zanotti-Cavazzoni S L, Hollenberg S M. Cardiac dysfunction in severe sepsis and septic shock[J]. Curr Opin Crit Care, 2009, 15(5): 392-397. |
| [8] | Omar A A, El-Shahat N, Ramadan M M. Cardiac functions in patients with sepsis and septic shock[J]. The Egyptian Heart Journal, 2012, 64(4): 191-196. |
| [9] | Pan C S, Yang J H, Cai D Y, et al. Cardiovascular effects of newly discovered peptide intermedin/adrenomedullin 2[J]. Peptides, 2005, 26(9): 1640-1646. |
| [10] | Zhao L, Peng D Q, Zhang J, et al. Extracellular signal-regulated kinase 1/2 activation is involved in intermedin1 53 attenuating myocardial oxidative stress injury induced by ischemia/reperfusion[J]. Peptides, 2012, 33(2): 329-335. |
| [11] | Li H, Bian Y, Zhang N, et al. Intermedin protects against myocardial ischemia-reperfusion injury in diabetic rats[J]. Cardiovas Diabetol, 2013, 12: 91. |



