2.400038 重庆,第三军医大学西南医院体检中心;
Department of Infectious Diseases, Southwest Hospital, Third Military Medical University, Chongqing, 400038, China;
肺血管重构是肺动脉高压的病理生理基础,肺动脉平滑肌细胞(pulmonary artery smooth muscle cells,PASMCs)过度增殖是肺血管重构的重要病理环节。研究表明,香烟烟雾中的主要成分尼古丁成分促进机体炎症反应和氧化应激状态[1, 2],从而引起PASMCs的增殖[3, 4],在吸烟相关慢性阻塞性肺病患者肺血管重构中起关键作用。二甲双胍是糖尿病的一线降糖药物,近年来的研究发现,二甲双胍有着降血糖作用以外的诸多效应,尤其是其抗炎、抗氧化效应备受关注[5, 6]。流行病学调查结果显示二甲双胍具有不依赖降血糖效应的心血管保护作用,其机制可能与其抗炎、抗氧化应激机制有关。动物实验显示二甲双胍抑制野百合碱和低氧环境下对肺循环有保护作用,抑制肺动脉高压形成[7];鉴于二甲双胍的抗炎、抗氧化应激效应,及其对肺循环的保护作用,我们推测二甲双胍可能对于香烟烟雾暴露下的肺血管重构具有抑制效应。本研究通过观察二甲双胍对尼古丁诱导的PASMCs增殖、细胞上清IL-6、TNF-α和ROS产生的影响,并对二甲双胍的主要作用底物AMPK表达和活性水平进行检测,明确二甲双胍对尼古丁暴露下PASMCs增殖、炎症反应和氧化应激状态的影响,并探讨及其可能机制。
1 材料与方法 1.1 主要材料和试剂DMEM/F-12培养基与胎牛血清(fetal calf serum,FBS)购自HyClone公司。小鼠抗α-actin、FITC标记山羊抗小鼠IgG(H+L)、活性氧(ROS)检测试剂盒及CCK-8试剂盒购自碧云天生物技术公司。尼古丁、Anti-phospho-AMPK α(pThr172)抗体购自美国Sigma公司。大鼠IL-6、TNF-α ELISA试剂盒购自上海沪尚生物公司。Anti-AMPK alpha 1+AMPK alpha 2购自美国Abcam公司。辣根过氧化物酶标记羊抗小鼠二抗购自中衫生物科技公司。Western blot相关试剂购自碧云天公司,实验动物SD大鼠由新桥医院实验动物中心提供。Bio-Rad电泳仪、FACS Verse流式细胞仪及Bio-Rad imark酶标仪由新桥医院全军呼吸内科研究所提供。
1.2 实验方法 1.2.1 PASMCs的培养与鉴定雄性SD大鼠购自第三军医大学实验动物中心,体质量200~300 g,戊巴比妥麻醉后引臼处死,无菌条件下取出肺动脉,刮去内膜和外膜,采用组织块贴壁法培养。细胞生长融合后,用0.25%的胰酶消化离心后传代。用免疫组化法对细胞内平滑肌肌动蛋白α-actin进行荧光标记,激光共聚焦镜下观察细胞质内α-actin蛋白呈绿色高表达并呈丝状分布,证实细胞为SD大鼠PASMCs。所有实验均采用3~8代细胞。
1.2.2 实验分组取3~8代对数生长期细胞,用含10%FBS的DMEM/F-12培养液置于37 ℃、5%CO2孵箱内培养,取第4代对数生长期PASMCs胰酶消化,计数后每孔加100 μL以4×104接种到96孔板贴壁24 h,无血清培养基处理24 h后,更换10%FBS的DMEM培养基,用不同浓度尼古丁(0.01、0.1、1.0、10 μmmol/L)处理细胞。每组设3个复孔,恒温培养箱培养48 h,加入CCK-8试剂10 μL培养30 min,酶标仪在450 nm波长测定各孔光密度值。确定尼古丁诱导PASMCs增殖的最佳浓度。为进一步观察二甲双胍对尼古丁诱导PASMCs增殖的影响及可能机制,实验分组如下:①对照组:加含10%FBS DMEM/F-12培养液;②尼古丁处理组(N组);③尼古丁+二甲双胍处 理组(N+M组):加入尼古丁处理时同时加入2 mmol/L 二甲双胍预处理。
1.2.3 IL-6和TNF-α表达检测取第4代PASMCs 胰酶消化后,以4×106接种到6孔板贴壁24 h,无血清培养基处理24 h后,更换含10%FBS的DMEM培养 基并 加入0.1 μmmol/L 尼古丁处理,分别在0,30 min,1 h,3 h,6 h,12 h时收集细胞上清,3000 r/min离心10 min后放入-20 ℃冰箱保存。用ELISA检测试剂盒检测并用酶标仪在450 nm波长测定各孔光密度值。取第4代对数生长期PASMCs胰酶消化,用上述 实验条件处理细胞,按实验分组加入二甲双胍干预后,在6 h 用酶标仪(Bio-Rad imark)检查各孔光密度值。
1.2.4 活性氧(ROS)表达检测取第4代PASMCs 胰酶消化后,以4×105接种到6孔板贴壁24 h,无血清培养基处理24 h后,更换含10%FBS的DMEM培养 基并加入0.1 μmmol/L尼古丁处理,分别在0,30 min,60 min,3 h,6 h加入含有10 μmmol/L无血清DCFH-DA原位装载探针,于恒温培养箱孵育20 min,之后用无血清培养液洗涤3次,以充分去除未进入细胞的DCFH-DA。收集细胞,并设阳性对照(加Rosup),用流式细胞仪(FACS Verse)观察平均荧光强度。另取第4代对数生长期PASMCs胰酶消化,用上述实验条件处理细胞,按实验分组加入二甲双胍干预后,60 min用流式细胞仪检测平均荧光强度。
1.2.5 Western blot检测AMPK蛋白表达和活性取第4代PASMCs胰酶消化后,以4×105接种到25 cm2培养瓶贴壁24 h,无血清培养基处理24 h后,更换含10%FBS的DMEM培养基并加入尼古丁使其终浓度为0.1 μmmol/L。分别在0、1、6、12、24 h提取细胞总蛋白,每孔上样20 μg以4%~12%的十二烷基硫酸钠-聚丙酰胺凝胶(SDS-PAGE)电泳分离,转膜后,5%BSA的TBST封闭2 h,加入一抗(1 ∶200稀释)4 ℃孵育过夜,洗膜3次,二抗室温孵育1 h,ECL试剂盒显带分析并测灰度值,实验重复3次;另取第4代PASMCs胰酶消化后,用上述实验条件处理细胞,按实验分组加入二甲双胍干预后,在以上相同的时间点检测各组灰度值。
1.3 统计学分析实验结果采用x±s表示,通过SPSS 13.0软件进行数据统计分析,各组间比较用单因素方差分析。
2 结果 2.1 PASMCs培养及鉴定光镜下可见,传代培养的第4代细胞呈长梭形,及典型的“峰-谷”样生长,(图 1)。PASMCs免疫荧光染色后,可见细胞质内α-actin被FITC标记的荧光 抗染成绿色,与细胞长轴平行的丝状分布,胞核经DAPI染为蓝色(图 2)。上述实验证实培养的细胞为PASMCs。
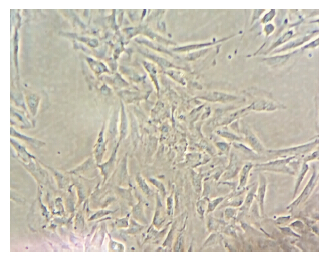 |
| 图 1 PASMCs培养结果 (倒置显微镜×200) |
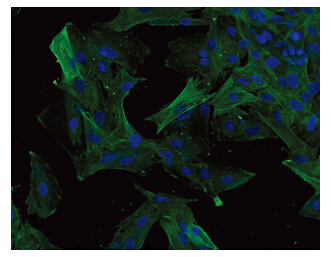 |
| 图 2 免疫荧光鉴定α-actin在细胞内的表达 (激光共聚焦显微镜×400) |
经CCK-8法检测不同浓度的尼古丁对PASMCs增殖的影响,尼古丁处理48 h结果发现: 0.1 μmmol/L尼古丁后促PASMCs增殖效应最强;高浓度的尼古丁反而抑制PASMCs增殖 (P<0.05,图 3)。因此,我们确定0.1 μmmol/L尼古丁为诱导PASMC增殖的最佳浓度。2 mmol/L二甲双胍预处理后能显著逆转尼古丁的促增殖作用(P<0.05),与N组相比,加入二甲双胍24、48、72 h时抑制率分别为14%、16%、28%(表 1)。
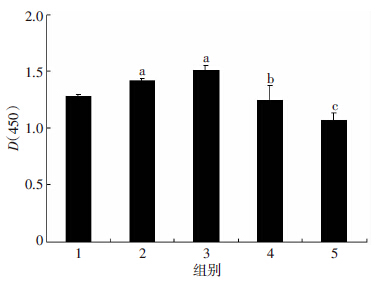 |
| 1:对照组;2:0.01 μmmol/L组;3:0.1 μmmol/L组;4:1.0 μmmol/L组;5:10 μmmol/L组 a:P<0.05,与对照组比较;b:P<0.05,与0.01 μmmol/L尼古丁组及0.1 μmmol/L尼古丁组比较;c:P<0.05,与对照组比较 图 3 CCK-8检测不同浓度的尼古丁刺激48 h对PASMCs增殖的影响 |
| 组别 | 24 h | 48 h | 72 h |
| 对照组 | 1.02±0.05 | 1.04±0.03 | 1.09±0.05b |
| N组 | 1.19±0.04a | 1.20±0.06a | 1.23±0.05a |
| N+M组 | 1.03±0.03b | 1.01±0.03b | 0.94±0.10b |
| a:P<0.05,与同时相点对照组比较;b:P<0.05,与同时相点N组比较 | |||
尼古丁可明显促进PASMCs中IL-6、TNF-α表达,在6 h达峰值(图 4),而二甲双胍组在6 h时能显著降低IL-6、TNF-α的表达(P<0.05,图 5)。
 |
| 1:对照组;2:30 min;3:60 min;4:3 h;5:6 h;6:12 h a:P<0.05,与对照组比较 图 4 尼古丁处理不同时间PASMCs对细胞分泌IL-6、TNF-α表达的影响 |
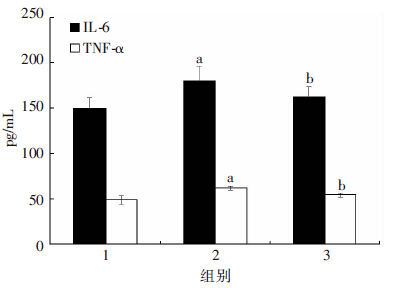 |
| 1:对照组;2:N组;3:N+M组 a:P<0.05,与对照组比较,b:P<0.05,与N组比较 图 5 二甲双胍对尼古丁诱导PASMCs分泌IL-6、TNF-α表达的影响 |
使用DCFH-DA探针检测尼古丁处理PASMCs后 细胞内ROS浓度,结果发现尼古丁可明显诱导PASMCs 中ROS的生成 。尼古丁处理30 min时,细胞内ROS水平与对照组相比开始升高(P<0.05),在60 min时达高峰(P<0.05),随后开始下降,见图 6。因此,我们选取60 min这一关键时间点观察二甲双胍对尼古丁诱导的 ROS产生是否存在影响作用。结果显示尼古丁诱导PASMCs内ROS的生成水平能明显被二甲双胍抑制(P<0.05)。 各组细胞ROS生成水平:对照组 (100±9.494 97),尼古丁组(236±10.879),尼古丁加二甲双胍组( 134±7.979)。各组细胞ROS生成量以对照组为100%基准值进行计算和统计学分析。
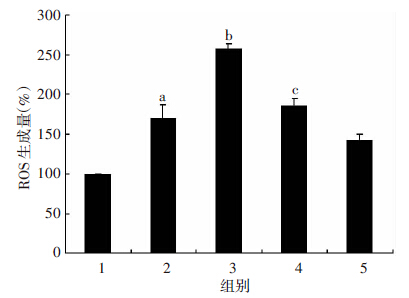 |
| 1:对照组;2:30 min;3:60 min;4:3 h;5:6 h a:P<0.05,与对照组比较,b:P<0.05,与30 min组比较; c:P<0.05,与60 min组比较 图 6 流式细胞仪检测不同时间点尼古丁诱导PASMCs产生ROS水平变化 |
与对照组相比,尼古丁处理后1 h时,磷酸化AMPK水平明显升高,随后逐渐减低,而AMPK表达水平在各时相点无明显变化。见图 7。而在二甲双胍同时处理的PASMCs中,PASMCs中磷酸化AMPK水平在尼古丁处理1、6、12、24 h均持续活化。与对照组相比,处理12 h后磷酸化AMPK水平有明显升高(P<0.05),与12 h组相比,24 h组磷酸化AMPK水平明显降低(P<0.05),各组AMPK表达水平未发生明显变化。见图 8。
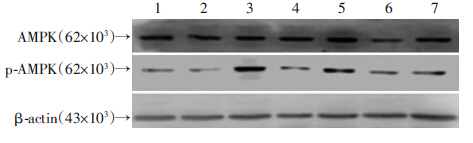 |
| 1:对照组;2:30 min;3:60 min;4:3 h;5:6 h;6:12 h;7: 24 h 图 7 Western blot检测不同时间点PASMCs AMPK活化情况 |
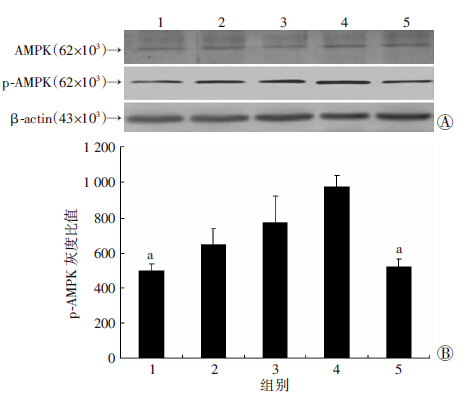 |
| 1:对照组;2:1 h;3:6 h;4:12 h;5:24 h A:Western blot检测结果,B:半定量分析结果 a: P<0.05,与12 h组比较 图 8 Western blot检测二甲双胍干预不同时间点 PASMCs AMPK活化情况 |
80% ~85% 慢性阻塞性肺病患者与吸烟有关,研究发现吸烟致慢性阻塞性肺病患者的早期无低氧阶段,甚至在肺功能正常阶段,就已经出现了肺血管重构;香烟烟雾中的主要成分尼古丁引起炎症反应和氧化应激,进一步引起IL-6、TNF-α和ROS的过表达,导致血管平滑肌细胞增殖。有研究证实,尼古丁可激活NF-κB通路,上调炎症因子IL-6及TNF-α的表达[8, 9]。 Brandes等[10]研究发现,尼古丁可通过NADPH氧化酶和线粒体途径,诱导内皮细胞产生内源性ROS。炎症因子、ROS与肺动脉平滑肌细胞增殖密切相关。IL-6可通过诱导VEGF的表达而促进肺动脉平滑肌的增殖[11]; 孟亮等[12]在研究中发现,IL-6过表达的PASMCs中TIMP1(tissue inhibitor of metalloproteinases 1)、基质金属蛋白酶(MMPs)、I型胶原(CollagenI)表达增加,促进血管平滑肌细胞细胞增殖及迁移;TNF-α可诱导血管平滑肌细胞内基质金属蛋白酶过表达,调控其增殖[13];TNF-α过表达可诱导内皮细胞活化,通过刺激IL-6释放,促进血管平滑肌细胞增殖[14]。有证据表明,ROS可诱导eNOS表达减少及活性降低,也直接灭活内皮源性NO,导致NO的明显降低,促使血管舒缩功能障碍,导致血管壁结构改变,同时促进平滑肌细胞增殖[15]。本实验结果发现 0.1 μmmol/L尼古丁促PASMCs增殖的同时,促进PASMCs IL-6、TNF-α的表达和释放,PASMCs中ROS生成明显增加;提示尼古丁促进PASMCs中炎症反应和氧化应激,诱导PASMCs增殖。
调控细胞能量代谢平衡的腺苷酸活化蛋白激酶(AMP-activated protein kinase,AMPK)的抗炎、抗氧化应激效应近年来备受关注。越来越多的证据表明,AMPK活性较低与机体高氧化应激和炎症状态密切相关,AMPK与体循环疾病如动脉粥样硬化和球囊损伤后再狭窄中的研究结果显示上调AMPK活性保护血管内皮细胞功能,抑制平滑肌细胞增殖[16]。本研究中我们采用尼古丁处理PASMCs1h后,磷酸化AMPK表达一过性升高,而后逐渐降低,同时伴随着PASMCs ROS生成、IL-6、TNF-A水平升高;尼古丁引起AMPK的短暂活化,可能是因为尼古丁诱发了炎症反应和氧化应激,触发了细胞的自我保护机制,致使AMPK活性一过性升高,随着AMPK的活化降低,其不足以抑制炎症因子和ROS持续高表达,导致肺动脉平滑肌细胞增殖;由此我们推测上调AMPK活性可能抑制尼古丁诱导PASMCs中的氧化应激和炎症反应,进而抑制PASMCs增殖。
二甲双胍是治疗糖尿病的一线降糖药物。AMPK的上游激酶是LKB1,是二甲双胍的作用底物[17];二甲双胍可以活化LKB1/AMPK信号通路。Agard等[7]研究显示传统降糖药物Metformin(AMPK激活剂)抑制野百合碱和低氧诱导的肺动脉高压形成,此项研究虽然未直接探讨其机制,但推测其机制可能与AMPK激活有关。一系列动物实验和临床研究表明,降脂药他汀类药物抑制吸烟所致的肺血管重构和肺动脉高压形成,其部分机制也可能与AMPK激活有关。本研究使用尼古丁处理PASMCs组同时加入二甲双胍,与单纯尼古丁处理组相比,磷酸化AMPK在尼古丁处理24 h仍然处于较高水平;且二甲双胍可显著抑制尼古丁诱导的PASMCs中IL-6、TNF-α释放和ROS生成(P<0.05);同时PASMCs增殖明显受到抑制(P<0.05)。表明二甲双胍抑制尼古丁诱导PASMCs中的氧化应激和炎症反应,进而抑制PASMCs增殖。与尼古丁处理组p-AMPK一过性升高相比,二甲双胍处理组维持AMPK的持续磷酸化,最终抑制尼古丁暴露下PASMCs的炎症反应和氧化应激及过度增殖。
综上所述,本研究结果初步从体外研究证实二甲双胍有效抑制尼古丁诱导PASMCs中的氧化应激和炎症反应,进而抑制PASMCs增殖。其机制可能与二甲双胍上调AMPK的活性相关[18],但是否存AMPK以外的其他机制尚需进一步研究。如能进一步从体内研究或临床研究证实二甲双胍能够抑制或逆转吸烟相关肺 血管重构,将对于开拓Metformin的临床新用途及慢性阻塞性肺病相关肺动脉高压的早期防治具有重要意义。
| [1] | 老启芳, 钟小宁, 何志义, 等.肺功能正常吸烟者和慢性阻塞性肺疾病患者肺腺泡动脉炎症特征[J].中华内科杂志, 2011, 50(10): 839-844. |
| [2] | MacNee W. Pathogenesis of chronic obstructive pulmonary disease[J].Proc Am Thorac Soc, 2005, 2(4): 258-266. |
| [3] | Lee J H, Lee D S, Kim E K, et al. Simvastatin inhibits cigarette smoking-induced emphysema and pulmonary hypertension in rat lungs[J].Am J Respir Crit Care Med, 2005, 172(8): 987-993. |
| [4] | Wu H, Yang S, Wu X, et al. Interleukin-33/ST2 signaling promotes production of interleukin-6 and interleukin-8 in systemic inflammation in cigarette smoke-induced chronic obstructive pulmonary disease mice[J]. Biochem Biophys Res Commun, 2014, 450(1): 110-116. |
| [5] | Isoda K, Young J L, Zirlik A, et al.Metformin inhibits proinflammatory responses and nuclear factor-kappaB in human vascular wall cells[J]. Arterioscler Thromb Vasc Biol, 2006, 26(3): 611-617. |
| [6] | Krymskaya V P, Snow J, Cesarone G, et al.mTOR is required for pulmonary arterial vascular smooth muscle cell proliferation under chronic hypoxia[J]. FASEB J, 2011, 25(6): 1922-1933. |
| [7] | Agard C, Rolli-Derkinderen M, Dumas-de-La-Roque E, et al. Protective role of the antidiabetic drug metformin against chronic experimental pulmonary hypertension[J]. Br J Pharmacol, 2009, 158(5): 1285- 1294. |
| [8] | Wang Y, Zhang F, Yang W, et al. Nicotine induces pro-inflammatory response in aortic vascular smooth muscle cells through a NF-κB/osteopontin amplification loop-dependent pathway[J]. Inflammation, 2012, 35(1): 342-349. |
| [9] | Li Q, Zhou X D, Kolosov V P, et al. Nicotine reduces TNF-α expression through a α7 nAChR/MyD88/NF-?B pathway in HBE16 airway epithelial cells[J].Cell Physiol Biochem, 2011, 27(5): 605-612. |
| [10] | Brandes R P, Weissmann N, Schroder K. Nox family NADPH oxidases in mechano-transduction: mechanisms and consequences[J]. Antioxid Redox Signal, 2014, 20(6): 887-898. |
| [11] | Steiner M K, Syrkina O L, Kolliputi N, et al. Interleukin-6 overexpression induces pulmonary hypertension[J].Circ Res, 2009, 104(2): 236-244. |
| [12] | 孟亮, 于波, 李阳, 等. IL-1β在细胞坏死过程中对血管平滑肌细胞I型胶原形成的影响及机制研究[J].医学分子生物学杂志, 2014, 11(1): 26-31. |
| [13] | Wright J L, Tai H, Wang R, et al. Cigarette smoke upregulates pulmonary vascular matrix metalloproteinases via TNF-alpha signaling[J]. Am J Physiol Lung Cell Mol Physiol, 2007, 292(1): L125- L133. |
| [14] | 韩伟, 张明泳, 冯伟伟, 等. 内皮细胞条件培养液对血管平滑肌细胞增殖和ICAM-1、IL-1β分泌的影响[J].中国现代医学杂志, 2013, 23(3): 15-18. |
| [15] | Aggarwal S, Gross C M, Sharma S, et al. Reactive oxygen species in pulmonary vascular remodeling[J]. Compr Physiol, 2013, 3(3): 1011-1034. |
| [16] | Kim E J, Choi Y K, Han Y H, et al. RORα suppresses proliferation of vascular smooth muscle cells through activation of AMP-activated protein kinase[J]. Int J Cardiol, 2014, 75(3): 515-521. |
| [17] | Bang S, Chen Y, Ahima R S, et al. Convergence of IPMK and LKB1-AMPK signaling pathways on metformin action[J]. Mol Endocrinol, 2014, 28(7): 1186-1193. |
| [18] | Coughlan K A, Valentine R J, Ruderman N B, et al. AMPK activation: a therapeutic target for type 2 diabetes?[J]. Diabetes Metab Syndr Obes, 2014, 24(7): 241-553. |



