2 421000 湖南 衡阳, 南华大学附属第一医院骨科
2 Department of Orthopaedics, First Affiliated Hospital of South China University, Hengyang, Hunan Province, 421000, China
神经干细胞(neural stem cells,NSCs)具有自我更新、干性维持和分化为神经系统三大主要神经细胞亚群的特性[1, 2]。近年来研究表明:NSCs在脑内存在于侧脑室壁的室管膜下区(subventricular zone,SVZ)和海马的齿状回区,尤其是SVZ区的NSCs可在脑组织受到损伤(如脑缺血、脑出血、脑外伤)后激活、增殖、分化为神经前体细胞(neuroblasts)向损伤灶迁移,整合于损伤的神经网络系统中,修复损伤的神经网络结构并可发挥相应的神经功能[3, 4, 5]。尽管研究证实其在脑组织损伤后的功能,但脑组织的修复功能仍然有限,大部分患者仍不能取得实质性的功能恢复[6, 7]。因此,激活内源性NSCs的增殖和/或体外培养NSCs行细胞替代治疗,为治疗脑组织损伤带来了新希望,开创了新的治疗方法,越来越受到研究者的关注。
青蒿琥酯(artesunate,ART)是半倍萜内酯化合物青蒿素的水溶性衍生物,现代研究发现,其具有高效、低毒的抗疟作用,易通过血脑屏障,在临床中被广泛用于疟疾的治疗,尤其对抢救和治疗脑型疟和恶性疟等疗效显著[8, 9]。而其对NSCs的影响却不清楚。我们前期的预实验证明其对NSCs的增殖有一定作用,但其机制不明,而PI3K-Akt是经典的与细胞增殖和存活密切相关的信号。本研究利用体外实验探讨ART对NSCs增殖的影响以及PI3K-Akt信号转导通路在其中的作用,以了解ART通过NSCs在脑组织损伤后修复中的可能作用和机制,旨在为临床转化提供一定的实验依据。 1 材料与方法 1.1 实验动物与材料 1.1.1 实验动物
25只SPF级孕14.5 d的SD大鼠由第三军医大学实验动物中心提供。手术过程及处死方式严格遵循国际通用实验动物使用指南及第三军医大学实验动物管理使用规定。 1.1.2 药品与试剂
Nestin抗体(Abcam公司,ab6142);GFAP抗体(武汉三鹰公司,16825-1-AP);Olig2抗体(武汉三鹰公司,13999-1-AP);Doublecortin抗体(Abcam公司,ab18723 );p-Akt抗体、Akt抗体(CST,4691);GAPDH抗体(北京中杉金桥公司,TA-08);Ki-67抗体(Abcam公司,ab15580);FITC-山羊抗小鼠二抗、CY3山羊抗兔二抗(北京中杉金桥公司);DMEM/F12(Thermo scientific公司);碱性成纤维细胞生长因子(bFGF,PeproTech公司);表皮生长因子(EGF,PeproTech公司);LY294002(MCE公司,HY-10108);CCK-8(日本DOJINDO公司)。 1.1.3 实验器材
低温离心机(美国Thermo scientific);倒置荧光显微镜(日本 Olympus);多功能酶标仪(美国 Thermo scientific);37 ℃、5% CO2培养箱(美国 Thermo Forma公司);激光共聚集显微镜(德国Carl Zeiss);Western blot电泳设备(美国Bio-Rad公司)。 1.2 方法 1.2.1 孕SD大鼠SVZ区NSCs的培养及鉴定
孕SD大鼠,水合氯醛50 mg/kg行腹腔注射麻醉,75%酒精消毒后,取出胚胎。在解剖显微镜下,以嗅球为中心矢状位纵切,在显微镜下以脑室壁为参照,取出SVZ区。0.25%胰酶37 ℃消化12 min,10%FBS终止消化,完全培养基(DMEM/F12+20 ng/mL bFGF+20 ng/mL EGF+2% B27)重悬,用5 mL枪头小心吹打细胞悬液12~15次,经台盼蓝染色后细胞计数,调整为1×106/mL,移入5% CO2、37 ℃恒温孵箱中培养。细胞传代以Accutase(Gibco公司,美国)消化,并半量换液,在培养5~7 d将细胞球或单细胞接种至10 μg/mL 多聚鸟氨酸包被的激光共聚焦培养皿中,行Nestin、DCX、GFAP、Olig2 Ki-67免疫荧光染色。第 9天换用添加不同浓度ART培养基进行分组干预。 1.2.2 采用CCK-8法检测ART对NSCs增殖作用
取对数期生长的NSCs,以8 000/100 μL接种于预先用10 μg/mL多聚鸟氨酸包被的96孔板。设置空白对照组、400 nmol/L、800 nmol/L、1.6 μmol/L、3.2 μmol/L组,孵育 24 h后,每孔加入10 μL CCK-8,孵育2.5 h 后,读取D(450)值。依照同样的方法,设置如下4组:空白对照组、LY294002组、800 nmol/L ART组和800 nmol/L ART+10 μmol/L LY294002组研究PI3K-Akt信号通路对NSCs增殖的影响。
1.2.3 Western blot检测PI3K-Akt通路在调控大鼠室管膜下区NSCs的增殖的作用p>取培养第9天的NSCs进行不同条件的干预,设置空白对照组、LY294002组、 800 nmol/LAR组、800 nmol/LART+10 μmol/L LY294002组。培养24 h后,提取总蛋白,测定蛋白浓度,取20 μg蛋白样品,上样、跑胶、转膜,封闭,加入不同一抗4 ℃孵育过夜;洗膜,孵育二抗,ECL显影液在ChemiDocXR+凝胶成像仪采集信息,并通过Image Lab程序分析条带,以检测各组Nestin、Akt及p-Akt蛋白的表达水平。 1.2.4 免疫荧光
各组细胞采用4%多聚甲醛固定,透膜,封闭后孵育相应的一抗在4 ℃孵育过夜,漂洗后孵育二抗复染细胞核封片,行荧光显微镜或激光共聚焦显微镜检测,分别在100倍镜下观察ki-67+细胞数目并拍照。 1.3 统计学分析
数据以x±s表示,采用SPSS 18.0统计软件,多组间比较行单因素方差分析。 2 结果 2.1 NSCs的培养和免疫荧光鉴定
NSCs悬浮培养,可见明显的神经干细胞球悬浮生长,NSCs球形态呈圆形,折光性好(图 1);免疫荧光细胞鉴定结果显示:大部分细胞表达NSCs的标志物Nestin(图 2A);去除生长因子及添加1%胎牛血清诱 导分化5~7 d后,可以观察到早期神经元细胞的标志物DCX(图 2B)、星形胶质细胞的标志物GFAP(图 2C) 及少突胶质细胞的标志物Olig2(图 2D)。
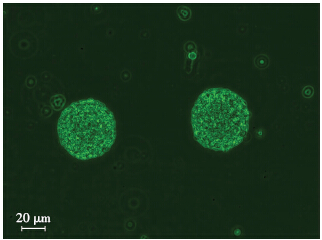 |
| 图 1 倒置显微镜下观察所培养的神经干细胞球形态 |
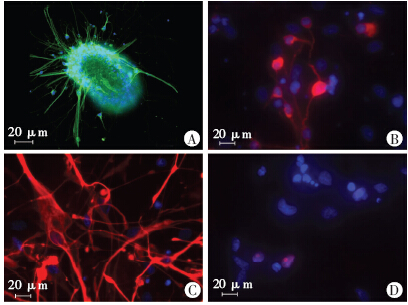 |
| A:Nestin;B:DCX;C:GFAP;D:Olig2;A:激光共聚焦;B~D:荧光显微镜图 2 免疫荧光染色观察神经干细胞、神经元细胞、胶质细胞、少突胶质细胞形态及标志物表达 |
ART在800 nmol/L浓度可促进NSCs的增殖(P<0.05),在设置的1.6、3.2 μmol/L浓度时,与对照组比较,差异无统计学意义(图 3)。CCK-8检测结果表明:在加入LY294002后,细胞增殖明显抑制,而在800 nmol/L ART组细胞增殖与前面的结果相符,且在先加入800 nmol/L ART 24 h,再加入10 μmol/L LY294002 24 h后,检测结果显示D(450)值与空白对照组相当(图 4)。在此基础上,设置如上分组,采用Ki-67免疫荧光染色方法,进一步确认PI3K-Akt通路在其中的作用(图 5),二者结果证实:PI3K-Akt通路在ART对NSCs增殖的作用中有重要作用。
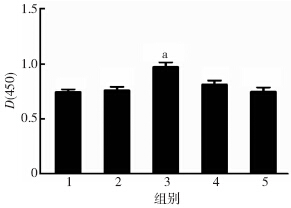 |
| 1:空白对照组; 2: 400 nmol/L组;3:800 nmol/L组;4:1.6 μmol/L组;5:3.2 μmol/L组;a:P<0.05,与空白对照组比较图 3 CCK-8法检测不同浓度ART对NSCs增殖的影响 |
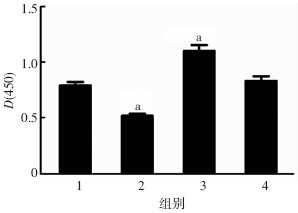 |
| 1:空白对照组;2:LY294002组;3:800 nmol/LAR组;4:800 nmol/L ART+10 μmol/L LY294002组;a:P<0.05,与空白对照组比较图 4 CCK-8法检测PI3K-Akt通路对ART对NSCs 增殖的影响 |
 |
| 图 5 Ki-67免疫荧光染色法检测PI3K-Akt通路在ART对NSCs增殖的影响(荧光显微镜) |
Western blot检测结果显示:应用800 nmol/L ART干预后,与其他各组比较,Nestin、p-Akt蛋白表达量均有明显增加(P<0.05),但当加入10 μmol/L LY294002 作用后,二者表达水平下降至空白对照组水平;与空白对照组比较,LY294002组Nestin、p-Akt蛋白表达量下降(P<0.05,图 6)。
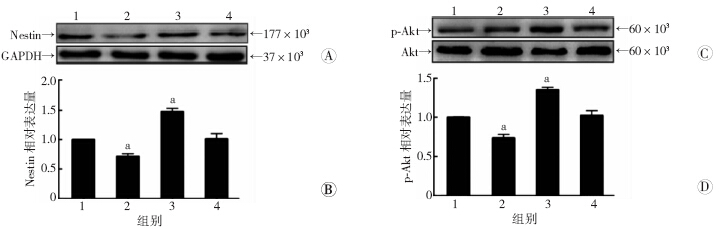 |
| 1:空白对照组;2:LY294002组;3:800 nmol/L ART组;4:800 nmol/L ART+10 μmol/L LY294002组;a:P<0.05,与空白对照组比较 A: Western blot检测Nestin表达;B:Nestin表达半定量分析;C:Western blot检测p-Akt表达;D:p-Akt表达半定量分析 图 6 Western blot检测各组NSCs中p-Akt、Nestin蛋白的表达 |
SVZ区是脑内NSCs的主要富集区之一,在脑组织受到损伤后,该区的NSCs可显著增殖,通过放射式(radial)向损伤灶及其周边迁移,并分化成熟为神经元整合于受损神经网络,发挥相应的功能[10, 11, 12, 13]。
ART可通过血脑屏障,且高效、低毒,临床上用于重型疟疾的治疗[14, 15],效果显著。而ART是否可通过调节机体内存在的内源性NSCs,从而在脑组织损伤后对神经修复起到促进作用及其可能机制,目前尚不清楚。本实验结果发现:ART对NSCs增殖的影响具有浓度依赖性,并随ART浓度的升高对NSCs增殖的增殖作用不显著,且促进NSCs增殖的作用浓度为800 nmol/L。
既往研究证明ART可通过PI3K-Akt信号转导通路影响气管平滑肌细胞的增殖,对哮喘患者具有积极的治疗作用[16]。本实验结果提示LY294002可抑制空白对照组NSCs增殖,而在促增殖作用明显的800 nmol/L ART组加入LY294002后可抵消ART作用带来的增殖效应,初步确认PI3K-Akt信号在ART对NSCs增殖中的作用。Western blot检测以上所结果证实LY294002可通过降低p-Akt的蛋白水平而减少Nestin蛋白的表达。
有研究显示2.5 μmol/L ART作用于神经鞘瘤细胞48 h,可明显降低其活性[17]。另有研究表明10 μmol/L ART作用于胰腺癌细胞、MiaPaCa-2和BxPC-3细胞24 h 后,均可使其活性下降至少25%[18]。据此本实验中设置的1.6 μmol/L及3.2 μmol/L ART两组,CCK-8检测光密度值降低的现象,我们考虑为ART的细胞毒性作用影响了细胞的活力,这一推测有待于接下来的实验中进行确认。
本研究结果提示ART可能在神经创伤后血管神经网络的修复中具有一定的作用。接下来尚需进行ART对SVZ区NSCs迁移和分化的影响及其机制研究,并进行ART作用系列时间的研究,以确定其安全性。本研究初步揭示了ART对SVZ区NSCs增殖的影响及信号机制,拓展了ART应用的空间,从另一侧面证实ART不仅可用于疟疾的治疗和肿瘤的研究,也为中枢神经系统损伤的药物辅助治疗开辟了新道路,提供了新策略。
| [1] | Gage F H. Mammalian neural stem cells[J]. Science, 2000, 287(5457): 1433-1438. |
| [2] | Ming G L, Song H. Adult neurogenesis in the mammalian brain: significant answers and significant questions[J]. Neuron, 2011, 70(4): 687-702.〖HJ1.7mm〗 |
| [3] | Arvidsson A, Collin T, Kirik D,et al. Neuronal replacement from endogenous precursors in the adult brain after stroke[J]. Nat Med, 2002 , 8(9): 963-970. |
| [4] | Astrup J, Siesjo B K, Symon L. Thresholds in cerebral ischemia-the ischemic penumbra[J]. Stroke, 1981, 12(6):723-725. |
| [5] | Briona L K, Dorsky R I. Radial glial progenitors repair the zebrafish spinal cord following transection[J]. Exp Neurol, 2014, 256: 81-92. |
| [6] | Lim P A, Tow A M. Recovery and regeneration after spinal cord injury: a review and summary of recent literature[J]. Ann Acad Med Singapore, 2007, 36(1): 49-57. |
| [7] | 陈飞, 王皓香, 向鑫, 等. 姜黄素对神经干细胞Wnt/βcatenin信号通路表达影响的离体研究 [J]. 第三军医大学学报, 2014, 36(8): 764-768. |
| [8] | 田樱, 魏振兴, 吴照华. 中药青蒿化学成分的研究[J]. 中草药, 1982, 13(2): 9-11. |
| [9] | 郭兴伯, 符永新, 陈沛泉, 等. 青蒿琥酯片治疗恶性疟疾100 例的临床观察[J]. 中华医学杂志, 1989, 69(9): 515-516. |
| [10] | Gould E. How widespread is adult neurogenesis in mammals?[J]. Nat Rev Neurosci, 2007, 8(6): 481-488. |
| [11] | Arvidsson A, Collin T, Kirik D,et al. Neuronal replacement from endogenous precursors in the adult brain after stroke[J]. Nat Med, 2002, 8(9): 963-970. |
| [12] | Parent J M, Vexler Z S, Gong C,et al. Rat forebrain neurogenesis and striatal neuron replacement after focal stroke[J]. Ann Neurol, 2002, 52(6): 802-813. |
| [13] | Paton J A, Nottebohm F N. Neurons generated in the adult brain are recruited into functional circuits[J]. Science, 1984, 225(4666): 1046-1048. |
| [14] | 张丽, 郑以山, 李娟, 等. 血液滤过联合青蒿琥酯治疗2例重症恶性疟疾的体会[J]. 内科急危重症杂志, 2013, 19(6): 375-376. |
| [15] | 牛艳红 王玉斌. 青蒿琥酯治疗维和人员疟疾109例疗效观察[J]. 中国预防医学杂志, 2009, 10(8): 764-765. |
| [16] | Tan S S, Ong B, Cheng C,et al. The antimalarial drug artesunate inhibits primary human cultured airway smooth muscle cell proliferation[J]. Am J Respir Cell Mol Biol, 2014, 50(2): 451-458. |
| [17] | Button R W, Lin F, Ercolano E,et al. Artesunate induces necrotic cell death in schwannoma cells[J]. Cell Death Dis, 2014, 5: e1466. |
| [18] | Youns M, Efferth T, Reichling J,et al. Gene expression profiling identifies novel key players involved in the cytotoxic effect of Artesunate on pancreatic cancer cells[J]. Biochem Pharmacol, 2009, 78(3): 273-283. |



