膀胱疼痛综合征/间质膀胱炎(bladder pain syndrome /interstitial cystitis,BPS/IC)是一种病因不明的膀胱慢性炎症性疾病,该疾病临床症状表现为尿急、尿频、盆腔疼痛以及其他不适为特点[1]。关于BPS/IC的病理生理假说有:上皮损伤,毒性物质损害,神经炎症,自身免疫紊乱等,但上述假说也无法完全阐述BPS/IC的具体发病机制,故对BPS/IC尚无特效的治疗手段和方法[2]。目前来说膀胱内药物[二甲基亚砜(dimethyl sulfoxide,DMSO),西施泰]灌注是治疗BPS/IC较为有效的手段和方法,但DMSO在我国尚未得到运用。研究表明BPS/IC膀胱组织有过量炎症介质如IL-6,TNF-a等表达[3],这提示炎症反应参与了该疾病的发生。DMSO是一种无色的有机溶剂,具有较好的渗透性,目前发现DMOS具有较强的干扰自由基生成,清除已生成的自由基、降低炎症介质和细胞因子,发挥抗炎症和氧化应激反应作用[4, 5]。据此,本研究采用鱼精蛋白(protamine sulfate,PS)诱导的大鼠IC模型,阐述DMSO对IC的治疗作用及其相关机制,以便为临床运用提供科学依据。 1 材料与方法 1.1 实验材料 1.1.1 主要试剂
SD雌性大鼠购自第三军医大学大坪医院野战外科研究所实验动物中心,全蛋白提取试剂盒购自凯基公司,Western blot凝胶试剂盒购自碧云天生物技术公司,PS购自美国 Sigma公司,乌拉坦购自美国Sigma公司,异戊巴比妥钠购自德国Merck公司,TNF-α、L-1B、SOD2、 GSH 兔抗大鼠以及β-actin小鼠抗大鼠抗体购自美国SantaCruz公司,IL-6兔抗大鼠购自于Abcom公司,HRP和羊抗鼠二抗购自北京中杉公司,ECL化学发光显色液购自美国Thermo公司。 1.2 方法 1.2.1 动物模型建立
SD雌性大鼠48只,体质量220~250 g,按随机数字表法分为正常组、鱼精蛋白灌注组(PS组)、DMSO灌注组(PS+DMSO组)、盐水灌注组(NS组),每组12只大鼠。正常组大鼠未给予任何处理;PS组用使用生理盐水溶解PS按照0.5 mL,30 mg/mL的PS膀胱内灌注并在膀胱内保留30 min;PS+DMSO组使用50% DMSO溶解PS按照0.5 mL,30 mg/mL的PS膀胱内灌注并在膀胱内保留30 min ;NS组用0.5 mL生理盐水膀胱灌注并保留30 min,各组大鼠每周处理1次,连续处理4周。各组大鼠用5%异戊巴比妥钠腹腔注射麻醉后硬膜外导管经大鼠尿道膀胱灌注。4周后其中6只大鼠膀胱组织被收集并称取湿质量,计算膀胱湿质量与大鼠体质量之比(膀胱mg/大鼠体质量g),随后将膀胱标本分为若干份用于后续实验;另外6只大鼠被用于尿动力学研究。 1.2.2 HE和甲苯胺蓝染色
将收集的大鼠膀胱(n=6)标本组织置于10%福尔马林液中固定,在梯度酒精脱水后石蜡包埋并切片(5 μm)用于HE和甲苯胺蓝染色。对于HE染色切片,在光镜下随机选取5个视野,观察炎症及黏膜损伤指数并进行炎症评分,评分标准参照文献[6],甲苯胺蓝染色用于肥大细胞计数研究,计数标准为在200倍光镜下随机选取5个视野,统计视野中肥大细胞数目。病理学检测和评价由对本实验不了解的病理医师完成。 1.2.3 Western blot检测
取各组部分大鼠膀胱组织40 mg,全蛋白提取试剂盒提取膀胱组织总蛋白。Western blot检测SOD2、 GSH-Px、 IL-6、IL-1B、TNF-α表达量,具体方法参见文献[7]。抗体浓度为SOD2(1 ∶1 000),GSH (1 ∶1 000),IL-6(1 ∶600),IL-β1(1 ∶800)、TNF-α(1 ∶1 000),β-actin(1 ∶1 000),LC3B(1 ∶600),山羊抗鼠二抗(1 ∶3 000),山羊抗兔二抗(1 ∶4 000)。 1.2.4 大鼠尿动力学检测
大鼠尿动力学检测采用文献[8, 9]报道的方法。1.2g/kg乌拉坦皮下注射,麻醉大鼠后硬膜外将导管置入大鼠膀胱,连接好多道生理信号采集处理系统,向大鼠膀胱内以速度为8 mL/h 灌注生理盐水并记录大鼠膀胱基线压(BP)、最大膀胱收缩压(MP)、收缩间歇 (ICI)、排尿频率(MF)、膀胱容量(BC)。 1.2.5 大鼠肌条实验研究
新鲜的膀胱组织修剪为6 mm×2 mm×2 mm大小的肌条,将肌条悬挂于装有Kreb’s营养液的37℃恒温水浴槽中,下端固定于槽底,上段连接张力传感器,并将传感器连接到多通道信号采集器上,Kreb’s液中通95% O2和5% CO2混合气体。孵育10 min后给予肌条0.75 g初始张力,记录肌条收缩的幅度和频率。 1.3 统计学处理
实验数据处理采用SPSS 16.0统计软件,数据以x±s表示,多组间差异使用单因素方差分析或非参数检验。 2 结果 2.1 各组大鼠膀胱湿质量和膀胱湿质量/体质量比值变化
如表 1所示:与正常组相比,PS组和NS组膀胱湿质量和膀胱湿质量/体质量比值显著增加(P<0.05),其中PS组较为严重;然而PS+DMSO组膀胱湿质量(P<0.05)和膀胱湿质量/体质量比值得到显著改善(P>0.05)。 2.2 组织学改变情况
HE染色(图 1)结果显示PS组和NS组都表现出上皮损伤,炎细胞浸润,黏膜及固有层明显水肿,炎症评分显著增加(表 1,P<0.05),其中PS灌注组更为严重;而PS+DMSO治疗组表现为上皮组织有较好的完整性,炎细胞浸润和组织水肿明显减轻。甲苯胺蓝染色(图 2)结果显示PS组和NS组都表现固有膜和肌层大量肥大细胞浸润数目显著增加(表 1,P<0.05),其中PS灌注组更为严重,而PS+DMSO治疗组表现为肥大细胞浸润显著减少,上述结果提示DMSO有较好的保护作用。
 |
| A:正常组;B:NS组;C:PS组;D:PS+DMSO灌注组 图 1 各组大鼠膀胱组织病理学变化 (HE×200) |
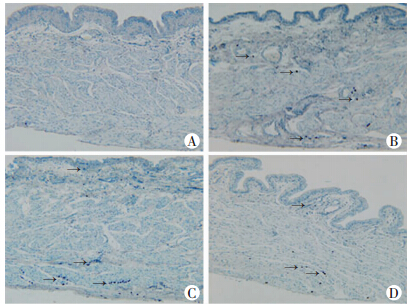 |
| A:正常组;B:NS组;C:PS组;D:PS+DMSO灌注组; ↑:示肥大细胞 图 2 各组大鼠膀胱组织甲苯胺蓝染色计数肥大细胞(×200) |
组别 | 膀胱湿质 量(mg) | 膀胱湿质量/ 体质量比值 (mg/g) | 炎症评分 (分) | 肥大细胞 计数(个) |
| 正常组 | 85.33±5.85 | 0.37±0.03 | 0.17±0.41 | 1.83±0.75 |
| NS组 | 149.33±10.78a | 0.69±0.06a | 1.83±0.41ab | 11.33±1.21ab |
| PS组 | 217.17±12.99a | 1.05±0.07ab | 3.00±0.00a | 19.66±2.16a |
| PS+DMSO组 | 127.50±12.27ab | 0.57±0.05b | 0.83±0.40abc | 6.16±1.16abc |
| a:P<0.05,与正常组比较;b:P<0.05,与PS组比较;c:P<0.05,与NS组比较 | ||||
Western blot检测结果(图 3)显示PS组和NS组IL-6、IL-β1和TNF-α三种炎症因子表达明显增强,而SOD2和GSH两种抗氧化应激的物达明显减少,其中 PS组这种变化趋势较为显著。与PS灌注组和盐水灌注组相比,PS+DMSO灌注组表现出IL-6、IL-β1、TNF-α三种炎症因子表达明显降低,SOD2和GSH两种抗氧化应激物达上升,这提示DMS0通过减低炎症和抗氧化应激发挥保护作用。
 |
| 图 3 Western blot检测各组大鼠膀胱SOD2、 GSH-Px 、 IL-6、IL-β1和TNF-α的表达 |
尿动力学研究(图 4,表 2)显示PS组和NS组都表现出大鼠膀胱容量降低、收缩间歇缩短、排尿频率加快,但PS组这种变化趋势更为显著(P<0.05)。与PS灌注组和盐水灌注组相比,PS+DMSO灌注组表现出大鼠膀胱功能得到改善、收缩间歇增加、排尿频率明显减低(P<0.05),这提示DMS0能显著改善大鼠膀胱功能。
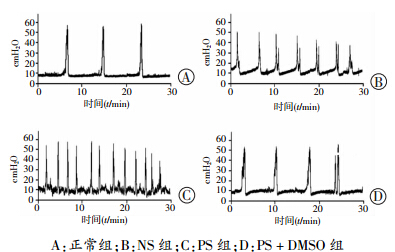 |
| A:正常组;B:NS组;C:PS组;D:PS+DMSO组 图 4 各组大鼠膀胱测压结果 |
| 组别 | BP (cmH2O) | MP (cmH2O) | MF (Nu/h) | ICI (min/s) | BC |
| 正常组 | 10.83±2.31 | 57.83±4.62 | 7.33±1.03 | 7.93±0.70 | 1.10±0.13 |
| NS组 | 13.17±1.72 | 53.33±2.80 | 14.83±2.31ab | 4.67±0.48ab | 0.55±0.08ab |
| PS组 | 15.33±1.96a | 56.66±5.57 | 23.83±2.14a | 2.42±0.37a | 0.35±0.04a |
| PS+DMSO组 | 12.17±1.94 | 57.00±4.24 | 9.67±0.87bc | 6.40±0.57abc | 0.85±0.09abc |
| a:P<0.05,与正常组比较;b:P<0.05,与PS组比较;c:P<0.05,与NS组比较 | |||||
肌条研究结果(图 5,表 3)显示PS组和NS组肌肉收缩紊乱,肌肉收缩不稳定和频繁,其中 PS组这种变化趋势更为显著(P<0.05)。与PS组和NS组相比,PS+DMSO灌注组表现出肌肉收缩较为稳定,肌肉收缩频率显著(P<0.05)恢复,这提示DMS0能显著改善大鼠膀胱收缩功能。
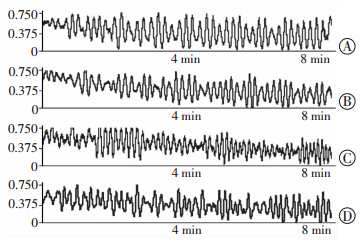 |
| A:正常组;B:NS组;C:PS组;D:PS+DMSO组 图 5 各组大鼠肌肉收缩频率和幅度变化 |
| 组别 | 收缩幅度(g) | 收缩频率(次/min) | ||
| 正常组 | 46.03±4.14 | 4.94±0.82 | ||
| NS组 | 42.14±3.20ab | 5.57±0.57ab | ||
| PS组 | 39.07±2.43ab | 6.93±0.97ab | ||
| PS+DMSO组 | 45.85±2.19bc | 4.94±0.73bc | ||
| a:P<0.05,与正常组比较;b:P<0.05,与PS组比较;c:P<0.05,与NS组比较 | ||||
BPS/IC的发病机制目前尚未阐明,目前认为肥大细胞激活和膀胱黏膜上皮损伤是其主要发病机制。肥大细胞激活和膀胱黏膜上皮损伤理论认为:膀胱泌尿道上皮损伤后,尿液中毒性物质渗入膀胱组织,导致膀胱局部微环境改变,进而引起浆细胞、肥大细胞等炎症细胞浸润,浸润的肥大细胞在局部炎症的诱导下激活并释放血管活性物质和促炎因子,最终加重了膀胱局部炎症和上皮损伤[10, 11]。PS是一种亲水性强碱性蛋白质,该物质对泌尿道黏膜上皮具有高度的亲和性,其同泌尿道黏膜上皮接触后,可导致上皮细胞损伤、脱落以及溃疡的形成,据此该物质被用于IC/PBS动物模型的制作和研究。本研究使用PS膀胱灌注构建模拟IC/PBS动物模型,研究的结果发现PS灌注后大鼠膀胱表现出明显的黏膜损伤以及肥大细胞等炎性细胞浸润,在病理学上同IC/PBS的病理表现相似,这提示动物模型建立成功。
间质性膀胱炎患者膀胱组织以及尿液中有过量炎症介质IL-6和TNF-α等表达,其中IL-6水平的含量同IC/PBS的这些严重程度成正比,这些研究提示着炎症在IC/PBS发病中不可替代的作用[3, 12]。目前研究认为氧化应激反应是炎症复合体和炎症瀑布反应的激动剂[13]。细胞和组织的氧化应激反应的发生最终激活和启动炎症反应导致组织损伤和炎症性疼痛持续性发生,据此降低氧化应激和炎症反应是改善组织损伤和疼痛的重要方式之一。
DMSO是一种较强的有机溶剂,具有较好的渗透性,研究提示 DMSO具有较强的干扰自由基生成,清除已生成的自由基、降低炎症介质和细胞因子,发挥抗炎症和氧化应激反应作用[4, 5]。尽管DMSO治疗IC/PBS的临床试验数据有限,但1960年FDA仍然批准使用50% DMSO用于IC/PBS膀胱灌注治疗,然而至今为止,DMSO的确切机制尚未完全阐明,目前推测DMSO在IC/PBS治疗中具有镇痛、抗炎、抑菌、阻止疼痛物质释放以及肌肉松弛等特性[14]。我们使用DMSO膀胱灌注PS诱导的IC/PBS大鼠发现,与PS组和盐水组相比,DMSO灌注后大鼠膀胱大体形态上表现为膀胱湿质量和膀胱湿质量/体质量比值得到显著改善;组织学表现为上皮组织有较好的完整性,组织水肿明显减轻,固有膜和肌层肥大细胞浸润数目显著减少;在功能学上表现为膀胱组织IL-6、IL-β1和TNF-α三种炎症因子表达明显降低,而SOD2和GSH两种抗氧化应激物达明显升高;大鼠肌肉收缩频率显著恢复,膀胱收缩间歇期增加、排尿频率明显减低,膀胱收缩功能显著改善。我们部分研究结果在其他学者的动物实验研究中同样也得到了证实[16, 17]。但是我们发现DMSO灌注后能显著的改善膀胱氧化应激反应和膀胱功能,并能显著降低肥大细胞在膀胱中的浸润和激活,该研究结果的发生可能是DMSO通过阻断氧化应激反应,降低炎症介质 IL-6、IL-β1和TNF-α的产生,减少肥大细胞趋化物质(IL-6、IL-β1和TNF-α)对肥大细胞的趋化和激活作用,最终发挥调控炎症和免疫反应阻断膀胱组织结构和功能的破坏。
总之,我们认为DMSO通过发挥其抗氧化应激反应、降低炎症物质产生,最终改善膀胱黏膜上皮损伤、膀胱收缩功能以及减轻炎症性疼痛,发挥保护膀胱的作用,本实验结果为DMSO治疗间质性膀胱炎提供了新的观点和思路。
| [1] | Humphrey L, Arbuckle R, Moldwin R, et al. The bladder pain/interstitial cystitis symptom score: development, validation, and identification of a cut score[J]. Eur Urol, 2012, 61(2): 271-279. |
| [2] | Nickel J C, Tripp D A, Pontari M, et al. Psychosocial phenotyping in women with interstitial cystitis/painful bladder syndrome: a case control study[J]. J Urol, 2010, 183(1): 167-172. |
| [3] | Grover S, Srivastava A, Lee R, et al. Role of inflammation in bladder function and interstitial cystitis[J]. Ther Adv Urol, 2011, 3(1): 19-33. |
| [4] | Cosar R, Eskiocak S, Yurut-Caloglu V, et al. Can radiation-induced chronic oxidative stress in kidney and liver be prevented by dimethylsulfoxide? Biochemical determination by serum and tissue markers[J]. J Buon, 2012, 17(1): 160-167. |
| [5] | Santos N C, Figueira-Coelho J, Martins-Silva J, et al. Multidisciplinary utilization of dimethyl sulfoxide: pharmacological, cellular, and molecular aspects[J]. Biochem Pharmacol, 2003, 65(7): 1035-1041. |
| [6] | Lv Y S, Yao Y S, Lin M E, et al. Interleukin-6 levels in female rats with protamine sulfate-induced chronic cystitis treated with hyaluronic acid [J]. Int J Urol, 2013, 20(10): 1017-1022. |
| [7] | Chen W, Jiang C, Jin X, et al. Roles of stem cell factor on loss of interstitial cells of Cajal in bladder of diabetic rats[J]. Urology, 2011, 78(6): 1443. e1-1443. e6. |
| [8] | 李龙坤, 宋波, 金锡御, 等. 骶神经根电刺激对大鼠神经源性膀胱储尿功能影响的实验研究[J]. 第三军医大学学报, 2003, 25(22): 1972-1974. |
| [9] | Li L, Jiang C, Hao P, et al. Changes of gap junctional cell-cell communication in overactive detrusor in rats[J]. Am J Physiol Cell Physiol, 2007, 293(5): C1627-C1635. |
| [10] | Theoharides T C, Kempuraj D, Sant G R. Mast cell involvement in interstitial cystitis: a review of human and experimental evidence[J]. Urology, 2001, 57(6 Suppl 1): 47-55. |
| [11] | Parsons C L. The role of the urinary epithelium in the pathogenesis of interstitial cystitis/prostatitis/urethritis[J]. Urology, 2007, 69(4 Suppl): 9-16. |
| [12] | Nasrin S, Masuda E, Kugaya H, et al. Improvement by phytotherapeutic agent of detrusor overactivity, down-regulation of pharmacological receptors and urinary cytokines in rats with cyclophosphamide induced cystitis[J]. J Urol, 2013, 189(3): 1123-1129. |
| [13] | Levine B, Mizushima N, Virgin H W. Autophagy in immunity and inflammation[J]. Nature, 2011, 469(7330): 323-335. |
| [14] | Smith K J, Chess-Williams R, McDermott C. Luminal DMSO: effects on detrusor and urothelial/lamina propria function[J]. Biomed Res Int, 2014, 2014: 347616. |
| [15] | 王亮, 赵江, 董兴有, 等. 乙酰半胱氨酸对硫酸鱼精蛋白诱导的大鼠膀胱炎的作用[J]. 第三军医大学学报, 2014, 36(7): 640-644. |
| [16] | Tyagi P, Hsieh V C, Yoshimura N, et al. Instillation of liposomes vs dimethyl sulphoxide or pentosan polysulphate for reducing bladder hyperactivity[J]. BJU Int, 2009, 104(11): 1689-1692. |
| [17] | Soler R, Bruschini H, Truzzi J C, et al. Urinary glycosaminoglycans excretion and the effect of dimethyl sulfoxide in an experimental model of non-bacterial cystitis[J]. Int Braz J Urol, 2008, 34(4): 503-511. |



