尿崩症(diabetes insipidus,DI) 是指由于抗利尿激素(ADH,又称精氨酸加压素)分泌不足或者由于肾脏对抗利尿激素不敏感,从而导致肾小管重吸收水功能障碍引起的一组征群。既往研究表明该病的误诊率较高,部分患者有上尿路积水,并且曾被长期误诊为神经源性膀胱、膀胱过度活动症等疾病[1]。本研究报告的10例患者,均以双肾积水就诊于我院泌尿外科,其中部分患者在外院误诊为神经源性膀胱并接受了不恰当的手术治疗,现就其诊治经验进行总结,以提高泌尿科、肾脏科和内分泌科等相关专科医生对该病的认识。 1 资料与方法 1.1 研究对象
收集中国康复研究中心附属北京博爱医院泌尿外科 2011年1月至2014年7月间,诊断为尿崩症的患者10例。本组均为男性,年龄12~34岁,平均17.8岁。病程1~15年,平均8.5年,所有患者均存在不同程度的双侧输尿管扩张、双侧肾积水。所有患者均行泌尿系B超检查、垂体磁共振成像(MRI)、磁共振尿路成像(MRU)、影像尿动力学检查、尿常规检查,禁水加压素试验。
尿崩症诊断标准:①多尿,烦渴,多饮症状。②尿比重<1.005,尿渗透压为50~200 mOsm/kg H2O,明显低于血浆渗透压,血浆渗透压可高于300 mmol/L。 ③禁水加压素试验阳性。禁水前测体质量、血压、脉率、尿量、尿比重、尿渗透压、血渗透压。持续8~12 h禁水,每2小时测上述指标,至尿量无变化、尿比重及尿渗透压持续2次不再上升为止。此时皮下注射抗利尿激素5 U,每小时再收集尿量,测尿比重、尿渗透压1~2次。尿崩症患者禁水后尿量减少不明显,尿比重、尿渗透压无明显升高,体质量和血压明显下降,血浆渗透压升高(>300 mmol/L)。中枢性尿崩症患者注射抗利尿激素后尿量明显减少,尿比重、尿渗透压成倍增高。肾性尿崩症患者禁水和肌注抗利尿激素,均不能使尿量减少及尿液浓缩。④弥凝(1-脱氨-8-右旋-精氨酸加压素片)诊断性治疗,中枢性尿崩症患者对弥凝治疗有效,肾性尿崩症对弥凝治疗无反应。⑤鞍区磁共振检查:有助于该区域器质性病变的诊断和鉴别诊断。
本组患者均常规连续记录3天的24 h排尿日记,排尿日记显示24 h尿量一般在6 000~10 000 mL,每日饮水量一般在8 000~11 000 mL,残余尿量20~600 mL不等。
本组有6例因双侧肾盂输尿管严重积水,大量残余尿量在外院诊断为神经源性膀胱。其中1例于外院行膀胱造瘘术,1例在外院诊断为双侧输尿管膀胱壁内段狭窄行双侧输尿管膀胱再植术,术后肾积水未见明显改善,1例在外院行膀胱颈切开手术治疗,术后大量残余尿未得到改善。其余4例因尿频、尿急曾被诊断为膀胱过度活动症,曾长期应用M受体阻滞剂酒石酸托特罗定治疗无效。 1.2 实验室及影像学检查
本组10例患者均有尿比重、尿渗透压的下降,血浆渗透压因采血时间通常在清晨,夜间摄入水量较少,故血浆渗透压稍高或正常。本组患者入组前尿比重1.000~1.004,尿渗透压为46~107 mOsm/kg H2O,血浆渗透压为294~307 mOsm/kg H2O。2例患者入组前肌酐有轻度升高,波动在163~201 μmol/L之间,其余患者肾功能均正常。电解质方面血钠和氯正常或稍高,空腹血糖均正常,甲状腺功能5项均正常。禁水加压试验结果4例患者诊断为中枢性尿崩症,6例患者诊断为肾性尿崩症。需要注意的是,当有大量残余尿时只有留置导尿彻底排空尿液、准确监测每小时尿量才能正确判断禁水加压试验结果。
本组患者泌尿系超声均提示双侧肾脏集合系统不同程度的分离和双侧输尿管的扩张。核磁水成像均有3~4度肾盂输尿管的积水扩张,膀胱容量增大,输尿管迂曲,未见狭窄梗阻征象,图 1A、B为1例中枢性尿崩症患者治疗前核磁水成像,分度标准参考2014版中国泌尿外科疾病诊断治疗指南中廖利民提出的方法[2]。头颅MRI检查:1例有垂体微腺瘤,1例提示部分性空泡蝶鞍,其余患者垂体无明显异常。为鉴别神经源性膀胱,3例行腰骶部MRI检查,1例有隐性骶裂,1例有腰椎间盘突出,1例正常,该3例均行盆底电生理检查,排除了神经系统损害。 1.3 影像尿动力学检查
10例患者均行影像尿动力学检查,均表现为充盈期逼尿肌稳定,2例膀胱感觉减退,其余8例感觉正常。压力流率测定,7例最大尿流率>15 mL/s,2例>10 mL/s,最大尿流率时的逼尿肌压力正常,1例患者只能排出少量尿液。残余尿情况:4例患者无残余尿,其余患者残余尿量在20~600 mL不等。本组患者尿动力学平均膀胱容量达到1 396.3 mL,最大尿流率平均19.7 mL/s,最大容积时逼尿肌压力平均46.3 cmH2O,残余尿量平均273.3 mL。
值得注意的是,有患者在外院行尿动力检查时通常灌注量达到500 mL时即停止灌注,由于多数患者有憋尿习惯,膀胱容量较大,膀胱感觉减退,这时大多数患者未达到强烈排尿感,故尿动力检查时未能反映患者平时情况,导致逼尿肌压力的变化未准确反映。
通过尿动力学检查结合膀胱灌注量、排出尿量、残余尿量及记录的灌注总时间,可计算出单位分钟内的产尿量:膀胱实际容量(mL)= 排出尿量+残余尿量,产尿速度(mL/min) = 膀胱实际容量(mL)-灌注量(mL)/灌注时间(min),产尿速度大于250 mL/h,对诊断尿崩症有意义,本组10例患者的产尿速度均大于250 mL/h。 2 结果
本组患者均行弥凝(1-脱氨-8-右旋-精氨酸加压素片)诊断性治疗,结合病史及实验室、辅助检查、禁水加压素试验,最终4例患者诊断为中枢性尿崩症,6例患者诊断为肾性尿崩症,其中1例患者自幼有多尿、多饮症状,其表哥也有类似病史,最终也确诊为肾性尿崩症。
诊断明确后,4例中枢性尿崩症患者开始规律服用弥凝,开始给予弥凝0.1 mg每天3次,记录排尿日记,并指导定时排尿,大量残余尿者留置尿管,初始用药阶段每天复查尿常规,每隔1 d复查血渗透压、血电解质Na+ 、K+水平,根据尿量、尿渗透压、血渗透压调整弥凝剂量。本组3例患者应用0.1每天3次,1例患者应用0.2 mg,每天3次,能够较好控制症状,最后出院时24 h的尿量控制在2 000~4 000 mL。出院后患者长期规律服药,随访1~3年,复查泌尿系彩超、核磁水成像均提示肾积水明显改善(图 1)。
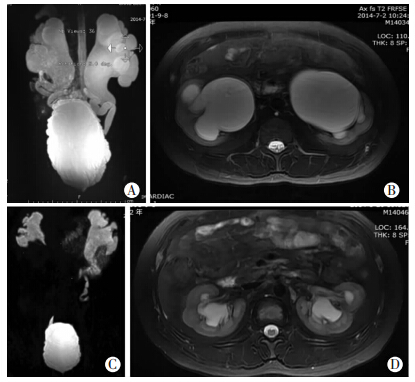 |
| A:肾盂输尿管4度积水扩张;B:肾脏严重积水;C:肾盂输尿管积水明显改善;D:肾脏积水缓解 图 1 中枢性尿崩症患者治疗前(A、B)、后(C、D)核磁水成像表现 |
6例肾性尿崩症患者,给予保钠利尿剂氢氯噻嗪片25 mg口服,每日3次,24 h尿量控制在2 500~3 000 mL,通过指导其改变排尿习惯,避免自觉膀胱憋胀感时排尿,建议30 min至1 h排空膀胱1次,出院时复查泌尿系彩超示双肾积水有改善。出院后随访1~3年,1例患者加用保钾利尿药物(阿米洛利片)后,尿量明显减少,24 h平均尿量在3 000 mL左右,辅助定时排空膀胱,复查肌酐降至正常,肾积水明显改善;2例患者坚持服用保钠利尿剂,并定时排空尿量,肾积水有改善;其余3例因依从性较差,未坚持服用药物,排尿习惯恢复以前,复查肾积水仍未改善。 3 讨论
DI是指由于抗利尿激素(antidiuretic hormone,ADH) 分泌不足,或者肾脏对ADH 反应不敏感,导致肾小管重吸水功能障碍,从而引起的临床上表现为多尿、烦渴、多饮等症状的症候群,实验室检查表现为低比重尿和低渗尿。其中由于垂体分泌ADH不足引起的称为中枢性尿崩症,由于肾脏对ADH 反应不敏感引起的称为肾性尿崩症。临床上对于任何持续多尿、烦渴、多饮、低比重尿者均应考虑DI的可能性,检测尿比重、血、尿渗透压、肾功能以及血浆抗利尿激素水平有助于诊断。在实际临床工作中常常因有尿频、多尿、夜间遗尿、排尿时间延长、排尿不尽感等症状而误诊为膀胱过度活动症、神经源性膀胱等疾病,部分患者还不恰当地接受了手术治疗,现结合本组患者讨论如下。
尿崩症是一个内科疾病,往往由于并发上尿路的扩张积水才就诊于泌尿外科,故对于该类疾病,还需要排除上尿路梗阻因素(包括输尿管的狭窄、结石等)和下尿路梗阻因素(包括膀胱颈挛缩、前列腺增生、尿道狭窄等)。尿崩症患者单位时间内产尿量增多,尿液从肾脏排出到达输尿管,造成输尿管输送尿液负荷增加,为了代偿输尿管需要加快收缩频率及加大收缩力来维持尿液的输送,当负荷增加超出了输尿管的最大排空能力后,尿液在输尿管内逐渐蓄积,造成整个上尿路的扩张积水。其次,大部分尿崩症患者由于因学习及工作等因素,不能做到随时排尿,均有长期憋尿习惯,憋尿后造成膀胱感觉减退,膀胱容积可进一步扩大。上述特点反映在尿动力学检查上经常表现为膀胱容量增加,膀胱感觉减退[1]。
国内学者曾报道9例诊断为肾性尿崩症合并上尿路严重积水的患者[3],尿动力学平均膀胱容量达到1 056.3 mL,最大尿流率平均30.8 mL/s,最大容积时逼尿肌压力平均51.3 cmH2O,残余尿量平均436.3 mL。 本组患者在外院行尿动力检查时通常膀胱灌注量达到500 mL时即停止灌注,这导致尿动力检查未能充分再现患者日常情况,大多数患者未达到强烈排尿感就已经停止膀胱灌注,未准确反映日常逼尿肌压力的变化,因此该类患者应适当增加膀胱灌注量,待达到强烈排尿感再停止膀胱灌注,这样才能准确评估逼尿肌压力和膀胱安全容量。通过尿动力学检查还可以计算出产尿速度,产尿速度>250 mL/h,对诊断尿崩症有意义,本组10例尿崩症患者的产尿速度均>250 mL/h。
诊断明确后,通过药物减少尿量的产生,降低输尿管输送尿液负荷,是治疗此类尿崩症的基本方法,药物治疗同时需要辅助定时排尿等措施。弥凝是治疗中枢性尿崩症的首选药物。张长征等[4]报道2例中枢性尿崩症,通过弥凝治疗达到满意效果,Korzets等[5]报道1例中枢性尿崩症患者,通过弥凝治疗后减少了尿量的产生,辅助定时排尿,治疗效果明显。本组4例中枢性尿崩症患者应用弥凝治疗,0.1 mg,每日3次,根据排尿日记指导定时排尿并调整弥凝剂量,最后出院时24 h 的尿量控制在2 000~4 000 mL,出院后随访1~3年,复查泌尿系彩超均提示肾积水明显改善。
保钾利尿剂 (阿米洛利片)、保钠利尿剂(氢氯噻嗪)、非甾体类消炎药(吲哚美率)均有成功治疗肾性尿崩症的报道。张小东等[6, 7, 8, 9]报道8例肾性尿崩症,均通过氢氯噻嗪或加用吲哚美率减少了尿量。国外Kirchlechner等[10]报道采用双氢克脲噻和非甾体类 镇痛药治疗4例肾性尿崩症患儿,随访时间长达5年,无1例出现尿路积水。本组6例肾性尿崩症患者,给予保钠利尿剂氢氯噻嗪片25 mg口服,每日3次,尿量均有改善,24 h尿量平均控制在2 500~3 000 mL,通过指导其改变排尿习惯,避免自觉膀胱憋胀感时排尿,建议定时排空膀胱,出院时复查泌尿系彩超示双肾积水均有改善。
通过药物控制尿量的同时,应指导患者定时排尿,避免过度憋尿,在残余尿量较多,且肾功能有下降,合并有下尿路梗阻,逼尿肌收缩乏力等,这些因素的情况下可建议行间歇导尿、膀胱造瘘术[11]。Tokunaka等[12]研究发现,无反流-无梗阻输尿管的部分患者膀胱壁内段输尿管未发生细胞超微结构改变,对于非梗阻性的上尿路扩张应避免行双侧输尿管再植术。本组1例在外院因上尿路积水行双侧输尿管膀胱再植术,术后肾积水未见明显改善。另外1例在外院行膀胱颈切开手术治疗,术后大量残余尿未得到改善。这些均说明,尿崩症继发的泌尿系扩张无明显的解剖性梗阻,主要为长期多尿引起的相对性梗阻和功能障碍,盲目手术治疗并不能解决该类患者问题。
膀胱过度活动症(overactivebladder,OAB)是一种以尿急症状为特征的症候群,常伴有尿频和夜尿增多症状,可伴或不伴有急迫性尿失禁,尿动力学上可表现为逼尿肌过度活动,也可为其他形式的尿道膀胱功能障碍。尿急是OAB的核心症状,而多数尿崩症患者有憋尿习惯,只有达到强烈排尿感时才去排尿。OAB患者的尿量、尿比重、尿渗透压及血电解质一般正常,通过规范记录及分析排尿日记,测定尿比重、尿渗透压一般可以鉴别。本组1例患者以尿频伴双侧肾积水3年余入院,在多家医院诊断为OAB,给予索利那新等药物治疗无效,最后通过分析排尿日记,相关实验室检查、泌尿系B超以及尿动力学检查,继行禁水-加压素试验,诊断为中枢性尿崩症,通过口服弥凝0.1 mg,每日3次,最终24 h尿量控制在1 800~2 000 mL,日间 排尿约4~7次,夜尿0~2次,每次量为170~260 mL。
神经源性膀胱(neurogenic bladder,NB)是一类由于神经系统病变导致膀胱和/或尿道功能障碍(即储尿和/或排尿功能障碍),进而产生一系列下尿路症状及并发症的疾病总称。NB因下尿路功能障碍进而引起上尿路的病理生理改变,以上尿路扩张积水为主要表现,但NB最主要的病史是神经系统病变,伴随下尿路,包括储尿期、排尿期、排尿后的各种症状,影像尿动力学检查可表现为逼尿肌过度活动或无反射、膀胱低顺应性、逼尿肌-括约肌协调失调、膀胱输尿管返流等。尿崩症与神经源性膀胱鉴别时影像尿动力检查、盆底电生理检查是非常重要的,本组3例怀疑合并神经源性膀胱的尿崩症患者行盆底电生理检查,均排除神经系统损害。
综上所述,对尿崩症患者上尿路积水的治疗,应首选通过药物达到减少尿量产生,辅助限制饮水、定时排尿,改变排尿习惯,慎重选择手术治疗。泌尿科医生在诊治类似的以泌尿道扩张和积水为表现的尿崩症患者时,应关注患者尿量,如存在明确的多尿则及时请内分泌科医生协同诊治,尽早明确诊断并给予及早治疗是取得良好治疗效果的关键。
| [1] | 姚丹, 王涌, 赵晓龙, 等. 以泌尿道扩张和积水为表现的3例尿崩症报告和文献复习[J]. 中华内分泌代谢杂志, 2013, 29(2): 130-134. |
| [2] | 那彦群, 叶章群, 孙颖浩, 等. 2014版中国泌尿外科疾病诊断治疗指南[M]. 北京: 人民卫生出版, 2014: 277-278. |
| [3] | Jin X D, Chen Z D, Cai S L, et al. Nephrogenic diabetes insipidus with dilatation of bilateral renal pelvis, ureter and bladder[J]. Scand J Urol Nephrol, 2009, 43(1): 73-75. |
| [4] | 张长征, 胡卫列, 邓志雄, 等. 继发于中枢性尿崩症的巨输尿管-巨膀胱综合征: 附2例报告[J]. 临床泌尿外科杂志, 2010, 25(2): 154-155. |
| [5] | Korzets A, Sachs D, Gremitsky A, et al. Unexplained polyuria and non-obstructive hydronephrosis in a urological department[J]. Nephrol Dial Transplant, 2004, 19(9): 2410-2412. |
| [6] | 张小东, 朱积川, 姜辉, 等. 继发于肾源性尿崩症的巨输尿管-巨膀胱综合征: 附1例报告并文献复习[J]. 中华泌尿外科杂志, 2001, 22(5): 278-280. |
| [7] | 瞿平, 周健, 季云天. 继发于肾源性尿崩症的巨输尿管-巨膀胱综合征1例[J]. 江苏医药, 2004, 30(12): 942-943. |
| [8] | 金晓东, 金百冶, 蔡松良, 等. 泌尿系扩张的肾性尿崩症5例诊治分析[J]. 中华外科杂志, 2005, 43(14): 965-966. |
| [9] | 岳峰, 杨进益, 姜兴金, 等. 先天性肾性尿崩症合并非梗阻性双侧尿路扩张1例报告[J]. 中华泌尿外科杂志, 2012, 33(8): 640. |
| [10] | Kirchlechner V, Koller D Y, Seidl R, et al. Treatment of nephrogenic diabetes insipidus with hydrochlorothiazide and amiloride[J]. Arch Dis Child, 1999, 80(6): 548-552. |
| [11] | Colliver D, Storey R, Dickens H, et al. Nonobstructive urinary tract dilatation in children with diabetes insipidus[J]. J Pediatr Surg, 2012, 47(4): 752-755. |
| [12] | Tokunaka S, Koyanagi T, Tsuji I, et al. Histopathology of the nonrefluxing megaloureter: a clue to its pathogenesis[J]. J Urol, 1982, 127(2): 238-244. |



