放射损伤合并创伤称为“放创复合伤”,战时多见于核爆炸,平时见于核事故、核恐怖活动,也可见于临床放疗等病例。其特点为正常创面愈合的过程受到抑制,导致创面愈合延迟或经久不愈,成为“难愈性创伤”[1]。前期研究发现其难愈的机制与放射损伤导致局部修复细胞数量减少和功能障碍以及抑制基质细胞产生生长因子等因素相关,如何促进放创复合伤难愈性伤口的愈合一直是研究的重点[2]。血小板源生长因子(platelet derived growth factor,PDGF)是由多种细胞产生的能刺激间质来源的细胞增殖的多肽,具有广泛的生理活性,在创伤愈合的各个阶段都发挥作用,对病理性创口有良好的作用,特别是对放射损伤性溃疡、糖尿病性皮肤溃疡等难愈合创伤的修复有明显的促进作用。研究表明从猪、牛等血小板中提取的PDGF,应用于临床深度烧烫伤或枪击伤等创伤愈合,取得了很好的疗效,其疗效优于重组人表皮生长因子凝胶(EGF)。本实验在前期大量研究的基础上,对PDGF的分子片段进行优化,并在Pichia酵母中表达纯化,表达量高于100 mg/L,获得了新型的重组人血小板源生长因子(rhThr6-PDGF-BB),拟利用放创复合伤的实验动物模型,重点观察此新型PDGF对放创复合伤的促愈效果并探讨部分促愈的机制,为研制开发特殊皮肤创伤治疗用新型血小板源生长因子提供理论依据。 1 材料与方法 1.1 实验动物与分组
清洁级Wistar雌性大鼠120只,体质量(180±20)g,由第三军医大学实验动物中心提供并统一饲养在清洁级动物房。动物在实验前常规饲养3 d,观察无异常者,通过抽签随机分为6组:空白对照组、凝胶基质对照组、低剂量药物组、中剂量药物组、高剂量药物组、阳性药物对照组,每组20只大鼠。 1.2 药物试剂
重组人新型血小板源生长因子(rhThr6-PDGF-BB)凝胶剂由军事医学科学院自主研制提供,其中“低剂量”药物浓度为0.005%,“中剂量”药物浓度为0.01%,“高剂量”药物浓度为0.02%,凝胶基质对照组为不含PDGF的药物凝胶,阳性对照药物选用已上市的重组人表皮生长因子凝胶(EGF,桂林华诺威基因药业有限公司生产,批号20131203),药物浓度为0.01%。 1.3 放创复合伤模型制作
各组大鼠均在第三军医大学辐照中心用60Coγ射线全身照射,照射剂量为4 Gy。照射后2 h,用 1%戊巴比妥钠溶液按40 mg/kg腹腔注射麻醉,麻醉起效后用剃毛刀备皮,固定背部,用半径1 cm圆形图章在尾根部以上3 cm处印出印记,在无菌操作台下进行皮肤消毒,用手术刀沿印记切出半径1 cm圆形切口,深度及全层皮肤,不伤及皮下筋膜层。 1.4 给药方式
每只大鼠分笼饲养,自由进食水,自创面制作当天开始,每天对大鼠背部的创面进行处理,碘伏棉球消毒1次,沾去创面上的粉尘、木屑,酒精棉球擦拭脱碘,最后按不同分组,将相应的药物均匀涂于创面表面。实验组凝胶用量均按照70 mg/cm2计算,阳性药物EGF组按照说明书推荐剂量100 mg/cm2给药,空白对照组仅用碘伏棉球消毒,开药取药等操作均在超净台进行,连续用药14 d。 1.5 检测指标 1.5.1 大体观察和组织取材
各组大鼠分别于制作创面后第7、10、14天,每组随机取5~6只处死,活杀前观察动物伤口愈合情况,称体质量,描记伤口面积并拍照,取创面皮肤组织,常规取材备用。 1.5.2 创面愈合面积分析
在第3、5、7、10、14天,麻醉大鼠(1%戊巴比妥溶液,35 mg/kg),对创面进行拍照,并进行创面面积描绘。创面描绘采用透明膜描记法。再以万分之一电子分析天平(德国SartorusA公司)称取透明塑料膜图样的质量,并换算成相应创面的面积。然后通过创面的面积变化,计算创面愈合率。创面面积=透明膜整体面积×描绘部分质量/透明膜整体质量。创面愈合率=(原创面面积-现创面面积)/原创面面积×100%。 1.5.3 病理学检查
取活杀大鼠背部创面皮肤标本置4%甲醛溶液固定,经脱水、透明、浸蜡、包埋及切片后行苏木精伊红(HE)常规组织学染色,光镜观察。显微镜下从各组伤后第7、14天创伤部位肉芽组织取5个视野,自动图像分析仪进行毛细血管及成纤维细胞计数分析。 1.5.4 免疫组化
采用两步法免疫组化检测试剂盒检测皮肤组织中Bcl-2、PDGF-A、VEGF抗体的表达。切片用去离子水洗,进行抗原微波修复,3% H2O2封闭,PBS冲洗,加生物素封闭液10 min,按1 ∶150稀释一抗,滴加后4 ℃过夜,PBS冲洗,滴加二抗,37 ℃孵育30 min,PBS冲洗,滴加DAB显色剂,苏木精复染,常规脱水、透明、封片。每次染色设阳性对照和阴性对照染色,阴性片做法为PBS取代一抗。每张片子随机取5个视野(×400)进行拍照,并用Image-Pro-Plus 6.0进行图像分析,进行免疫组化综合评分。 综合评分为阳性染色评分和阳性细胞数比例评分之和。阳性染色评分标准为:未着色0分,浅黄色1分,黄色2分,黄褐色3分,深棕色4分。阳性细胞比例评分标准为:阳性细胞比例<5%为0分,5%~25%为1分,25%~50%为2分,50%~75%为3分,>75%为4分。每张组 化切片的5个视野分别计算阳性染色评分和阳性比例评分的平均值,相加得到该组化切片的免疫组化综合评分。 1.6 统计学分析
采用SPSS 13.0统计软件对创面愈合率及免疫组化评分行单因素方差分析,数据以x±s表示。 2 结果 2.1 各组大鼠创面愈合率比较
药物处理组与对照组大鼠创面7、14 d愈合率均存在显著差异(P<0.05)。其中空白对照组创面愈合情况优于凝胶基质对照组,且略优于低剂量药物组,考虑是由于空白对照组大鼠的创面干燥,对于创面愈合更加有利。而各组含有药物成分的实验组,创面愈合率的趋势基本与药物浓度呈正相关。 其中高剂量药物组创面愈合率最好,且优于已上市的阳性对照药物EGF,表明高剂量药物对促进放创复合伤的创面愈合有显著疗效(图 1)。
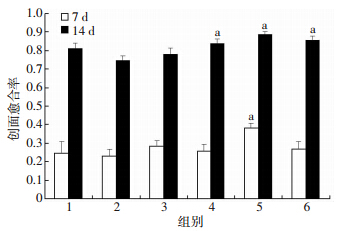 |
| 1:空白对照组;2:凝胶基质对照组;3:低剂量药物组;4:中剂量药物组;5:高剂量药物组;6:阳性对照组 a:P<0.05,与空白对照组比较 图 1 各组大鼠用药7 d和14 d创面愈合率比较 |
伤后第7天:高剂量药物组肉芽组织明显较对照组增多,新生毛细血管和成纤维细胞含量丰富,毛细血管垂直创面生长,成纤维细胞排列趋于有序,伤口周围表皮细胞已见再生,并向伤口内爬行(图 2A~C)。伤后第14天:对照组创面未完全愈合,尚未见皮肤附件的出现(图 2D)。高剂量药物组表皮细胞已经覆盖创面,并有角质层形成,表皮层开始变薄,新生血管数量明显减少几近消失,胶原含量明显增多,创面已完全愈合,且皮肤附件开始出现和增多明显(图 2E);而阳性药物愈合效果也优于空白对照组(图 2F)。
 |
| A:空白对照组第7天;B:高剂量药物组第7天;C:阳性对照组第7天;D:空白对照组第14天;E:高剂量药物组第14天;F:阳性对照组第14天;箭头示创面 图 2 各组大鼠创面肉芽组织、新生血管及表皮再生情况(HE×100) |
毛细血管形成和成纤维细胞增生的情况观察显示:伤后各药物组第7天肉芽组织内新生毛细血管和成纤维细胞数量多于对照组,高剂量药物组较为明显,且优于阳性药物对照组。第14天高剂量药物肉芽组织内新生血管数量明显减少几近消失,主要为大量排列有序的纤维细胞,胶原含量明显增多(图 3)。
 |
| A:空白对照组第7天;B:高剂量药物组第7天;C:阳性对照组第7天;D:空白对照组第14天;E:高剂量药物组第14天;F:阳性对照组第14天 图 3 各组大鼠肉芽组织区毛细血管、成纤维细胞增生情况(HE×200) |
Bcl-2、PDGF-A以及VEGF均主要表达于胞浆,免疫组化获得的图像可见药物处理组和阳性对照组的Bcl-2及PDGF-A表达均强于凝胶对照组,高剂量药物组VEGF表达强于凝胶对照组和阳性对照组。对照组肉芽组织内阳性细胞主要分布于成纤维细胞和巨噬细胞胞浆内呈淡黄色表达,阳性细胞为5%~25%。PDGF高剂量药物组肉芽组织内阳性成纤维细胞和巨噬细胞较对照组明显增多,新生血管内皮细胞胞浆内也有阳性表达,阳性细胞为50%~75%,呈黄褐色表达。免疫组化综合评分的统计分析结果表明高剂量药物组和凝胶对照组之间均有显著差异(P<0.05)。见图 4、5。
 |
| A~C:分别为凝胶基质对照组皮肤切片检测Bcl-2、PDGF-A、VEGF的表达;D~F:分别为高剂量药物组皮肤切片检测Bcl-2、PDGF-A、VEGF的表达;G~I:分别为阳性对照组皮肤切片检测Bcl-2、PDGF-A、VEGF的表达 图 4 免疫组化观察药物处理14 d各组大鼠Bcl-2、PDGF-A、VEGF表达(SV法 ×400) |
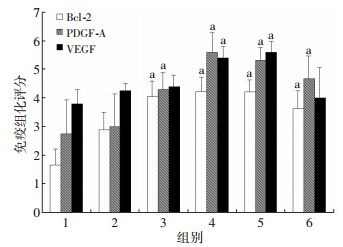 |
| 1:空白对照组;2:凝胶基质对照组;3:低剂量药物组;4:中剂量药物组;5:高剂量药物组;6:阳性对照组 a:P<0.05,与空白对照组比较 图 5 药物处理14 d各组大鼠Bcl-2、PDGF-A、VEGF表达 免疫组化评分 |
大量的研究表明皮肤创面修复与血小板衍生生长因子(platelet derived growth factor,PDGF)、成纤维细胞生长因子(fibroblast growth factor,FGF)、血管内皮细胞生长因子(vascular endothelial growth factor,VEGF)、神经生长因子(nerve growth factor,NGF)、表皮生长因子(epithelial growth factor,EGF)等许多生长因子介导和参与调控伤口肉芽组织的生长、血管再生和再上皮化密切相关[2, 3, 4, 5, 6]。外源性PDGF 可以促进难愈性皮肤溃疡和局部照射皮肤伤口的愈合[7, 8]。研究表明,从人血小板提取物中纯化的PDGF-BB,通过N端氨基酸分析表明存在3种不同的剪切形式,20% Ser1,35% Thr33及45% Thr6,这些切割的异质性,导致PDGF的不均一性,使质量控制较为困难;而104个氨基酸的蛋白保持了与109个氨基酸同样的生物学活性,鉴于以上原因,自主研制重组人新型血小板源生长因子(rhThr6-PDGF-BB)为在毕赤酵母中表达了104个氨基酸的Thr6-PDGF-B,并进行了工程菌高密度发酵培养,表达量高于100 mg/L,工艺简单,易于放大。在前期研究的基础上,本实验主要利用体外、体内实验对其促愈效果进行系统评价,期望能形成有自我知识产权的特殊伤口促愈药物。
本实验室前期已制作好放创复合伤大鼠模型,并对创伤愈合进行了系列研究[9, 10, 11],包括PDGF,也发现PDGF对放创复合伤的创面有促愈效果。在以上工作基础上,本实验主要将自主克隆的人新型血小板源生长因子局部涂于放射复合伤大鼠的创面,系统观察其对皮肤创伤愈合的影响。结果发现rhThr6-PDGF-BB药物组大鼠创面愈合速度明显加快,以高剂量药物组明显,14 d 创面基本愈合,而对照组愈合速度减慢,14 d 残留面积仍有19%,表明高剂量rhThr6-PDGF-BB药物组能明显促进放射复合创伤伤口的愈合。光镜下观察发现rhThr6-PDGF-BB能促进创面上皮的移行和肉芽组织增生,成纤维细胞和新生毛细血管均较对照组丰富,尤其以高剂量药物组较为明显,提示加快表皮细胞生长,促进内皮细胞增殖和毛细血管生长,以及促进成纤维细胞增殖、分化,可能是PDGF加速皮肤创伤愈合的机制之一。
电离辐射对创伤愈合延迟的影响与创面内源性生长因子含量低下或因子受体活性下调等因素有关[12, 13, 14]。在本实验中重点观察了创面新生肉芽组织中Bcl-2、PDGF-A及VEGF免疫组化阳性表达情况,结果显示rhThr6-PDGF-BB 能抑制Bcl-2的表达,促进PDGF-A和VEGF的表达,提示 rhThr6-PDGF-BB对创面愈合可能通过抑制细胞凋亡,促进细胞增殖、移行及及肉芽组织增生等促进创面愈合。
1997年美国FDA批准Regranex上市,用于糖尿病足部溃疡的治疗,其活性成分是酿酒酵母表达的0.01%的重组人血小板源生长因子,具有较好的促愈效果,但每支售价高达400多美元,价格极其昂贵,限制其临床的应用。本实验在前期大量研究的基础上,对PDGF的分子片段进行优化,并在Pichia酵母中表达纯化,表达量高于100 mg/L,获得了新型的具有自主知识产权的重组人血小板源生长因子,利用放创复合伤的实验动物模型观察其对放创复合伤的促愈效果,为研制开发特殊皮肤创伤治疗用新型血小板源生长因子提供理论依据,但对人难愈性创面是否有促愈效果及其促愈信号传导通路还待进一步研究。
| [1] | 柏书博, 王国栋, 王良, 等. 辐射损伤小鼠皮肤缺损模型愈合评价[J].第二军医大学学报, 2011, 32(8): 840-844. |
| [2] | 李金凤, 崔春萍, 段海峰, 等. 肝细胞生长因子与皮肤创面修复[J].中国康复医学杂志, 2007, 22(7): 669-672. |
| [3] | 王国栋, 王佳琪, 赵云富, 等. PDGF-BB、TNF-α参与电离辐射致小鼠皮肤创面愈合延迟[J]. 第二军医大学学报, 2013, 34(9): 954-959. |
| [4] | 李晶哲, 夏芸, 刘柏东, 等. 芦荟大黄素促进皮肤创伤修复作用机理研究[J].中国中医基础医学杂志, 2011, 17(11): 1260-1263. |
| [5] | Farhadi M R, Capelle H H, Erber R, et al. Combined inhibition of vascular endothelial growth factor and platelet-derived growth factor signaling: effects on the angiogenesis, microcirculation, and growth of orthotopic malignant gliomas [J]. J Neurosurg, 2005, 102(2): 363-370. |
| [6] | Darby I A, Laverdet B, Bonte F, et al. Fibroblasts and myofibroblasts in wound healing[J]. Clin Cosmet Investig Dermatol, 2014, 7: 301-311. |
| [7] | Mandraucchia V J , Sanders S M, Frerichs J A. The use of bacaplermin (rhPDGF-BB) gel for chronic nonhealing ulcers. A retrospective analysis[J]. Chin Podiatr Med Surg, 2001, 18(1): 189-209, viii. |
| [8] | 谢晓英, 严励. 糖尿病皮肤病变及其机制的研究进展[J]. 国际内分泌代谢杂志, 2009, 29(6): 417-420. |
| [9] | 冉新泽, 程天民, 林远, 等.大鼠放创复合伤时皮肤创伤愈合的形态学观察[J]. 第三军医大学学报, 2003, 25(14): 1233-1236. |
| [10] | 艾国平, 粟永萍, 闫国和, 等.骨髓间充质干细胞对合并局部放射损伤创面促愈作用及机理研究[J].中华医学杂志, 2002, 82(23): 1632-1636. |
| [11] | Yan G, Sun H, Wang F, et al. Topical application of hPDGF-A-modified porcine BMSC and keratinocytes loaded on acellular HAM promotes the healing of combined radiation-wound skin injury in minipigs[J]. Int J Radiat Biol, 2011, 87(6): 591-600. |
| [12] | 程治强, 李钰珑. 生长因子在创伤愈合过程中的机制[J].中国民康医学, 2007, 19(10A): 875, 891. |
| [13] | 柏书博, 王国栋, 吴洋. 细胞因子对创伤愈合的影响[J]. 现代生物医学进展, 2011, 11(17): 3370-3372, 3351. |
| [14] | 杜丽, 张庆林, 莘旭妮, 等. 携带人肝细胞生长因子的重组裸质粒对放射复合皮肤创伤促愈作用的实验研究[J]. 创伤外科杂志, 2010, 12(4): 314-318. |



