经典眨眼条件反射(classical eyeblink conditioning,EBC)被广泛应用于研究伤害性运动记忆(aversive motor memory)的神经生理学研究。在EBC建立的过程中,条件刺激(conditioned stimulus,CS,如纯音)需要不断地被非条件刺激(unconditioned stimulus,US,如角膜吹气)所强化。行为学上,EBC可以被分为延迟性眨眼条件反射和痕迹性眨眼条件反射两种模式。前者中CS和US的出现时间具有重叠,而后者CS与US之间则存在一个时间间隔。故动物需要保留关于CS的记忆痕迹,并做出针对CS的眨眼运动行为,即条件性眨眼反应(conditioned eyeblink response,CR)。在生物学上,CR必须具有相当大的发生概率、精确的发生时间(如发生在施予US之前)和适宜的发生强度(如眨眼幅度),才能保护动物眼角膜免受US伤害。有趣的是,如果CS不再被US强化,已习得的CR就会逐渐消退[1]。目前观点认为,条件发射的消退是一种主动的学习过程,它抑制了对原有记忆的提取或表达[2, 3]。近年来,本课题组成功建立了豚鼠EBC模型[4],确定了豚鼠延迟和痕迹性眨眼条件反射建立过程中各类眨眼反应的变化特征[5]。在此基础上,本实验拟进一步比较豚鼠延迟性和痕迹性眨眼条件反射消退的行为学特征,旨在为后期研究伤害性运动记忆消退的生理学机制奠定基础。 1 材料与方法 1.1 实验动物
实验选用成年雄性白化Dunkin-Hartley豚鼠27只,体质量450~600 g(重庆医科大学实验动物中心提供)。受试动物按照随机抽签法分成为2组,分别接受不同时间模式的眨眼条件反射训练:延迟性眨眼条件反射组(n=13,延迟组)和痕迹性眨眼条件反射组(n=14,痕迹组)。在实验期间,每只豚鼠均在室温条件下单笼饲养,自由饮食和进水。 1.2 手术和行为训练
手术的基本流程和EBC的习得过程参照本课题组既往的方法[5]。消退训练是在习得期结束后的第1天开始。总体而言,在EBC消退的训练阶段,其他实验条件不变,但CS开始后不再被给予US进行强化。 1.3 统计学处理
眨眼反应测量和分析方法参见文献[6]。数据以x±s表示,采用SPSS 13.0统计软件进行分析。每组动物CR发生率和拓扑学特征的变化采用重复测量数据的方差分析,而两组动物之间CR发生率和保留率的比较则采用混合设计的双因素方差分析。CR自发恢复的分析采用配对样本t检验。 2 结果 2.1 延迟性和痕迹性眨眼条件反射建立过程中CR的变化
通过1~10 d的延迟性眨眼条件反射配对训练,CR的发生率显著增加(P<0.05),并于训练第4天达到平台期[CR发生率:(93.0±1.5)%]。延迟性眨眼条件反射配对训练(131.8±9.0)次后,CR发生率即可达到70%水平。类似的,在痕迹性眨眼条件反射训练的1~10 d,CR发生率逐渐增加(P<0.05),并于训练的第9天到达平台期[CR发生率:(80.3±3.7)%]。 但相对而言,痕迹组动物需要(317.9±28.0)次配对训练,才能使CR发生率达到70%水平,显著多于延迟组动物所需的训练次数(P<0.05)。
与CR发生率的变化趋势相似,在延迟性眨眼条件反射配对训练的1~10 d,CR的幅度逐渐增加(P<0.05,图 1),并于配对训练的第5天到达平台期[CR幅度:(7.3±0.7) mV]。在第10天,延迟组动物CR幅度为(7.6±0.8) mV,而痕迹组动物CR幅度为(3.5±0.3) mV。此外,在10 d的眨眼条件反射配对训练过程中,延迟组动物的CR幅度均始终显著高于痕迹组动物(P<0.05)。以上结果表明:相对于延迟组动物,痕迹组动物CR习得速率更慢。
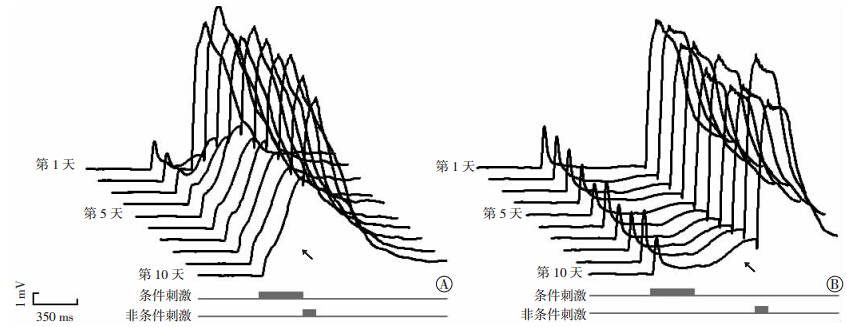 |
| 图 1 豚鼠延迟性(A)和痕迹性(B)眨眼条件反射习得速率的比较↑:示条件性眨眼反应 |
结果显示:不论是延迟组还是痕迹组动物,CR发生率在消退训练期均逐渐减少(P<0.05)。在消退训练的第1天,延迟组和痕迹组动物的CR发生率为分别为(85.7±3.0)%和(58.9±6.7)%。而在消退训练的第7天,延迟组和痕迹组动物CR发生率则为分别为(24.6±5.8)%和(25.9±5.6)%。以上结果表明:在没有US强化的情况下,针对CS的CR会逐渐消失(图 2)。由于延迟性和痕迹性眨眼条件反射在第1~10天的习得水平显著不同(图 1),为比较这两种模式CR的实际消退速率,我们计算了消退训练期间两组动物每天的CR保留率(如第11天CR发生率/第10天CR发生率)。结果显示,尽管在消退训练的第1天,延迟组动物CR保留率为(91.0±3.8)%,显著高于痕迹组动物CR保留率(72.6±7.4)%(P<0.05)。但就整个消退期而言,延迟组动物CR保留率与痕迹组动物CR保留率在统计学上是相当的(P>0.05)。这些结果提示:两种时间模式的眨眼条件反射具有相似的消退速率。
 |
| 图 2 豚鼠延迟性(A)和痕迹性(B)眨眼条件反射消退的比较↑:示条件性眨眼反应 |
结果显示,延迟性CR的峰潜伏期在消退过程中显著前移(P<0.05,图 3A),而痕迹性CR的峰潜伏期则保持相对恒定(P>0.05,图 3B)。
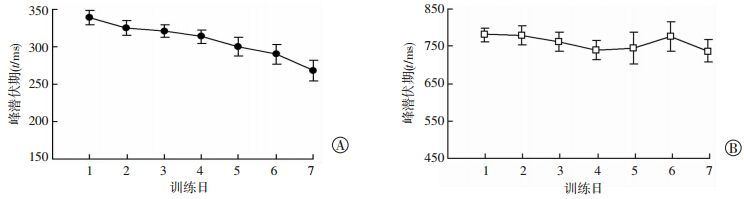 |
| 1~7:分别为训练的第11~17天 图 3 豚鼠延迟性(A)和痕迹性(B)眨眼条件反射消退的行为学特征 |
延迟组动物在训练的第13、14、15、16天和第17天均发生明显的自发恢复现象,表现为第1组训练中的CR发生率显著高于前一训练日最后1组训练中的CR发生率(P<0.05,图 4)。相比较而言,痕迹组动物的自发恢复则不明显(P>0.05,图 4)。
 |
| 1~5:分别为单日内5个连续训练组;a:P<0.05,第12天第5组比较;b:P<0.05,与第13天第5组比较;c:P<0.05,与第14天第5组比较;d:P<0.05,与第15天第5组比较;e:P<0.05,与第16天第5组比较 图 4 豚鼠延迟性和痕迹性眨眼条件反应自发恢复的比较 |
在EBC建立过程中,动物需要形成针对CS的防御性眨眼运动行为,以保护眼角膜免受US伤害。但当外界环境发生变化,特别是没有US强化CS时,CR就应消失,以使动物的运动行为能适应变化的外界环境[7]。目前发现:在某些精神疾病(如精神分裂症)和脑老化患者中,伤害性运动记忆的消退均受到严重损害[8, 9]。因此,研究该类记忆消退的行为学特征,进而确定相关的神经生理学机制,对于改善患者相关临床症状就具有重要意义。
在本研究中,我们发现:尽管延迟性和痕迹性EBC建立的速率存在显著地差异,但二者的消退速率却是相同的。这一结果提示:EBC的建立和消退可能依赖于不同的机制。支持这种可能的证据还在于:我们既往发现EBC建立过程中CR峰潜伏期在第2~3天即进入平台期[10],而在本研究的EBC消退过程中CR峰潜伏期则是逐渐前移或者保持恒定(图 3)。目前认为,EBC消退并非记忆的简单遗忘。相反,它是一个学习过程,需要主动抑制对原有运动性记忆的提取和(或)表现[11]。研究证实:运动性记忆主要存储在小脑中,其特定神经元(如浦肯野细胞)的发放活动控制着运动性记忆的表现[12]。因此,在EBC的消退过程中,需要其他脑结构对小脑的眨眼相关发放活动进行抑制。目前发现,头端内侧前额叶皮层(rostral medial prefrontal cortex,rmPFC)在眨眼条件反射的消退过程中活动增强[13]。激活该区域可使CR表现受到抑制,而失活该区域则可以使CR表现增强,故被推测可能在EBC的消退过程中发挥抑制运动记忆的作用[14]。我们最近工作则证实,mPFC与小脑在EBC消退过程中存在theta频带(5~10 Hz)振荡活动的显著相关性,为眨眼条件反射的消退可能需要rmPFC与小脑的相互作用提供了支持证据[6],该机制区别于EBC建立所依赖于小脑的可塑性机制[15]。
如前所述,EBC消退需要主动抑制原有运动记忆的提取和表现。支持之一观点的证据是:消退训练后,小脑突触传递的可塑性仍然部分保留[16]。如果某些原因引起这种主动抑制减弱,原有的运动性记忆就会重新表现出来,即EBC的自发恢复。本研究显示延迟性EBC消退过程中具有明显的自发恢复现象(图 4)。这一结果支持了EBC消退的“主动学习”学说。但相对而言,痕迹性EBC自发恢复则不显著。这可能是由于延迟性条件反射消退具有更强场景特异性所致[17],相关的神经机制仍需要进一步确定。
综上所述,EBC是研究伤害性运动记忆的理想模型。该反射消退的行为学特征提示:不同时间特性CR的消退,可能具有不同神经机制。深入探讨介导EBC消退的生物学基础,有望为减轻患者的伤害性运动记忆消退障碍症状提供新思路。
| [1] | Kehoe E J, Ludvig E A, Sutton R S. Time course of the rabbit’s conditioned nictitating membrane movements during acquisition, extinction, and reacquisition[J]. Learn Mem, 2014, 21(11): 585-590. |
| [2] | Kalmbach B E, Mauk M D. Multiple sites of extinction for a single learned response[J]. J Neurophysiol, 2012, 107(1): 226-238. |
| [3] | Orsini C A, Maren S. Neural and cellular mechanisms of fear and extinction memory formation[J]. Neurosci Biobehav Rev, 2012, 36(7): 1773-1802. |
| [4] | 杨丽, 胡波, 范郑丽, 等. 不同眼轮匝肌活动记录方法对豚鼠痕迹性眨眼条件反射建立的影响[J]. 第三军医大学学报, 2009, 31(18): 1732-1735. |
| [5] | 陈浩, 胡波, 杨丽, 等. 延迟性和痕迹性条件反射建立过程中豚鼠眨眼反应特征参数的变化[J]. 第三军医大学学报, 2010, 32(2): 95-98. |
| [6] | Wang Y J, Chen H, Hu C, et al. Baseline theta activities in medial prefrontal cortex and deep cerebellar nuclei are associated with the extinction of trace conditioned eyeblink responses in guinea pigs [J]. Behav Brain Res, 2014, 275: 72-83. |
| [7] | Carrel A J, Zenitsky G D, Bracha V. Blocking glutamate-mediated inferior olivary signals abolishes expression of conditioned eyeblinks but does not prevent their acquisition [J]. J Neurosci, 2013, 33(21): 9097-9103. |
| [8] | Parker K L, Andreasen N C, Liu D, et al. Eyeblink conditioning in unmedicated schizophrenia patients: a positron emission tomography study [J]. Psychiatry Res, 2013, 214(3): 402-409. |
| [9] | Thurling M, Galuba J, Thieme A, et al. Age effects in storage and extinction of a naturally acquired conditioned eyeblink response [J]. Neurobiol Learn Mem, 2014, 109: 104-112. |
| [10] | Chen H, Yang L, Chen F, et al. Functional inactivation of orexin 1 receptors in the cerebellum disrupts trace eyeblink conditioning and local theta oscillations in guinea pigs [J]. Behav Brain Res, 2013, 250: 114-122. |
| [11] | Robleto K, Poulos A M, Thompson R F. Brain mechanisms of extinction of the classically conditioned eyeblink response [J]. Learn Mem, 2004, 11(5): 517-524. |
| [12] | Longley M, Yeo C H. Distribution of neural plasticity in cerebellum-dependent motor learning[J]. Prog Brain Res, 2014, 210: 79-101. |
| [13] | Leal-Campanario R, Delgado-Garcia J M, Gruart A. The rostral medial prefrontal cortex regulates the expression of conditioned eyelid responses in behaving rabbits[J]. J Neurosci, 2013, 33(10): 4378-4386. |
| [14] | Leal-Campanario R, Fairen A, Delgado-Garcia J M, et al. Electrical stimulation of the rostral medial prefrontal cortex in rabbits inhibits the expression of conditioned eyelid responses but not their acquisition [J]. Proc Natl Acad Sci U S A, 2007, 104(27): 11459-11464. |
| [15] | Carey M R. Synaptic mechanisms of sensorimotor learning in the cerebellum [J]. Curr Opin Neurobiol, 2011, 21(4): 609-615. |
| [16] | Tracy J A, Thompson J K, Krupa D J, et al. Evidence of plasticity in the pontocerebellar conditioned stimulus pathway during classical conditioning of the eyeblink response in the rabbit [J]. Behav Neurosci, 2013, 127(5): 676-689. |
| [17] | Grillon C, Alvarez R P, Johnson L, et al. Contextual specificity of extinction of delay but not trace eyeblink conditioning in humans[J]. Learn Mem, 2008, 15(6): 387-389. |



