既往研究表明,弥漫性轴索损伤(diffuse axonal injury,DAI)后脑内N-乙酰天冬氨酸 (N-acetyl aspartate,NAA)、N-乙酰天冬氨酸/肌酸(NAA/Cr)含量下降伴随 着乙酰胆碱(choline,Cho)、乙酰胆碱/肌酸(Cho/Cr) 的上升[1],并认为NAA/Cr等变化可以预测其预后。醒脑静注射液被认为具有抗凝、增强组织细胞耐缺氧能力,调节中枢神经系统平衡作用,可改善DAI患者预后,缩短昏迷时间,但其对DAI患者脑内化合物NAA、Cr代谢的影响尚不清楚。本研究通过观察醒脑静注射液治疗重度DAI患者的格拉斯哥昏迷评分(GCS)评分及对MRS的NAA/Cr及Cho/Cr定量分析,探讨醒脑静对DAI患者的脑代谢影响及脑保护作用机制。 1 资料与方法 1.1 一般资料
选取我院神经外科2012年10月至2013年10月收治的40例重度DAI住院患者,入选标准:年龄20~50岁,其中男性29例,女性11例,有明确的外伤史,伤后昏迷时间>30 min,GCS评分为5~8分,伤后24 h 内入院,无明确神经定位体征。影像学或临床支持诊断,有明确的外伤史,昏迷时间>6 h,CT或MRI提 示中线结构处多发出血灶或非出血性损伤,临床症状严重与影像学不符[2],排除孕妇,合并有其他系统严重外伤者,伤前有心、 脑血管疾病史者,不能配合检查者。将患者按随机数字表分为两组,两组患者在GCS评分、性别、年龄均无统计学差异(P>0.05)。 1.2 方法
给药方法:对照组给予基础治疗[2],治疗组在基础治疗上每天给予5%GS 250 mL+醒脑静注射液(无锡济民可信山禾药业,5 mL/支,国药准字号Z32020563)20 mL静脉滴注。基础治疗(包括维持水盐电解质平衡、营养支持、控制血压、控制体温等)两组相同。2组均在24 h,治疗后15、30 d进行GCS评分,1H-MRS进行NAA/Cr及Cho/Cr定量分析(MRI由泸州医学院附属医院提供,飞利浦,荷兰公司,3.0T)。 1.3 检测及分析步骤
常规行头颅MRI检查明确损伤部位及性质后选取胼胝体膝部、压部和基底节1H-MRS各指标的波峰下面积,计算各指标和Cr波峰下面积的比值,分别以NAA/Cr、Cho/Cr代表脑内相对含量(图 1、2)。
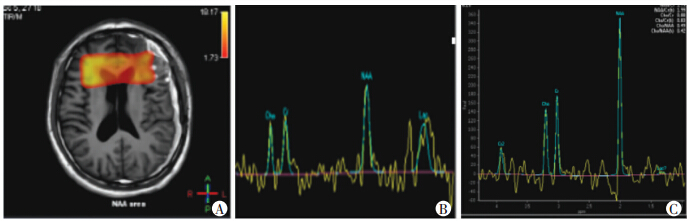 |
| 图 1 治疗组MRI表现(A)及15(B)、30 d(C)波谱成像(橘黄色区域代表多体素波谱分析选择的扫描视野,即感兴趣区域) |
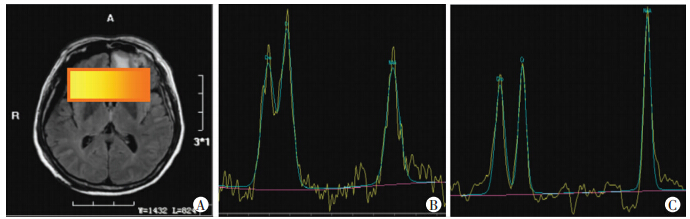 |
| 图 2 对照组MRI表现(A)及15(B)、30 d(C)波谱成像(橘黄色区域代表多体素波谱分析选择的扫描视野,即感兴趣区域) |
采用SPSS 13.0统计软件,数据均以x±s表示,行方差分析。 2 结果 2.1 2组患者GCS评分
治疗后15、30 d醒脑静治疗组GCS评分较对照组升高(P<0.05,P<0.01,表 1)。
| 组别 | 24 h | 15 d | 30 d |
| 对照组 | 6.11±1.10 | 8.63±1.34 | 9.68±1.60 |
| 治疗组 | 6.30±1.03 | 9.55±1.23 | 11.80±2.12 |
| F | 0.326 | 4.955 | 12.29 |
| P | 0.572 | 0.032 | 0.001 |
醒脑静注射液治疗第15天和第30天,脑内 NAA/Cr 定量较常规治疗组升高(P<0.05,P<0.01),而Cho/Cr量降低(P<0.05,表 2)。
| 组别 | NAA/Cr | Cho/Cr | ||||
| 24 h | 15 d | 30 d | 24 h | 15 d | 30 d | |
| 对照组 | 0.87±0.14 | 1.08±1.44 | 1.45±1.28 | 0.98±0.12 | 0.86±0.11 | 0.65±0.12 |
| 治疗组 | 0.84±0.13 | 1.17±1.32 | 1.61±0.16 | 0.98±0.11 | 0.79±0.87 | 0.55±0.12 |
| F | 0.443 | 4.378 | 12.404 | 0.031 | 5.484 | 7.474 |
| P | 0.510 | 0.043 | 0.001 | 0.860 | 0.025 | 0.010 |
DAI是最常见的创伤性颅脑损伤类型,白质纤维和轴突的损伤加剧大脑功能障碍,常规CT和MRI是很难作出一个积极的诊断,功能性磁共振成像能提高诊断检出率,近年来多有研究采用MR波谱成像检测脑内代谢物浓度,从而判断损伤程度及预后[3]。本实验发现伤后24 h脑内NAA/Cr开始降低,而Cho/Cr升高,与国内外相关研究一致。临床研究发现DAI患者外伤后 NAA/Cr较正常人显著降低,并认为NAA、NAA/Cr与昏迷时间呈负相关,与GCS评分呈正相关,且NAA/Cr比值越低越提示预后不良[4]。NAA降低提示神经元及轴索的缺损或功能不全,其机制可能是由于脑损伤后代谢合成受抑,NAA加速分解以满足细胞供能的需要及髓鞘修复的脂质合成[5, 6]。脑内Cho变化虽然不能提示预后[7],但仍有研究表明,DAI患者Cho显著升高可能与神经胶质细胞增生及脱髓鞘改变时胞膜裂的产物相关[3]。
醒脑静注射液的主要成分为麝香、郁金、冰片、栀子等,是一种新型中药复方制剂,具有抗炎、兴奋中枢、解热、耐缺氧等作用,临床广泛用于脑炎、肺性脑病、意识障碍、卒中等,疗效安全、可靠。在脑内可以通过减轻脑水肿、稳定血脑屏障、抑制炎症反应、改善细胞代谢、抑制胶质细胞增生等途径达到脑保护作用[8, 9]。研究表明DAI患者早期使用醒脑静注射液可改善预后,缩短昏迷时间[10],其机制可能是通过改善局部循环,缓解脑组织缺血缺氧状况,提高脑细胞耐缺氧能力阻断因缺氧而造成的一系列脑损伤起脑保护作用,同时通过抗氧化及清除自由基作用起到脑保护作用[11]。但目前尚缺乏醒脑静对DAI患者脑内化合物代谢的影响及机制的相关研究,故本研究采用1H-MRS分析NAA/Cr、Cho/Cr值探讨醒脑静注射液对DAI患者脑内化合物代谢的影响,并探讨其机制。
本组资料显示,DAI患者使用醒脑静治疗后GCS评分较对照组升高(P<0.05),结果表明早期使用醒脑静注射液治疗DAI患者可以改善患者的意识障碍 ,提高GCS评分。醒脑静治疗组15、30 d其脑内NAA/Cr 较对照组升高,而Cho/Cr较对照组降低(P<0.05)。在既往的研究中我们发现醒脑静能够维持神经细胞的机能,能增加脑内葡萄糖及氧的利用[12],此外,醒脑静可以通过修复血脑屏障、减轻炎症反应等一系列脑保护作用减少脑组织的耗氧量[13],因此推断醒脑静注射液通过减少脑细胞需氧量使得NAA代谢分解减少,脑内NAA/Cr升高。另一方面,醒脑静注射液具有修复血脑屏障减轻细胞水肿作用,减轻炎症反应抑制细胞凋亡[8],胶质细胞增生减少从而Cho/Cr降低。本研究结果提示醒脑静注射液可以改善脑内代谢及细胞功能,减少神经元及细胞膜的损伤,提高脑内化合物的代谢率,促进意识障碍的恢复,发挥脑保护作用。
本研究通过对DAI患者进行GCS评分及脑内NAA/Cr、Cho/Cr的含量分析表明:脑内NAA/Cr及Cho/Cr的含量能反映患者的脑损伤程度及预后,与对照组比较,醒脑静治疗可以提高患者的脑内NAA/Cr值,减少Cho/Cr值,促进神经功能恢复,改善预后,进一步证实了醒脑静注射液在DAI患者中的临床应用价值,但对于醒脑静注射液的治疗剂量、治疗时间窗与疗效的相关关系仍有待进一步研究。我们希望在未来的研究中,能进一步探索醒脑静注射液对DAI的疗效及相关机制。
| [1] | Chen J, Jin H, Zhang Y, et al. MRS and diffusion tensor image in mild traumatic brain injuries[J]. Asian Pac J Trop Med, 2012, 5(1): 67-70. |
| [2] | Zheng W B, Liu G R, Li L P, et al. Prediction of recovery from a post-traumatic coma state by diffusion-weighted imaging (DWI) in patients with diffuse axonal injury[J]. Neuroradiology, 2007, 49(3): 271-279. |
| [3] | 赵兆, 于建云, 吴昆华, 等. 磁共振弥散张量成像与质子磁共振波谱技术在脑损伤鉴定中的应用[J]. 法医学杂志, 2012, 28(3): 207-210. |
| [4] | Babikian T, Marion S D, Copeland S, et al. Metabolic levels in the corpus callosum and their structural and behavioral correlates after moderate to severe pediatric TBI[J]. J Neurotrauma, 2010, 27(3): 473-481. |
| [5] | 于明琨, 叶春琳. 磁共振波谱分析与外伤性脑损伤研究[J]. 中华神经医学杂志, 2004, 3(1): 70-74. |
| [6] | Jansen J F, Backes W H, Nicolay K, et al. 1H MR spectroscopy of the brain: absolute quantification of metabolites[J]. Radiology, 2006, 240(2): 318-332. |
| [7] | Holshouser B A, Tong K A, Ashwal S. Proton MR spectroscopic imaging depicts diffuse axonal injury in children with traumatic brain injury[J]. AJNR Am J Neuroradiol, 2005, 26(5): 1276-1285. |
| [8] | Xu P, Du P, Lu Y, et al. The effect of stroke and other components in Xing-Nao-Jing on the pharmacokinetics of geniposide[J]. J Ethnopharmacol, 2014, 152(2): 302-307. |
| [9] | Peng W, Yang J, Wang Y, et al. Systematic review and meta-analysis of randomized controlled trials of xingnaojing treatment for stroke[J]. Evid Based Complement Alternat Med, 2014, 2014: 210851. |
| [10] | 廖圣芳, 王玉差, 张义王, 等. 醒脑静注射液治疗弥漫性轴索损伤的临床研究[J]. 现代中西医结合杂志, 2014, 23(4): 360-362. |
| [11] | 王寅安. 醒脑静注射液对脑保护作用的临床研究[J]. 临床医药实践, 2008, 17(12): 990-991. |
| [12] | 朱志鑫, 单利华. 脑醒静注射液治疗急性脑出血50例疗效观察[J]. 海峡药学, 2009, 21(4): 143-144. |
| [13] | 关宏, 武变瑛, 张丽娜, 等. 醒脑静对中重度颅脑损伤患者血清sFractalkine含量的影响及临床意义[J]. 河北医药, 2011, 33(8): 1129-1131. |



