mitsugumin 53(MG53)是三重结构域蛋白家族成员(tripartite motif containing 72,TRIM72),属于肌特异性蛋白,主要分布在骨骼肌和心肌组织,其余组织很少表达或者没有表达[1]。MG53对细胞膜的修复作用在骨骼肌细胞和心肌细胞中都得到了证实[1, 2, 3]。MG53-/-小鼠在缺血再灌注(ischemia/reperfusion,I/R)过程中损伤更严重,心肌缺血面积、LDH、凋亡细胞数量等明显升高,而在细胞实验中,过表达MG53的细胞能有效地减少缺氧-复氧损伤,证实了MG53在心脏I/R损伤中发挥了重要保护作用[4, 5]。然而MG53对心脏缺血再灌注心律失常是否具有保护作用。因此,我们采用SD大鼠心脏进行Langendorff灌流研究,观察MG53蛋白预处理在缺血再灌注心律失常中的作用。 1 材料与方法 1.1 实验材料
8~10周龄SPF级健康SD大鼠40只,雌雄各半,体质量200~240 g,由第三军医大学大坪医院野战外科研究所实验动物中心提供。Krebs-Henseleit(K-H)液配方如下(mmol/L):NaCl(118.5),KCl(4.7),MgSO4(1.2),CaCl2(1.8),NaHCO3(24.8),KH2PO4(1.2),Glucose(10),pH值为7.2~7.4[6]。MG53蛋白由俄亥俄州立大学麻建杰教授提供。 1.2 方法 1.2.1 Langendorff模型制备
SD大鼠肝素化(500 U/kg)15 min后,腹腔注射2.5%戊巴比妥钠2.5 mL/kg 常规麻醉,确认麻醉效果后,迅速开胸取出大鼠心脏置于预冷的无钙K-H液里,使其短暂停跳,暴露主动脉,悬挂于Langendorff灌流装置上,用95%O2-5%CO2鼓泡式氧和的K-H液经主动脉逆行灌注,恒流8 mL/min,恒温(37.0±0.5)℃。心脏固定完成后,用带针7/0号线贯穿冠状动脉左前降支的两端和基底部,该血管表面放置带凹槽硅胶管,连接心脏表面心电图[7, 8]。平衡20 min,结扎左冠前降支,进入缺血期;持续30 min后,在凹槽处剪断缝线,即为再灌注期,持续30 min。 1.2.2 动物分组
离体灌注的大鼠心脏经平衡期后分为5组(n=8):① Sham组:平衡期后予常规K-H液灌注60 min;②缺血再灌注(I/R)组:平衡期后缺血30 min,再灌注30 min,全程予常规K-H液灌注;③MG53低浓度+I/R组:平衡10 min后,予含MG53蛋白0.35 μg/mL的K-H液继续平衡10 min,缺血30 min,再灌注30 min,缺血期与再灌注期予常规K-H液;④MG53中浓度+I/R组:平衡10 min后,予含MG53蛋白0.7 μg/mL的K-H液继续平衡10 min,余同③;⑤MG53高浓度+I/R组:平衡10 min后,予含MG53蛋白1.4 μg/mL的K-H液继续平衡10 min,余同③。 1.2.3 心律失常的监测
心电图电极正极接左室,负极接右房,使用Labchart软件记录心电图参数。心律失常评判参考Curist-Walker评分标准[9],①0分:<10次室性早搏(VPB);②1分:>10次VPB;③2分:1~5次室性心动过速(VT);④3分:>5次VT或者1次室颤(VF)(VT和VF总共持续时间<40 s);⑤4分:由VT转化的VF 2~5次,且VF持续时间总和<80 s;⑥5分:由VT转化为VF>5次,且VF持续时 间总和<160 s;⑦6分:VT和VF总共持续时间<300 s;⑧7分:VT和VF总共持续时间>300 s。 1.3 统计学分析
心律失常评分及持续时间以x±s表示,采用SPSS 18.0统计软件。心率、心律失常评分采用单因素方差分析,其中两两比较采用LSD法。室速、室颤发生率采用Fisher确切概率法。室速、室颤持续时间采用Kruskal-Wallis H检验。 2 结果 2.1 典型心律失常
缺血再灌注心律失常多于再灌注早期出现,常表现为VPB、VT以及VF等快速心律失常,典型心律失常心电图见图 1。I/R组常发生持续性VT以及VF,给予MG53中、高浓度预处理后未见VF发生,多发生短暂VT及VPB(心电图来源,窦性心律、室性早搏:MG53高浓度预处理组,室性心动过速、不可逆性室颤:I/R组,可逆性室颤:MG53低浓度预处理组)。
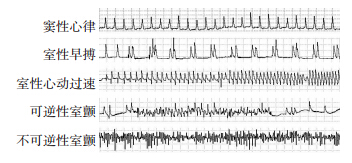 |
| 图 1 再灌注期间发生的典型心电图 |
各组平衡期均无心律失常的发生,且MG53预处理后各组基础心率无明显差异(P>0.05)。与I/R组相比,虽MG53低浓度预处理组再灌注心律失常评分及VF发生率降低,但两者差异不具有统计学意义(P>0.05);MG53中、高浓度预处理组较I/R组能显著降低再灌注心律失常评分(P<0.01),减少再灌注期VT发生率(P<0.01)以及VF发生率(P<0.05),缩短VT、VF持续时间(P<0.05)。与MG53低浓度预处理组比较,MG53中、高浓度预处理组能明显降低VT发生率(P<0.01)。MG53中、高浓度预处理组在心律失常评分、VT及VF发生率、VT持续时间上,两组差异无统计学意义(P>0.05,表 1)。
| 分组 | 平衡期心率(/min,x±s) | 心律失常评分(x±s) | VT发生率(%) | VF发生率(%) | VT持续时间(s,x±s) | VF持续时间(s,x±s) |
| Sham组 | 295.6±31.8 | 0 | 0 | 0 | 0 | 0 |
| I/R组 | 296.2±24.5 | 3.4±2.4 | 75.0 | 37.5 | 118.0±208.3 | 310.9±604.1 |
| MG53低浓度+I/R组 | 288.0±26.3 | 2.6±1.9 | 75.0 | 25.0 | 137.9±348.6 | 99.2±280.1 |
| MG53中浓度+I/R组 | 279.4±22.3 | 1.4±0.7a | 50.0ac | 0a | 3.7±5.0a | 0a |
| MG53高浓度+I/R组 | 289.4±27.7 | 1.1±0.8b | 37.5ac | 0a | 2.2±3.6a | 0a |
| a:P<0.05,b:P<0.01,与I/R组比较;c:P<0.05,与MG53低浓度+I/R组比较 | ||||||
缺血再灌注心律失常是临床常见的电生理现象,也是患者死亡的重要原因。随着冠心病治疗方法的改进,特别是急诊PCI的早期使用,该现象的发生率越来 越高。再灌注心律失常是I/R中的一种主要表现形式,但也有别于传统意义上的I/R,主要表现为离 子通道和电传导的异常。Valle等[10]发现在该医院85位PCI术后死亡病人中,因再灌注心律失常死亡的有12位,占12.1%,是导致病人死亡的三大原因之一。因此,防治再灌注心律失常成为临床上针对I/R的重要研究课题。
再灌注心律失常发生机制极其复杂,包括钙超载、氧自由基增加、缝隙连接重塑、游离脂肪酸增加等[11, 12, 13, 14, 15]。目前治疗再灌注心律失常的药物主要针对钙离子超载、氧自由基等,效果都不理想,但无针对缝隙连接重塑的药物,而缝隙连接在再灌注心律失常中的作用越来越受到重视。缝隙连接蛋白家族包括大约20个成员,其中Cx43是哺乳动物心室中最主要的缝隙连接蛋白,主要存在于细胞膜上。生理状态下,Cx43以磷酸化形式呈簇状分布于心肌闰盘处,形成缝隙连接通道的特点、数目、大小及互相连接的心肌细胞的几何形状促进了电冲动在纵向的优势传导,是正常心肌冲动各向异性传导的解剖学基础[16]。I/R过程中心肌缝隙连接的变化主要有:Cx43的去磷酸化以及缝隙连接侧面化[17] 。
Cx43主要存在于细胞膜上,而MG53已被证实与胞浆内囊泡和肌纤维膜紧密结合,在细胞膜结构损伤后,MG53蛋白可在膜破损处聚集,封闭破损的细胞膜,参与其修复从而发挥保护作用[1, 2, 3, 18],提示其能够在细胞膜受损时修复细胞膜使Cx43的磷酸化水平及分布维持稳定,从而降低再灌注心律失常的恶性程度。故Cx43可能在MG53预处理改善缺血再灌注心律失常中发挥重要作用及其具体机制,还需进一步验证。
本实验利用Langendorff离体灌流装置,选择再灌注心律失常评分、VT和VF的发生率以及持续时间作为观察指标,反映再灌注心律失常的严重程度。结果表明MG53蛋白预处理能明显降低VT和VF的发生率,缩短VT和VF的持续时间,降低再灌注心律失常分数。提示MG53蛋白预处理能改善缺血再灌注心律失常,而缺血预适应(ischemic preconditioning,IPC)能够增加MG53的表达[4],同时IPC已被证实可显著减少或减轻多种实验动物的再灌注心律失常发生率及严重程度[19, 20],由此间接证实MG53在改善再灌注心律失常中发挥了重要作用。MG53蛋白成为治疗再灌注心律失常的一个重要靶点,可能会给PCI术、溶栓的患者带来益处,但其调控机制,有待进一步研究。
| [1] | Weisleder N, Lin P, Zhao X, et al. Visualization of MG53-mediated cell membrane repair using in vivo and in vitro systems[J]. J Vis Exp, 2011(52).pii: 2717. |
| [2] | Cai C, Masumiya H, Weisleder N, et al. MG53 nucleates assembly of cell membrane repair machinery[J]. Nat Cell Biol, 2009, 11(1): 56-64. |
| [3] | Weisleder N, Takeshima H, Ma J. Mitsugumin 53 (MG53) facilitates vesicle trafficking in striated muscle to contribute to cell membrane repair[J]. Commun Integr Biol, 2009, 2(3): 225-226. |
| [4] | Cao C M, Zhang Y, Weisleder N, et al. MG53 constitutes a primary determinant of cardiac ischemic preconditioning[J]. Circulation, 2010, 121(23): 2565-2574. |
| [5] | Zhang Y, Lv F, Jin L, et al. MG53 participates in ischaemic postconditioning through the RISK signalling pathway[J]. Cardiovasc Res, 2011, 91(1): 108-115. |
| [6] | Xi J, McIntosh R, Shen X, et al. Adenosine A2A and A2B receptors work in concert to induce a strong protection against reperfusion injury in rat hearts[J]. J Mol Cell Cardiol, 2009, 47(5): 684-690. |
| [7] | Johansen D, Cruciani V, Sundset R, et al. Ischemia induces closure of gap junctional channels and opening of hemichannels in heart-derived cells and tissue[J]. Cell Physiol Biochem, 2011, 28(1): 103-114. |
| [8] | 周平,蒋鑫,杨小利,等.整合素连接激酶对大鼠离体心脏缺血再灌注室性心律失常的影响[J].第三军医大学学报,2014,36(18):1872-1875. |
| [9] | Curtis M J, Walker M J. Quantification of arrhythmias using scoring systems: an examination of seven scores in an in vivo model of regional myocardial ischaemia[J]. Cardiovasc Res, 1988, 22(9): 656-665. |
| [10] | Valle J A, Smith D E, Booher A M, et al. Cause and circumstance of in-hospital mortality among patients undergoing contemporary percutaneous coronary intervention: a root-cause analysis[J]. Circ Cardiovasc Qual Outcomes, 2012, 5(2): 229-235. |
| [11] | Antoons G, Willems R, Sipido K R. Alternative strategies in arrhythmia therapy: evaluation of Na/Ca exchange as an anti-arrhythmic target[J]. Pharmacol Ther, 2012, 134(1): 26-42. |
| [12] | Liu C N, Yang C, Liu X Y, et al. In vivo protective effects of urocortin on ischemia-reperfusion injury in rat heart via free radical mechanisms[J]. Can J Physiol Pharmacol, 2005, 83(6): 459-465. |
| [13] | Boulaksil M, Winckels S K, Engelen M A, et al. Heterogeneous Connexin43 distribution in heart failure is associated with dispersed conduction and enhanced susceptibility to ventricular arrhythmias[J]. Eur J Heart Fail, 2010, 12(9): 913-921. |
| [14] | Zemljic-Harpf A E, Godoy J C, Platoshyn O, et al. Vinculin directly binds zonula occludens-1 and is essential for stabilizing connexin-43-containing gap junctions in cardiac myocytes[J]. J Cell Sci, 2014, 127(Pt 5): 1104-1116. |
| [15] | Rutledge C A, Ng F S, Sulkin M S, et al. c-Src kinase inhibition reduces arrhythmia inducibility and connexin43 dysregulation after myocardial infarction[J]. J Am Coll Cardiol, 2014, 63(9): 928-934. |
| [16] | Figueroa X F, Duling B R. Gap junctions in the control of vascular function[J]. Antioxid Redox Signal, 2009, 11(2): 251-266. |
| [17] | Sato T, Ohkusa T, Honjo H, et al. Altered expression of connexin43 contributes to the arrhythmogenic substrate during the development of heart failure in cardiomyopathic hamster[J]. Am J Physiol Heart Circ Physiol, 2008, 294(3): H1164-H1173. |
| [18] | Masumiya H, Asaumi Y, Nishi M, et al. Mitsugumin 53-mediated maintenance of K+ currents in cardiac myocytes[J]. Channels (Austin), 2009, 3(1): 6-11. |
| [19] | Yamakawa K, Zhou W, Ko Y, et al. Improved cardioprotection using a novel stepwise ischemic preconditioning protocol in rabbit heart[J]. J Surg Res, 2014, 188(2): 381-386. |
| [20] | Walsh S R, Tang T Y, Kullar P, et al. Ischaemic preconditioning during cardiac surgery: systematic review and meta-analysis of perioperative outcomes in randomised clinical trials[J]. Eur J Cardiothorac Surg, 2008, 34(5): 985-994. |



