长期以来我国尸体供器官的传统来源一直是阻挠器官移植迈向国际化、规范化的主要障碍,饱受争议。2010年3月,原国家卫生部(现卫生计生委)委托中国红十字会正式启动了我国心脏死亡器官捐献(donor after cardiac death,DCD)为重点的人体器官捐献工作。此后移植等待者预约名单系统和器官分配与共享系统相继建立,标志着我国器官移植捐献模式发生了根本性的变革。与我国司法途径的标准供者(standard criteria donors,SCD)肾移植比较,DCD供器官移植在捐献程序、器官获取保存方法和器官质量评估等方面均有不同[1, 2, 3]。本研究对我院2013年1-9月施行的尸体供肾移植进行回顾性分析,对比DCD供肾移植与SCD供肾移植的存活效果。 1 资料与方法 1.1 研究对象
筛选我院2013年1-9月施行的105例尸体供肾移植病例,纳入标准:①成年尸体供者;②初次移植受者;③受者年龄16~70岁;④受者术前群体反应性抗体(PRA)阴性(<10%)。受者排除标准:①两种及以上器官联合移植;②恶性肿瘤病史;③糖尿病史;④使用西罗莫司、硫唑嘌呤或咪唑立宾免疫抑制治疗。共 有89例肾移植受者纳为研究对象,其中依据《中国心脏死亡器官捐献工作指南》[4],完成符合中国Ⅱ类或中国Ⅲ类标准的器官捐献41例,供者年龄23~66岁,平均年龄44.9岁,原发病包括重度颅脑损伤、脑血管意外、脑瘤和电击伤。施行DCD供肾移植术(DCD组)56例,受者男性48例,女性8例,年龄17~64岁,平均年龄41.3岁。同期施行司法途径SCD供肾移植(SCD组)33例,受者男性16例,女性17例,年龄19~59岁,平均年龄39.5岁。供者手术采用腹部十字切口,无菌冰置于腹腔内快速降温,分别经腹主动脉和门静脉插管,HTK液原位灌注,再整块切取肝脏和双肾等腹部脏器。DCD组供肾采用Lifeport低温机器灌注保存(hypothermic machine perfusion,HMP)25例,单纯静态低温保存31例,HMP开始时肾脏阻力为(0.70±0.44) mmHg/(mL·min),结束时阻力下降为(0.21±0.08)mmHg/(mL·min),HMP开始时灌注流量为 (50.92±33.99) mL/min,结束时流量增加至(138.60± 42.19) mL/min;SCD组供肾全部采用单纯低温保存。DCD组与SCD组受者的一般资料见表 1,因SCD组供者资料不全,本研究未做2组供者比较。本研究方案经同济医院伦理委员会批准施行。
| 组别 | 例数 | 年龄(岁) | 男性(%) | BMI | WIT(min) | CIT(h) | HLA错配数 |
| DCD组 | 56 | 41.3±11.3 | 85.7 | 21.8±2.9 | 14.6±2.5 | 8.5±5.1 | 2.9±0.7 |
| SCD组 | 33 | 39.5±11.8 | 48.5 | 21.4±2.0 | 5.8±3.3 | 12.2±4.6 | 2.7±0.6 |
| P值 | 0.39 | <0.01 | 0.41 | <0.01 | <0.01 | 0.09 |
DCD组采用抗体诱导+他克莫司(TAC)+麦考酚酯(MMF)+泼尼松(Pred)四联免疫抑制方案,其中手术当天和术后第1、2天应用兔抗胸腺细胞球蛋白(rATG)25 mg/d或手术当天、 术后第4天分别应用抗CD25单克隆抗体20 mg/d;SCD组采用 TAC+MMF+Pred三联用药。所有受者于手术当天和术后第1、2天予甲基强的松龙500 mg/d静脉滴注,TAC与 MMF自术后第3天开始口服,TAC起始剂量为0.05~0.2 mg/(kg·d ),MMF为1.0~2.0 g/d,以后依据药物浓度监测结果调整剂量,术后3个月内TAC谷值浓度维持于8~10 ng/mL,3个月后5~8 ng/mL。 1.3 急性排斥反应的诊断和治疗 1.3.1 诊断
急性排斥反应的诊断:当患者出现体温升高、尿量减少、移植肾肿大压痛以及血压升高、体质量增加等临床表现,或实验室检查发现不明原因的血肌酐值升高>30 μmol/L,或较基线值升高25%以上时应怀疑急性排斥反应的可能,并排除其他引起肾功能异常的原因,如感染、中毒或移植肾血管/输尿管并发症等,必要时需要经皮肾穿刺活检确诊。 1.3.2 治疗
急性排斥反应的治疗首选大剂量甲基强的松龙冲击疗法,500 mg/d快速静脉滴注,连续3 d,耐激素的急性排斥反应则应用rATG,25~50 mg/d,连用5~7 d;针对其中的急性体液性排斥反应(acute antibody-mediated rejection,AMR),除采用rATG治疗外,还应用血浆置换与大剂量丙种球蛋白(IVIg)或蛋白酶体抑制剂硼替佐米。 1.4 随访评价指标 1.4.1 主要评价指标
移植肾6个月、1年存活率与受者6个月、1年存活率;移植肾功能延迟恢复(delayed graft function,DGF)发生率。DGF是指移植术后1周内需要透析治疗者或术后1周血肌酐下降缓慢、维持于400 μmol/L以上者。 1.4.2 次要评价指标
肾功能状况包括血肌酐值(SCr)和估算肾小球滤过率(estimated glomerular filtration rate,eGFR)、急性排斥反应发生率及感染并发症。受者透析期间的血肌酐值和eGFR不做统计,eGFR采用简化“肾脏病膳食改良试验”(MDRD)公式进行计算,肾小球滤过率[mL/(min·1.73 m2)] =186.3×(SCr/88.4)-1.154×年龄-0.203×(0.742女性)[5]。 1.5 统计学分析
采用SPSS 20.0统计软件,应用Kaplan-Meier生存分析和Log-Rank检验,比较2组术后6个月和1年受者/移植肾存活率、DGF发生率。计量数据以x±s表示,F检验方差齐性,采用双样本等方差t检验或异方差t检验。 2 结果 2.1 受者存活率
随访6~15个月,DCD组56例中有18例随访超过1年,其中因肺部感染死亡1例,受者6个月存活率98.2%(55/56),1年存活率94.4%(17/18);SCD组33例中有14例随访超过1年,其中因肺部感染死亡1例,受者6个月存活率97.0%(32/33),1年存活率92.9%(13/14),2组受者6个月及1年存活率的差异无统计学意义(P>0.05)。 2.2 移植肾存活率
DCD组受者移植肾带功能死亡1例,因假性肾动脉瘤和急性体液性排斥反应导致移植肾切除各1例,移植肾6个月存活率94.6%(53/56),1年存活率83.3%(15/18);SCD组移植肾带功能死亡1例,因AMR导致移植肾失功、肾切除1例,移植肾6个月存活率93.9%(31/33),1年存活率85.7%(12/14),2组 6个月及1年移植肾存活率差异无统计学意义(P>0.05)。 2.3 移植肾功能恢复情况
DGF发生率DCD组为21.4%(12/56),SCD组18.2%(6/33),2组间差异无统计学意义(P=0.20)。术前和术后1周血肌酐值,DCD组与SCD组间差异均无统计学意义(P>0.05),而术后1、3、6、12个月血肌酐值,DCD组均显著高于SCD组,2组间差异有统计学意义(P<0.05,图 1)。2组间eGFR差异在各时间点则均无统计学意义(P>0.05,图 2)。
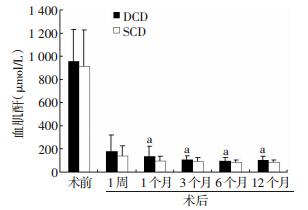 |
| a: P<0.05,与SCD组比较 图 1 2组肾移植受者血肌酐值变化 |
 |
| 图 2 2组肾移植受者eGFR值变化 |
SCD组急性排斥反应发生率12.1%(4/33),其中3例逆转,1例术后早期肾功能恢复正常,第5天出现尿量减少至无尿,术后12 d PRAⅠ类75%,Ⅱ类阴性,穿刺活检证实为AMR,移植肾广泛缺血坏死,遂切除移植肾。DCD组急性排斥反应发生率8.9%(5/56),4例予MP冲击治疗逆转,1例活检证实的AMR经治疗无效而切除移植肾;该受者术前PRA阴性,术后7 d血肌酐升高,移植肾肿胀变硬,PRAⅠ类94.1%,Ⅱ类38.8%,给予血浆置换、IVIg等治疗后复测PRAⅠ类89.2%,Ⅱ类54.1%,未见明显下降,肾穿刺活检提示肾小球广泛微血栓形成。 2.5 感染并发症
DCD组出现间质性肺部感染7例,其中死亡1例,尿路感染2例,单纯-带状疱疹病毒感染3例;SCD组出现肺部感染5例,其中1例并发急性呼吸窘迫综合征(ARDS)死亡,尿路感染4例。 3 讨论
供者器官极度短缺是器官移植发展面临的最突出问题。据美国器官共享与获取网络数据,截至2012年底,全美肾移植术前登记等待者名单接近100 000例,且每年新增34 000例,而每年施行的肾移植数目不过17 000例[6]。我国的形势更不容乐观。终末期肾病患者至2012年底已经达到100多万,进行透析病例信息登记的患者也超过了20万,而每年能够接受肾移植手术的患者不足2%。因此,拓展供器官来源是解决供需失衡的重要途径,即在广泛采用脑死亡(donation after brain death,DBD)器官捐献的基础上,充分利用适宜的DCD供者器官和扩大标准的供者器官。
由于热缺血时间较长,缺血损伤程度较重,因此,相较于DBD供肾,DCD供肾移植术后移植肾原发性无功能(primary non-function,PNF)或DGF发生率较高。Dominguez-Gil等[7]分析了欧洲2 992例DCD供肾移植,结果显示可控型DCD与非可控型DCD供肾移植后DGF发生率分别高达50.2%和75.7%,PNF发生率分别为5%和6.4%。虽然DCD供肾移植后DGF发生率增高,但是研究发现其对移植肾存活效果并没有产生不利影响,移植肾1、5、10年存活率差异无统计学意义[8, 9, 10]。近年来DCD供器官移植数量不断增加。1999-2008年,全美DCD供器官的数量增长了10倍,大约10%的尸体供肾来自于DCD供者[11]。在我国,司法途径供器官的减少直至消失是社会文明发展的大势所趋。由于国际通用的脑死亡标准尚未被国内社会公众普遍认可,对死亡的认识还停留在“心跳停止、自主呼吸消失为死亡”。为了推动和指导公民逝世后器官捐献工作,2011年4月,《心脏死亡器官捐献分类标准》[12]颁布实施,其中除涵盖国际标准化脑死亡器官捐献(DBD,中国Ⅰ类)和国际标准化心脏 死亡器官捐献(DCD,中国Ⅱ类)以外,还开创性地提出了符合现实国情的“中国过渡时期脑-心双死亡标准器官捐献”(DBCD),即中国Ⅲ类标准,明确指出:在潜在供者脑死亡已经确诊的基础上,经由主治医师判断其病情不可逆,预计其撤除心肺生命支持治疗后60 min内死亡,且已得到家属对器官捐献的知情同意者,可以考虑实施DBCD器官捐献[13]。这是在国内脑死亡立法暂时缺位的情况下,将符合中国Ⅰ类的供者按照中国Ⅱ类处理,严格实施器官捐献的现实选择。3年来,国内DCD移植病例数量稳定增长,目前DCD供肾移植数量已占我院年度尸体供肾移植总数的60%左右。
我国司法途径的供者是特殊历史条件下形成的,为特殊类型的心脏死亡器官捐献,供者一般无基础疾病,供器官获取前功能可维持正常水平,热缺血时间短,移植后近远期存活效果较好。而公民心脏死亡后器官捐献因供者存在严重颅脑损伤或心脑血管病变或伴发有器官功能不全,术后出现DGF甚至PNF的危险度明显增加。国内陈国栋等[14]报道69例DCD肾移植后DGF发生率为29%,相较传统尸体肾移植组DGF发生率(13.8%),差异有统计学意义。本研究结果显示,在术后6个月和1年受者存活率与移植肾存活率等指标方面,DCD组与SCD组比较差异没有统计学意义,均取得较好的近期存活效果。虽然DCD组术后1~12个月各随访时间节点受者血肌酐值均显著高于SCD组,但是考虑可能为DCD组中男性受者比例大、血肌酐基线水平高造成的差异影响。通过进一步计算受者eGFR,发现2组eGFR在各时间点并没有统计学差异,表明维持期2组移植肾功能状况相当。本组DCD供肾移植后未出现PNF病例,DGF发生率也低于国外文献报道[7],分析原因可能在于:①DCD供者捐献多数符合中国Ⅲ类(DBCD)标准,是在脑死亡确诊基础上再有计划地撤除呼吸机等生命支持系统,属于“可控制型心脏死亡”(controlled DCD),供肾热缺血时间和冷缺血时间相对较短;而且在器官捐献前的过渡期,我们尽力对潜在供者实施医疗干预,如积极纠正低蛋白血症,采取维持血压、尿量和氧合状态等措施均有利于保护供器官功能。②受者均为初次移植,术前PRA阴性,排除了免疫致敏因素的不利影响;而且受者BMI正常水平,没有供受者体质量比极度不匹配的情况。③HMP的应用明显降低DCD供肾阻力,有助于减轻供肾的缺血灌注损伤,研究显示HMP可以降低DGF发生风险,改善移植肾功能和存活效果[15]。④DCD组供肾热缺血时间虽然明显长于SCD组,但是因为在供肾获取前即能够检测DCD供者的HLA分型和进行免疫学配型筛选,从而在器官获取后可以快速完成供肾分配,这是司法途径供者不具备的优势,所以冷缺血时间DCD组较SCD组显著缩短。而冷缺血时间是DGF发生的独立危险因素,也是影响肾移植存活效果的重要因素之一[16, 17]。⑤采集DCD供者数据资料(年龄、BMI、死亡原因、血生化检验结果、热缺血时间、冷缺血时间等),HMP提供的移植肾灌注动力学参数(如肾脏阻力和灌注流量),以及移植肾零点穿刺活检或快速冰冻切片结果,进行综合分析研判,在实施移植手术前评估DCD供肾的危险指数。研究发现HMP结束时的肾脏阻力既是DGF发生的独立危险因素,也是影响移植肾1年存活率的独立危险因素[18]。因此,肾脏阻力和灌注流量等参数可以作为预测移植术后效果的客观指标。但是术前对供肾质量进行全面准确的评价并非易事,因为DGF发生和移植肾存活效果受到供者、受者和手术等多方面因素影响,所以不能仅仅根据肾脏阻力等单一指标判定供肾的利用或弃用。我们的体会是,针对存在下列情况者,可以考虑供肾弃用:器官获取前供者肌酐清除率(CrCL)低于70 mL/min,供肾热缺血时间超过60 min,HMP结束时供肾流量低于60 mL/min及阻力大于0.6 mmHg/(mL·min),活检发现明显肾小球硬化或中度以上血管、肾小管和间质病变。遵循以上原则,我们在本研究观察期内弃用5个DCD供肾,从而保证了移植成功率,避免了PNF等严重并发症的发生。
AMR在DCD组与SCD组各出现1例,受者术前PRA阴性,但是术后早期出现不明原因的PRA水平快速增高,为新产生的抗HLA抗体,主要以抗HLAⅠ类抗体为主,呈强阳性表达(>80%),最终导致肾脏内广泛微血栓形成、移植肾失功。因此,对于未致敏受者在围手术期出现由新生抗HLA抗体介导的AMR风险应引起足够重视。
综上所述,本研究中DCD供肾移植近期存活效果良好,术后肾功能恢复和维持状况与司法途径SCD供肾移植比较无显著差异。DCD供肾能够成为扩大我国尸体肾移植供者池的重要来源。由于DCD器官捐献工作开展的时间不长,移植受者病例数尚不多,本研究主要评价了DCD供肾移植的近期存活效果,今后还需要 通过持续的病例累积,对其远期存活效果继续随访观察。
| [1] | 霍枫, 汪邵平, 李鹏, 等. 心脏死亡器官捐献获取流程探讨[J]. 中国普外基础与临床杂志, 2012, 19(5): 468-472. |
| [2] | 鞠卫强, 何晓顺, 王东平, 等. 心脏死亡器官捐赠中器官切取的手术方法与技巧总结[J]. 中华器官移植杂志, 2013, 34(1): 24-27. |
| [3] | 刘永锋. 心脏死亡供者器官移植现状及展望[J]. 中华普通外科杂志, 2013, 28(3): 169-172. |
| [4] | 中华医学会器官移植学分会. 中国心脏死亡器官捐献工作指南(2版)[J]. 中华器官移植杂志, 2011, 32(12): 756-758. |
| [5] | Levey A S, Greene T, Kusek J W, et al. A simplified equation to predict glomerular filtration rate from serum creatinine[J]. J Am Soc Nephrol, 2000, 11: A0828. |
| [6] | Organ Procurement and Transplantation Network (OPTN) Data 2012. Available at: |
| [7] | Dominguez-Gil B, Haase-Kromwijk B, Van-Leiden H, et al. Current situation of donation after circulatory death in European countries[J]. Transpl Int, 2011, 24(7): 676-686. |
| [8] | Singh R P, Farney A C, Rogers J, et al. Kidney transplantation from donation after cardiac death donors: lack of impact of delayed graft function on post-transplant outcomes[J]. Clin Transplant, 2011, 25(4): 255-264. |
| [9] | Hoogland E R, Snoeijs M G, van-Heurn L W. DCD kidney transplantation: results and measures to improve outcome[J]. Curr Opin Organ Transplant, 2010, 15(2): 177-182. |
| [10] | Ledinh H, Bonvoisin C, Weekers L, et al. Results of kidney transplantation from donors after cardiac death[J]. Transplant Proc, 2010, 42(7): 2407-2414. |
| [11] | Klein A S, Messersmith E E, Ratner L E, et al. Organ donation and utilization in the United States, 1999-2008[J]. Am J Transplant, 2010, 10( 4 Pt2): 973-986. |
| [12] | 中华人民共和国卫生部医疗服务监管司. 卫生部办公厅关于启动心脏死亡捐献器官移植试点工作的通知(附件1-中国心脏死亡器官捐献分类标准.doc)[EB/OL]. |
| [13] | 王东, 朱继业.心脏死亡器官捐献的伦理学问题[J].中华消化外科杂志, 2013, 12(9): 644-647. |
| [14] | 陈国栋, 袁小鹏, 李军, 等. 心脏死亡器官捐献供肾与传统尸体供肾肾移植的疗效比较[J]. 中华器官移植杂志, 2013, 34(7): 392-395. |
| [15] | Lam V W, Laurence J M, Richardson A J, et al. Hypothermic machine perfusion in deceased donor kidney transplantation: a systematic review[J]. J Surg Res, 2013, 180(1): 176-182. |
| [16] | Doshi M D, Garg N, Reese P P, et al. Recipient risk factors associated with delayed graft function: a paired kidney analysis[J]. Transplantation, 2011, 91(6): 666-671. |
| [17] | Rao P S, Schaubel D E, Guidinger M K, et al. A comprehensive risk quantification score for deceased donor kidneys: the kidney donor risk index[J]. Transplantation, 2009, 88(2): 231-236. |
| [18] | Jochmans I, Moers C, Smits J M, et al. The prognostic value of renal resistance during hypothermic machine perfusion of deceased donor kidneys[J].Am J Transplant, 2011, 11(10): 2214-2220. |



