相较其他部位的颅内动脉瘤,大脑前动脉远端动脉瘤(distal anterior cerebral artery aneurysms,DACAA)临床较少见,手术难度高,漏、误诊率及残废率、病死率较高[1]。近年,随着诊治水平的不断提高,DACAA的手术残废率和病死率明显减少,但治疗效果仍不能令人满意,可能是由于DACAA在临床上相对少见,临床医师通常对其了解不足。DACAA至今仍是神经外科医师面临的巨大挑战之一,具有较高手术难度,容易发生术后并发症,直接影响患者预后。因此,对DACAA的诊断和治疗研究十分必要。我们于2007年1月至2012年12月共收治969例颅内动脉瘤患者,其中手术治疗的DACAA患者32例,本研究对其临床资料进行回顾性分析,旨在探讨DACAA的显微解剖、诊断和外科治疗技术特点。 1 资料与方法 1.1 临床资料
泸州医学院附属医院神经外科2007年1月至2012年12月手术治疗DACAA患者32例,包括男性14例,女性18例。年龄38~75岁,平均54.8岁。均突然起病,主要表现为头痛21例,恶心呕吐15例,意识改变15例,缄默症1例,双下肢无力6例,认知障碍8例,有2例既往(1个月余)有车祸伤颅内血肿清除病史。Hunt-Hess分级Ⅰ级4例,Ⅱ级14例,Ⅲ级9例,Ⅳ级5例。纳入标准:通过CTA诊断为DACAA者,患者及其家属愿意接受手术治疗而无手术禁忌证者。 1.2 影像学检查
CT平扫发现自发性蛛网膜下腔出血27例,蛛网膜下腔出血(subarachnoid hemorrhage,SAH)主要位于前纵裂胼胝体附近,部分还位于侧裂区、鞍上池及扣带回。脑内血肿5例,包括3例胼胝体血肿伴脑室积血及左、右侧额叶血肿各1例。32例中CTA检查发现大脑前动脉远端解剖变异5例(16%),单一大脑前动脉型3例(9%),优势大脑前动脉供应双侧半球与存在胼胝体正中动脉型都为1例(3%)。多发动脉瘤4例,包括1例前交通动脉瘤和右侧大脑前动脉胼周动脉段动脉瘤(责任动脉瘤),1例2个动脉瘤均位于A3段,1例动脉瘤分别位于A2段和左后交通动脉起始部(责任动脉瘤),1例动脉瘤分别位于A2段和右后交通动脉起始部。在32例患者发现的36个动脉瘤中,DACAA为责任动脉瘤30个,均为囊状动脉瘤,直径为2.3~11.7 mm,位于A2段动脉瘤9个,A3段动脉瘤为18个,A4段3个。动脉瘤形状不规则者20个,宽颈动脉瘤为23个(动脉瘤体颈比<1.12)。 1.3 手术方法 1.3.1 治疗选择
根据患者的Hunt-Hess分级、脑血管痉挛情况及DACAA的解剖特点分为显微夹闭手术组(n=22)及介入治疗组(n=10)。夹闭组倾向选择Hunt-Hess分级Ⅰ~Ⅱ、DACAA伴颅内血肿(血肿量>30 mL)、脑血管痉挛情况较重者;介入组倾向选择Hunt-Hess分级Ⅲ~Ⅳ、瘤颈<4 mm、血管痉挛情况较轻及夹闭手术风险较大者。其中夹闭组男性10例,女性12例,平均年龄47.7岁,Hunt-Hess分级Ⅰ级3例,Ⅱ级12例,Ⅲ级6例,Ⅳ级1例;介入组男性 4例,女性6例,平均年龄52.3岁,Hunt-Hess分级 Ⅰ级1例,Ⅱ级2例,Ⅲ级3例,Ⅳ级4例。在手术时机的选择上,家属同意后即尽快手术治疗。发病到手术的时间(24.0±14.3)h(6 h至7 d)。 1.3.2 显微夹闭手术
共22例26个动脉瘤选择显微夹闭手术,包括4例多发动脉瘤及2例介入治疗失败者。根据易接近载瘤动脉、动脉瘤颈以及血肿大小和位置而选择相应的手术入路,多选择额或/和顶纵裂入路,多发动脉瘤者联合动脉瘤侧翼点入路,并先处理责任动脉瘤。经额部纵裂具体操作如下:气管插管全麻下,患者先行腰大池穿刺引流,选额顶正中跨中线切口,采用四边形骨瓣,骨窗过中线以充分显露上矢状窦,便于控制矢状窦出血且牵开大脑镰显露载瘤动脉。硬脑膜翻向上矢状窦,尽力避开或少损伤桥静脉进入纵裂,沿大脑镰向下探查,解剖纵裂及胼胝体池蛛网膜,确认胼胝体和双侧大脑前动脉,根据影像结果确定动脉瘤的位置和术中所见,分辨出载瘤侧大脑前动脉,尽可能在动脉瘤近端解剖出载瘤动脉,然后再沿载瘤动脉向远端分离至动脉瘤。一般不临时阻断载瘤动脉,因为大脑前动脉远段动脉瘤通常体积较小,阻断后不利于暴露,且由于大多数大脑前动脉远段动脉瘤瘤颈较宽,夹闭角度有限,术中需要多颗动脉瘤夹进行夹闭。与Willis环动脉瘤的术中处理不同的是,术中常需彻底显露动脉瘤瘤体,才好对瘤颈塑形,如发现术中夹闭不全或怀疑夹闭载瘤动脉,需及时调整。本组共夹闭动脉瘤颈25个,烧灼切除1个(右额极动脉终末分支动脉瘤)。 1.3.3 介入栓塞治疗
10例10个动脉瘤(包括2例未破裂DACAA)采用介入治疗,在气管插管全麻下,行全身肝素化,常规DSA检查。将导引导管放置在C3水平并保持稳定,微导管根据动脉瘤的形态塑形,在微导丝的引导下将微导管送入动脉瘤内,依次填塞弹簧圈,直至动脉瘤填塞至最大程度为止,术后复查DSA。1例需要支架辅助栓塞者,术前3 d给予阿司匹林300 mg/d,术后给予低分子肝素0.4 mL皮下注射,连用3 d。在术中不论有无发现脑血管痉挛,均加压维持动脉滴注罂粟碱150 mg(500 mL生理盐水稀释)。术后每天除行腰大池引流术释放血性脑脊液外,常规静脉应用罂粟碱100 mg+生理盐水50 mL缓慢微泵注射(0.5 mL/min);低分子右旋糖酐500 mL/d静脉 滴注;20%人血白蛋白50 mL/次静脉滴注,2次/d;多巴胺40 mg+生理盐水50 mL缓慢微泵注射(1 mL/min,血压调控140~160/95~100 mmHg),疗程为2周。 1.3.4 术后处理
所有病例在术后行1次以上CT平扫+1次CTA检查,以了解颅内情况,有无脑水肿、脑缺血及颅内血肿形成,以及动脉瘤夹闭及栓塞情况。常规给予3H治疗,输液量2.5~3.5 L/d;小剂量20%甘露醇125 mL,2次/d,并给予钙离子通道拮抗剂尼莫地平5 mL/h持续泵入,防止脑血管痉挛,如血压低,可用多巴胺2 μg/(kg·min),维持血压高于基线20%~30%,中心静脉压(CVP)≥8~10 mmHg,肺毛细血管楔压(PCWP)≥12 mmHg。对27例SAH者,术后给予持续的腰大池引流术释放血性脑脊液。4例患者术后出现脑积水(显微夹闭手术组3例,介入治疗组1例),给予持续腰大池引流术7~14 d,患者症状逐渐缓解后出院。 1.4 术后随访和预后评估
术后3、6个月及1年以电话联系及来院复查的方式随访,复查CTA检查。按照GOS评分评估预后。 2 结果 2.1 并发症
术后严密观察患者病情变化,肢体痛温觉障碍10例,偏瘫7例,缄默症2例,精神异常15例,大小便障碍8例。4例患者术后出现脑积水,腰大池持续引流缓解。 2.2 即刻影像结果
夹闭组22例患者23个动脉瘤完全夹闭,2个夹闭不全,1例载瘤动脉闭塞;介入组10例患者6例致密栓塞,1例瘤内栓塞,3例载瘤动脉闭塞。 2.3 近期疗效及随访结果
术后平均随访12(6~24)个月,动脉瘤复发者2例(6%)。预后GOS评分,22例恢复良好,5例中残,5例重残,无死亡病例。4例载瘤动脉闭塞者中残2例,重残2例。 2.4 典型病例
典型病例1:女性,45岁,因“突发意识障碍3 h余” 入院。入院查体:神智呈昏睡状态。血压153/98 mmHg,双侧瞳孔等大圆形3 mm,光反射存在。颈阻征(+),kernig征(+),病理征未引出。入院CT示:CT示大脑鞍上池、环池、纵裂池及双侧外侧裂池广泛蛛网膜下腔出血。CTA示:右侧大脑前动脉A2段末A3起始(膝段)见一囊性动脉瘤,瘤体大小约6.7 mm×7.3 mm,瘤颈3.5 mm,其上有1小阜存在,并有第3支大脑前动脉(图 1A)。右侧大脑前动脉水平段较对侧细小,右侧大脑后交通动脉未见显示。于入院第2天先行血管内治疗,术中发现双侧颈内动脉颈段及海绵窦段迂曲,A1段发育纤细,右侧大脑前动脉A3段发出的动脉瘤经前交通动脉由双侧A1段供血。将导引导管置于右侧颈内动脉C3段水平,分别将2条微导管及微导丝塑形后试图送入动脉瘤瘤腔内,均未能到达。为保证安全,遂转行显微手术夹闭治疗。术中沿纵裂解剖达胼胝体,见右侧大脑前动脉膝段有一动脉瘤大小约为7 mm×5 mm,用2枚动脉瘤夹(B.BRAUN公司)夹闭动脉瘤颈(图 1B)。术后CTA检查动脉瘤夹闭满意,载瘤动脉保留满意,血流通畅(图 1C)。术后患者症状好转,于1周后出院。术后8个月复查CTA示原动脉瘤区域动脉瘤复发,遂转外院治疗(图 1D)。
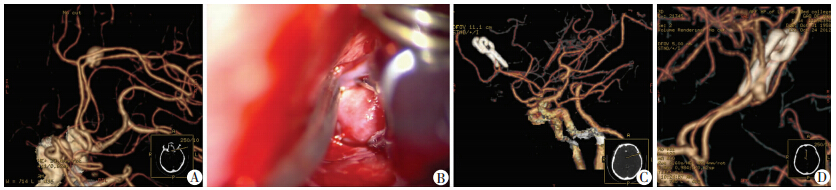 |
| A:术前CTA示右侧大脑前动脉A2段末A3起始(膝段)见一囊性动脉瘤,其上有一小阜存在,并有第3支大脑前动脉;B:术中探查见动脉瘤在另一支A3分支(靠右下)有残留,分离瘤体,用一长6 mm动脉瘤夹予以夹闭;C:术后CTA示右侧大脑前动脉A3段区域见一金属夹影,动脉瘤消失,载瘤动脉通畅,但明显痉挛;D:术后8个月复查CTA示原动脉瘤区域动脉瘤复发 图 1 显微手术夹闭治疗大脑前动脉远端动脉瘤典型病例 |
典型病例2:男性,20岁,因“车祸伤后21 d,突发剧烈头痛伴恶心呕吐呼之不应3 h”入院。入院查体:半昏迷,双侧瞳孔等大形圆约3 mm,对光反射灵敏。颈阻征(+),kernig征(+)。20 d前车祸伤,肺挫伤与颅脑损伤重。外院CT示:左侧急性硬膜下血肿,血肿量较多 ,脑中线偏移明显。急诊行血肿清除+去骨瓣减压术。术后CTA示:术前CTA、DSA示右侧大脑前动脉A4段末宽颈动脉瘤,动脉瘤较小(2.5 mm×3.4 mm),与载瘤动脉关系密切(图 2A、B)。于入我院后第3天行介入栓塞治疗,将导引导管置于右侧颈内动脉C3段水平并保持稳定,将微导管塑性后小心送入动脉瘤瘤腔内,依次填塞5枚(helical coils eV3 Neurovascular,Irvine,CA)弹簧圈。术后造影显示动脉瘤栓塞可,但载瘤动脉闭塞(图 2C)。2年后复查CTA:动脉瘤栓塞可,载瘤动脉不显影,有脑梗死形成,合并颅骨缺损和脑积水(图 2D)。
 |
| A、B:分别为术前CTA、DSA表现,示右侧大脑前动脉A4段末宽颈动脉瘤;C:术后DSA示动脉瘤不显影,载瘤动脉闭塞;D:术后复查CTA示大脑前动脉A4段远端不显影,有脑梗死形成,合并颅骨缺损和脑积水 图 2 介入栓塞治疗大脑前动脉远端动脉瘤典型病例 |
DACAA在临床较少见,占全部颅内动脉瘤的1.5%~9%,女性患者多见,本组占同期颅内动脉瘤的3.3%,男女比为1 ∶1.29,与文献[2, 3, 4]报道相似。
DACAA以A3段动脉瘤最常见,发病率占69%~72%,其次为A2段动脉瘤占5%~22%;而A4、A5段动脉瘤发病率较低仅占8%,本组病例中A3段动脉瘤为18个(50%),A2段动脉瘤12个(33%),A4段3个(8%),与以往的文献报道类似[3, 4]。DACAA以囊状动脉瘤多见,且体积通常较小,一般为5~8 mm[5],50%以上的破裂动脉瘤直径<7 mm[6]。本组36个动脉瘤以囊状动脉瘤多见,直径为2.3~11.7 mm,不规则形态20个(56%)。宽颈动脉瘤占多数,动脉瘤体颈比<1.12为64%,>1.12为36%。DACAA常伴颅内其他位置动脉瘤,但本组仅有4例(13%),少于文献[2]报道的38.5%~58%,可能与本组的例数较少有关。
尽管目前学术界认为数字减影造影(DSA)仍是诊断血管性疾病的金标准,但近年来计算机断层扫描造影术(CTA)作为无创、安全、快速的检查方式,有取代DSA的趋势,尤其是应用于颅内动脉瘤的急诊诊断中。通过本组资料,我们认为CTA完全可以对DACAA患者做出准确评估,了解胼周动脉的数量,确定责任动脉,以及动脉瘤的准确位置、大小、数目、形态指向,瘤颈宽窄,动脉瘤相对胼胝体的位置,毗邻血管的形态走向,以及动脉瘤至脑皮层表面及颅骨的距离等。特别是A2、A3段动脉瘤,利于手术骨窗的设计和到达载瘤动脉和动脉瘤颈角度的选择。因而可以单独应用于动脉瘤的术前诊断和术后随访[7]。
DACAA的治疗方式有直接手术夹闭和血管内治疗两种。由于纵裂池和胼胝体池狭窄、扣带回之间粘连非常紧密、纵裂内血肿破坏了正常的血管解剖关系等因素,使得DACAA手术夹闭难度较大,对操作者技术要求高。DACAA手术入路可以分为经翼点入路和经额部纵裂入路,也可以采用翼点联合纵裂入路。我们治疗的病例多选择额或/和顶纵裂入路,其中23个动脉瘤完全夹闭,2个夹闭不全,1例载瘤动脉闭塞,术后并发症较多,包括脑积水、血管痉挛、脑梗死及肢体瘫痪、缄默症及认知障碍等,并存在一定复发率。在处理上我们的体会如下:①术前行腰大池引流。因为腰大池引流术可以明显降低患者的颅内压,缩小脑容积,减少牵拉脑组织的力量和对脑组织的压迫,使手术野的显露更清楚,术者操作更方便[8];②处理多发DACAA,
应优先处理破裂出血的动脉瘤,在术中分离出多发动脉瘤共同的载瘤动脉之后再分别进行夹闭,以便于对于大脑前动脉远端未破裂动脉瘤的保护;③处理合并颅内血肿的DACAA,由于较大的颅内血肿可能会减少手术操作的空间,因此清除部分颅内血肿可以获得更好的手术空间,但需要注意的是其操作难度较大,可能会造成动脉瘤的破裂;④处理额前动脉的DACAA,由于其位于胼胝体膝部的下方,最好的方式是切除胼胝体来完成暴露;⑤当载瘤动脉成为DACAA瘤体一部分或宽颈动脉瘤时,在分离和夹闭动脉瘤的过程中,锐性分离减少动脉瘤的张力;⑥如发现术中夹闭不全或怀疑夹闭载瘤动脉,需及时行术中调整。有条件的医院最好行术中B超、DSA造影或CTA检查证实。
尽管目前手术夹闭作为首选的治疗方式,但近年有文献报道DACAA的介入治疗获得较好的疗效[5, 9]。DACAA因其特殊的解剖位置使得血管内治疗的难度较其他位置的颅内动脉瘤要大,相较手术夹闭治疗,血管内治疗对临床状况较差、手术夹闭风险较大及动脉瘤瘤颈较窄者有一定的优势[9, 10]。所以,在目前的治疗手段中,介入栓塞治疗仍然是有效的治疗方法,如治疗瘤体较小的动脉瘤、瘤颈相对较宽的动脉瘤、分支的起源靠近颅底的动脉瘤、载瘤动脉管径较窄和位置较深的动脉瘤等。黄清海等[11] 报道了29例DACAA的血管内介入治疗结果,技术成功率达到96.6%(28例); 包括载瘤动脉闭塞3例,瘤内栓塞25例,动脉瘤致密栓塞22例(88.0%)。本组病例中,栓塞治疗12例,其中2例栓塞失败转行手术夹闭,10例栓塞治疗成功,其中6例致密栓塞,1例瘤内栓塞,3例载瘤动脉闭塞。我们分析瘤内栓塞及载瘤动脉闭塞的原因可能有:①DACAA位置较远,微导管很难到位且不易保持稳定,不易进行瘤内致密栓塞;②DACAA多为小型宽颈动脉瘤,使得瘤内弹簧圈填塞较为困难,易导致动脉瘤栓塞不全;③对DACAA瘤体真实大小的误判等。根据以上情况,我们总结的操作技术要点如下:①微导管的准确塑形。将微导管塑形成“J”型及使用更柔软、数量更少的弹簧圈,或将微导管塑形成“S”型以稳定微导管顶端[9];②保持微导管的稳定,由于大脑前动脉远段动脉瘤的血管径路迂曲延长,其与常规动脉瘤栓塞技术的不同在于导引导管应置于颈内动脉远端,以达到进一步稳定微导管的目的;③使用辅助措施,如支架辅助技术可能对宽颈动脉瘤会取得更满意的效果。
值得注意还有治疗后的再出血。据报道,不论血管内治疗还是手术夹闭,大脑前动脉远段动脉瘤治疗后再出血的几率都比其他部位动脉瘤高[12]。我们治疗组的术后随访中未发现有动脉瘤再通及破裂再次出血的情况,这可能由于载瘤动脉管径窄且位于远端,血管壁受到的血流的剪切力较小有关。
| [1] | Suzuki S, Kurata A, Yamada M, et al. Outcomes analysis of ruptured distal anterior cerebral artery aneurysms treated by endosaccular embolization and surgical clipping[J]. Interv Neuroradiol, 2011, 17(1): 49-57. |
| [2] | Sekerci Z, Sanli M, Ergun R, et al. Aneurysms of the distal anterior cerebral artery: a clinical series[J]. Neurol Neurochir Pol, 2011, 45(2): 115-120. |
| [3] | Park K Y, Kim B M, Lim Y C, et al. The Role of Endovascular Treatment for Ruptured Distal Anterior Cerebral Artery Aneurysms: Comparison with Microsurgical Clipping[J]. J Neuroimaging, 2013, doi: 10.1111/jon.12073. |
| [4] | Navarro R, Chao K, Steinberg G K. Microsurgical management of distal anterior cerebral artery aneurysms: from basic to complex, a video review of four cases[J]. Acta Neurochir (Wien), 2013, 155(11): 2115-2119. |
| [5] | Park H S, Kwon S C, Kim M H, et al. Endovascular Coil Embo-lization of Distal Anterior Cerebral Artery Aneurysms: Angiographic and Clinical Follow-up Results[J]. Neurointervention, 2013, 8(2): 87-91. |
| [6] | Lehecka M, Lehto H, Niemela M, et al. Distal anterior cerebral artery aneurysms: treatment and outcome analysis of 501 patients[J]. Neurosurgery, 2008, 62(3): 590-601. |
| [7] | Lehecka M, Dashti R, Hernesniemi J, et al. Microneurosurgical management of aneurysms at A4 and A5 segments and distal cortical branches of anterior cerebral artery[J]. Surg Neruol, 2008, 70(4): 352-367. |
| [8] | 王珏基, 袁坚列, 陈杰, 等. Hunt-Hess Ⅰ~Ⅲ级动脉瘤性蛛网膜下腔出血早期手术术前腰大池外引流的临床观察[J]. 中华神经外科杂志, 2011, 27(3): 271-274. |
| [9] | Oishi H, Nonaka S, Yamamoto M, et al. Feasibility and efficacy of endovascular therapy for raptured distal anterior cerebral artery aneurysms[J]. Neurol Med Chir (Tokyo), 2013, 53(5): 304-309. |
| [10] | 蒋宇钢, 向军, 朱海东, 等. 颅内动脉瘤治疗方案的比较[J]. 医学与哲学, 2005, 26(22): 9-12. |
| [11] | 黄清海, 许奕, 洪波, 等. 远侧大脑前动脉动脉瘤的血管内栓塞治疗[J]. 中国微侵袭神经外科杂志, 2009, 14(9): 399-402. |
| [12] | Vora N, Thomas A J, Gupta R, et al. Endovascular treatment of distal anterior cerebral artery aneurysms: technical results and review of the literature[J]. J Neuroimaging, 2010, 20(1): 70-73. |



